
16.(2010.浙江台州)现有甲、乙、丙三种金属,分别与空气和氧气反应,现象如下表所示:
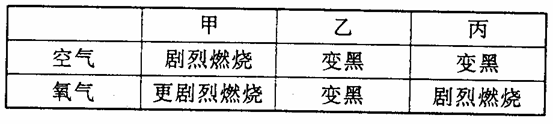
据以上信息,这三种金属活动性由强到弱
A.甲>丙>乙 B.甲>乙>丙 C.乙>丙>甲D.丙>乙>甲
答案:A
21.(2010.浙江杭州)铁制品在通常情况下很易生锈,制造时往往在铁制品表面电镀一层铜起防锈作用。下列说法正确的是
A.镀铜铁制品不可以在弱酸性条件下使用
B.镀铜铁制容器可盛硝酸银溶液
C.镀铜铁制品不易生锈的原因之一是使铁隔绝了空气
D.镀铜铁制品是一种合金
答案:C
2010.浙江湖州) 7.上海世博会上的“冰壶”展馆(如图)体现了芬兰的生态创新。所
7.上海世博会上的“冰壶”展馆(如图)体现了芬兰的生态创新。所
有的建筑材料都是在环保理念上经过精挑细选的,其中采用的纸
塑复合材料属于
A.金属材料 B.无机非金属材料
C有机合成材料 D.新型超导材料
答案:B
2010.浙江杭州) 1.下列用品中,由有机合成材料制成的是( )
A.玻璃杯 B.瓷碗 C.木桌 D.塑料瓶
答案:D
14.①金、银、铜 ②化学性质稳定 ③大
[10福建宁德]6.往ZnSO4和CuSO4的混合溶液中加入过量的铁粉,充分反应过滤,滤纸上剩余物质是
A.Fe和Cu B.Cu C.Zn D.Fe
[10新疆]13.废旧手机的某些部件中含有Mg、Al、Cu、Ag等金属,为了回收重金属,将旧手机的部件粉碎并浸入足量稀硫酸中充分反应过滤,所得固体中含有的金属是
A.Mg、Al B.Cu、Ag C.Al、Cu D.Mg、Ag
[10桂林25.]小红同学为研究金属腐蚀的条件,用细尼龙线将三根大小相同的铁钉分别固定在下图所示的三个液面高度相同的相同装置中,放置一星期后观察现象。下列描述错误的是
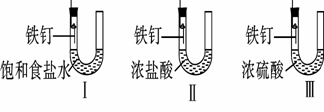
A.装置Ⅰ的铁钉一侧的液面一定会上升 B.装置Ⅰ、Ⅱ中的铁钉都被腐蚀
C.比较铁钉一侧的液面,装置Ⅱ比装置I的高 D.装置Ⅲ中的铁钉几乎没被腐蚀 (10天津市21).有X、Y、Z三种金属,能发生以下反应:Y+2 XNO3== Y(NO3)2+2X, Z+YSO4== ZSO4+Y,则X、Y、Z三种金属活动性由强至弱的顺序是_____________________。
答案:Z Y X
(10天津市22).铝、铁、铜是我们生活中常见的金属。
(1)下列生活用品中,主要是利用金属具有良好导热性的是_______________。(填序号)
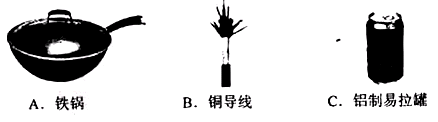
(2)铝具有很好的抗腐蚀性能,原因是____________。
(3)在高温下,利用焦炭和氧气反应生成的一氧化碳可把铁从铁矿石里还原出来。某炼铁厂现用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是____t。(计算结果精确到0.1)
(4)工人师傅切割铁板时,用硫酸溶液在铁板上画线可留下红色的印迹。其反应的化学方程式为__________________________。
答案:(1)A铝和氧气反应在其表面反应生成一层致密的氧化铝薄膜,从而保护里层的铝不再和氧气反应
13.(10泸州19).(1)工业炼铁是用CO和Fe2O3反应制得铁,其化学方程式为
3CO+Fe2O3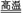 2Fe+3CO2 。
2Fe+3CO2 。
(2)根据铁、铜、铝三种金属的活动顺序判断下列化学方程式正确的是 ③ (填序号)。
①3Fe+2AlCl3=3FeCl2+2Al ②3Cu+2AlCl3=3CuCl2+2Al ③Fe+CuCl2=FeCl2+Cu
(3)某实验室废液中含有HCl、FeCl2和CuCl2等物质,若向其中加入稍过量的铁粉,充分反应后过滤,则滤渣中含有 Fe和Cu (填化学式)。
[10福建宁德] 7.2010年上海世博会中国馆--“东方之冠”给人强烈的视觉冲击,它的主体结构是由四根钢筋混凝土制作的核心筒。其中的钢属于
7.2010年上海世博会中国馆--“东方之冠”给人强烈的视觉冲击,它的主体结构是由四根钢筋混凝土制作的核心筒。其中的钢属于
A.非金属材料 B.合成材料
C.天然材料 D.金属材料
[10湖北十堰]1.2010年上海世博会中国馆一“东方之冠”给人强烈的视觉冲击,它的主体结构大量使用钢材,其中钢与下列哪种物质属同类材料:
A.石器 B.青铜器 C.高分子材料 D.天然纤维
[10乌鲁木齐市]14.人们常说的“五金”是指“金、银、铜、铁、锌”,根据所学知识判断,不能与盐酸反应的金属是 ① (填名称)。世界上常用黄金作金融储备、货币等,其原因是 ② 。黄铜是铜锌合金,其硬度比纯铜 ③ (填“大”、“小”或“相同”)。
12.(10泸州15).(1)铝在氧气中燃烧的化学方程式为
4Al+3O2  Al2O3 ;此反应属于基本反应类型中的 化合 反应。
Al2O3 ;此反应属于基本反应类型中的 化合 反应。
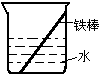 (2)如右图所示,将部分铁棒插入水中,部分露在干燥的空气中,试判断铁棒哪一部分生锈更快 ① (填序号)。
(2)如右图所示,将部分铁棒插入水中,部分露在干燥的空气中,试判断铁棒哪一部分生锈更快 ① (填序号)。
①插入水中的那部分铁棒生锈更快
②露在干燥的空气中那部分铁棒生锈更快
③两部分铁棒生锈一样快
11.(10泸州9).下列常见材料中,属于金属材料的是 ( )
A.不锈钢 B.玻璃钢
C.大理石 D.“塑料王”聚四氟乙烯
31.(10,娄底31)Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
|
|
加入稀硫酸的质量(g) |
充分反应后剩余固体的质量(g) |
|
第1次 |
20 |
17.4 |
|
第2次 |
20 |
14.8 |
|
第3次 |
20 |
12.2 |
|
第4次 |
20 |
12.0 |
|
第5次 |
20 |
m |
试回答下列问题:
(1)上述表格中m的值为 70 ;
(2)黄铜样品中锌的质量分数为 71 ;
(3)所用稀硫酸中硫酸的质量分数是多少? 72
31题: 70. 12.0(或12) 71. 40% (每空1分)
72.[共3分,化学方程式1分,计算过程1分,结果1分(无计算过程不给分)]
解:设所用稀硫酸中硫酸的质量分数为x,据题意得:
Zn + H2SO4 = ZnSO4 + H2↑ …………1分
65 98
20g-17.4g=2.6g 20g·x
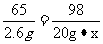 …………1分
…………1分
x=19.6% …………1分
答:所用稀硫酸中溶质的质量分数为19.6%。(合理解法均给分)
(10,威海10)应用广泛的金属
没有金属,生活是难以想象的。请你根据所学知识回答下列问题:
(1)只要观察一下你的周围,你就能理解金属是多么有用。在一百余种元素中,金属元素的种类比非金属元素的种类________。由于金属具有特殊的组成和结构,决定了金属具有优良的物理性能。你认为金属比较重要的两种物理性质是____________________________。
现代社会以各种金属为支撑,其中用量最大、应用最广泛的金属是_________。地壳中含量最丰富的金属是__________。
(2)尽管金属有非常优良的物理性质,但应用金属经常遇到的问题是大多数金属化学性质活泼,易与其它物质发生反应。例如,大多数金属暴露在空气中易被腐蚀,这是因为金属易与氧气发生反应,该反应的实质是_________反应。从金属的原子结构看,你认为金属易与其它物质发生反应的根本原因是______________________________________________。
(3)我国早在春秋战国时期就开始炼铁、应用金属铁。请你用化学方程式表示用一氧化碳还原氧化铁的化学反应原理______________________________________。
多 导电性、导热性(或延性、展性、硬度大等) 铁 铝
(2)(共2分,每空l分)
|
(3)(1分) Fe2O3+3CO====2Fe+3CO2
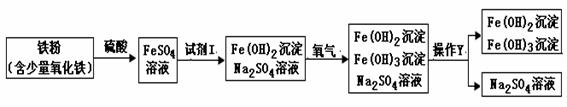 (10龙岩市15).(10分)下图是氧化沉淀法生产复印用高档Fe3O4粉的部分工艺流程简图。
(10龙岩市15).(10分)下图是氧化沉淀法生产复印用高档Fe3O4粉的部分工艺流程简图。
(1)试剂I和操作Y的名称分别为________________、___________________。
(2)硫酸与氧化铁的反应为__________________________________。
(3)往铁粉(含少量氧化铁)中加入硫酸,除铁、氧化铁与硫酸发生反应外,一定还发生其它反应。作出这种 判断的依据是_______________________________。
判断的依据是_______________________________。
(4)某铁矿主要成分为Fe3O4,利用CO将该物质中 铁还原出来的方程式为___________。答案
铁还原出来的方程式为___________。答案
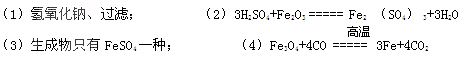
22.(10,娄底22)钢铁在生产、生活中有广泛的用途。建造上海世博会的中国馆--“东方之冠”的核心筒 就是用四根巨型钢筋混凝土制成的,其中用了大量的钢铁。
就是用四根巨型钢筋混凝土制成的,其中用了大量的钢铁。
(1)钢铁属于 30 (填“纯净物”或“混合物”);
(2)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁Fe2O3)、空气等为主要原料炼铁,请写出一氧化碳与氧化铁在高温下反应的化学方程式: 31 ;
(3)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的 32 和 33 共同作用的结果;
(4)为了防止钢铁锈蚀,人们常采用 34 的方法(任写一种)来达到目的。
22题: 30. 混合物 31. 3CO+Fe2O3 2Fe+3CO2 32. 氧气(O2)(或水)
2Fe+3CO2 32. 氧气(O2)(或水)
33. 水(H2O)(或氧气) 34. 喷漆(合理答案均可)
(10,浙江衢州36.)构建知识网络是一种重要的学习方法。图为某同学绘制的铁的化学性质网络示意图。请分析回答下列问题:
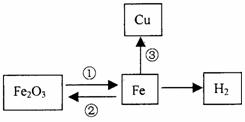 (1)反应①中可用 ▲ (填化学式)作还原剂;
(1)反应①中可用 ▲ (填化学式)作还原剂;
(2)反应②导致每年有大量的钢铁锈蚀,为阻止该反应的发生,人们常采用在钢铁表面涂刷油漆或镀上其它金属等方法。这两种方法的共同原理是阻止钢铁与 ▲ 接触;
(3)早在西汉时期,我国劳动人民就利用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”,即反应③,若用该方法制得铜16千克,理论上需要溶质质量分数为10%的硫酸铜溶液多少千克?
(1)CO(或H2或C)(2分)
(2)氧气和水(2分)
(3)设需要10%的硫酸铜溶液的质量为x
Fe + CuSO4===FeSO4+Cu (1分)
160 64
10%x 16千克
160﹕64=10%x﹕16千克 (2分)
x=400千克 (1分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com