
9.“绿色试剂”双氧水可作为矿业废液消毒剂,如消除采矿业废液中的氰化物(如KCN),反应的化学方程式为;KCN+H2O2+H2O=A+NH3↑
回答下列问题:
(1)生成物A的化学式为____________。
(2)在标准状况下有0448 L氨气生成,则转移的电子数为____________。
(3)反应中被氧化的元素为____________。
(4)H2O2被称为“绿色氧化剂”的理由是- 。
8.(2010年浙江杭州一中)Na2FeO4是一种高效多功能水处理剂,应用前景广阔,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应下列说法不正确的是
( )
A.Na2O2在反应中只作氧化剂
B.O2是氧化产物
C.Na2FeO4既是氧化产物又是还原产物
D.2 mol FeSO4发生反应时,共有8 mol电子转移
7.(2009年江苏镇江)在下列溶液中,各组离子一定能够大量共存的是
( )
A.含Fe3+的溶液中:K+、H+、Cl-、MnO4-
B.使石蕊试液变红的溶液:Na+、Cl-、SO42-、Fe3+
C.含有大量ClO-的溶液:H+、Mg2+、I-、SO42-
D.c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-
6.下列反应的离子方程式正确的是
( )
A.Fe3O4与稀盐酸反应:
Fe3O4+8H+=Fe2++2Fe3++4H2O
B.将Cu片插入AgNO3溶液中:Cu+Ag+=Cu2++Ag
C.过氧化钠溶于水中:Na2O2+H2O=2Na++2OH-+O2↑
D.实验制取Cl2:MnO2+4H++4Cl- MN2++2Cl2↑+2H2O
MN2++2Cl2↑+2H2O
5.将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
下列有关说法正确的是
( )
A.还原性Cr3+>Fe2+>SO2
B.氧化性Cr2O72->SO2>Fe3+
C.Cr2O72-能将Na2SO3氧化成Na2SO4
D.两个反应中Fe2(SO4)3均作还原剂
4.下列叙述正确的是
( )
A.发生化学反应时失去电子越多的金属原子,还原能力越强
B.金属阳离子被还原后,一定得到该元素的单质
C.核外电子总数相同的原子,一定是同种元素的原子
D.能与酸反应的氧化物,一定是碱性氧化物
3.(2010年青岛联考)ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,在以上反应中,NaClO3和Na2SO3的物质的量之比为
( )
A.1∶1
B.2∶1
C.1∶2
D.2∶3
2.(2009年临沂质检)离子反应、复分解反应、置换反应和氧化还原反应之间可用下列集合关系表示,其中正确的是
( )

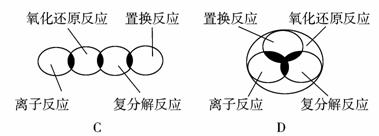
1.(2009年广州)三氟化氮(NF3)是一种无色无味的气体,它是氨和氟(F2)在一定条件下直接反应得到:
4NH3+3F2=NF3+3NH4F,下列有关NF3的叙述正确的是
( )
A.NF3中的原子最外层均达8电子
B.NF3的还原性比NH3强
C.NF3的氧化性比F2强
D.每生成1 mol NF3转移6 mol电子
14.(13分)(2009·全国卷Ⅰ)化合物H是一种香料,存在于金橘中,可用如下路线合成:

回答下列问题:
(1)11.2 L(标准状况)的烃A在氧气中充分燃烧可以产生88 g CO2和45 g H2O.A的分
子式是__________;
(2)B和C均为一氯代烃,它们的名称(系统命名)分别为_________________________;
(3)在催化剂存在下1 mol F与2 mol H2反应,生成3苯基1丙醇.F的结构简式是
________________________________________________________________________;
(4)反应①的反应类型是__________________________________________________;
(5)反应②的化学方程式为________________________________________________;
(6)写出所有与G具有相同官能团的G的芳香类同分异构体的结构简式:
________________________________________________________________________.
解析:(1)88 g CO2为2 mol,45 g H2O为2.5 mol,标准状况的烃11.2 L,即为0.5 mol,
所以烃A中含碳原子数为4,H原子数为10,则化学式为C4H10.
(2)C4H10存在正丁烷和异丁烷两种,但从框图上看,A与Cl2光照取代时有两种产物,
且在NaOH醇溶液作用下的产物只有一种,则只能是异丁烷.取代后的产物为2甲基
1氯丙烷和2甲基2氯丙烷.
 (3)F可以与Cu(OH)2反应,故应为醛,与H2之间以1∶2加成,则应含有碳碳双键.从
(3)F可以与Cu(OH)2反应,故应为醛,与H2之间以1∶2加成,则应含有碳碳双键.从
生成的产物3苯基1丙醇分析,F的结构简式为
(4)反应①为卤代烃在醇溶液中的消去反应.
(5)F被新制的Cu(OH)2氧化成羧酸,D至E与信息相同的条件,则类比可不难得出E
 的结构为
的结构为
E与G在浓硫酸作用下可以发生酯化反应.
(6)G中含有官能团有碳碳双键和羧基,可以将官能团作相应的位置变换而得出其芳香
类的同分异构体.
答案:(1)C4H10 (2)2甲基1氯丙烷 2甲基2氯丙烷
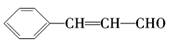
(3) (4)消去反应


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com