
28£®(Õã½Ê¡¿ª»¯ÖÐѧ08Äê1Ô¸ßÈýÄ£Äâ)ÏÖÓг£ÎÂÏÂ0.1 mol¡¤L-1µÄ´¿¼îÈÜÒº¡£
¡¡(1)ÏÂÁд¿¼îÈÜÒºÖÐÀë×ÓŨ¶ÈÖ®¼äµÄ¹ØϵÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡ ¡£
A£®c(H+)+c(Na+)=c(OH-)+c(HCO3-)+2c(CO32-)
B£®c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
C£®c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
D£®c(CO32-)=c(HCO3-)+c(H2CO3)
¡¡(2)´¿¼îÈÜÒº³Ê¼îÐÔ£¬ÆäÔÒòÊÇ(ÓÃÀë×Ó·½³Ìʽ±íʾ)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £¬ÑéÖ¤´¿¼îÈÜÒº³Ê¼îÐÔµÄʵÑé·½·¨(¼òÊö²Ù×÷¹ý³Ì)£º ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡(3)´¿¼îÈÜÒºÓëÂÈ»¯ÂÁÈÜÒº»ìºÏÓдóÁ¿ÅÝÄÉú³É£¬ÆäÔÒòÊÇ(ÓÃÀë×Ó·½³Ìʽ±íʾ) ¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡(4)ijͬѧÈÏΪ´¿¼îÈÜÒºÖÐNa2CO3µÄË®½âÊÇ΢ÈõµÄ£¬·¢ÉúË®½âµÄCO32-²»³¬¹ýÆä×ÜÁ¿µÄ10%¡£ÇëÄãÉè¼ÆʵÑéÖ¤Ã÷¸ÃͬѧµÄ¹ÛµãÊÇ·ñÕýÈ·¡£ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡
Ñ¡Ôñ´ð°¸ÌîÈë±í¸ñÄÚ
27£®(Õã½Ê¡¿ª»¯ÖÐѧ08Äê1Ô¸ßÈýÄ£Äâ)ÏÂÁÐÐðÊöÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡ A£®95 ¡æ´¿Ë®µÄpH£¼7£¬ËµÃ÷¼ÓÈȿɵ¼ÖÂË®³ÊËáÐÔ
¡¡¡¡¡¡ B£®pH = 3µÄ´×ËáÈÜÒº£¬Ï¡ÊÍÖÁ10±¶ºópH = 4
¡¡¡¡¡¡ C£®0.2 mol¡¤L£1µÄÑÎËᣬÓëµÈÌå»ýË®»ìºÏºópH = 1(ºöÂÔÌå»ýµÄ±ä»¯)
¡¡ ¡¡ D£® Na2CO3ÈÜÒºÖУºc(Na+) + c(H+) = c(HCO3-) +c(CO32-) + c(OH-)
26£®(Õã½Ê¡¿ª»¯ÖÐѧ08Äê1Ô¸ßÈýÄ£Äâ)ÏÂÁÐÊÂʵÖУ¬ÄÜÖ¤Ã÷NH3¡¤H2OÊÇÈõµç½âÖʵÄÊÇ¡¡¡¡¡¡¡¡¡¡
A£®³£ÎÂʱ£¬Ï¡°±Ë®µÄµ¼µçÐÔ±ÈÏ¡NaOHÈÜÒºµÄµ¼µçÐÔÈõ
B£®³£ÎÂʱ£¬µÈŨ¶ÈµÈÌå»ýµÄ°±Ë®ºÍÑÎËá»ìºÏ£¬»ìºÏÒºpHСÓÚ7
C£®1mol¡¤L£1µÄ°±Ë®¿ÉÒÔʹ·Ó̪ÊÔÒº±äºìÉ«¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®Òº°±²»µ¼µç
25£®(Õã½Ê¡¿ª»¯ÖÐѧ08Äê1Ô¸ßÈýÄ£Äâ)¶þÔªËáH2AÔÚË®Öз¢ÉúµçÀ룺H2A H++HA£ºÍHA£
H++HA£ºÍHA£ H++A2-£¬ÔòÏÂÁÐÎïÖʵÄË®ÈÜÒºÖдæÔڵĹØϵʽ²»ÕýÈ·µÄÊÇ
H++A2-£¬ÔòÏÂÁÐÎïÖʵÄË®ÈÜÒºÖдæÔڵĹØϵʽ²»ÕýÈ·µÄÊÇ
A£®NaHA£ºc(Na+)>c(HA£)>c(OH£)>c(H+)
B£®NaHA£ºc(Na+)= c(A2£)+ c(HA£)
C£®Na2A£ºc(Na+)> c(A2£)>c(OH£)>c(H+)
D£®H2A£ºc(H+)= c(HA£)+ 2c(A2£)+ c(OH£)
24¡¢(Õã½Ê¡¿ª»¯ÖÐѧ08Äê1Ô¸ßÈýÄ£Äâ)ÎïÖʵÄÁ¿Å¨¶È¾ùΪ0.01mol¡¤L-1µÄHAºÍMOHÈÜÒº£¬pH·Ö±ðΪ3ºÍ12£¬½«Á½ÈÜÒºµÈÌå»ý»ìºÏºó£¬ËùµÃÈÜÒºµÄpHΪ¡¡¡¡¡¡
¡¡ A£®¡Ý7 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®Ò»¶¨´óÓÚ7 ¡¡¡¡¡¡¡¡C£®¡Ü7 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®¿ÉÄܵÈÓÚ7
23¡¢(Õã½Ê¡¿ª»¯ÖÐѧ08Äê1Ô¸ßÈýÄ£Äâ)25¡æʱ£¬pHΪ9µÄNa2CO3ÈÜÒººÍpHΪ5µÄFeCl3ÈÜÒºÖУ¬Ë®µÄµçÀë³Ì¶ÈµÄ´óС
A£®Ç°Õß´ó¡¡ ¡¡¡¡¡¡B£®Á½ÕßÏàµÈ ¡¡¡¡¡¡¡¡C£®ºóÕß´ó ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®ÎÞ·¨È·¶¨
0.03 mol Fe2O3¡ú0.06 mol Fe2+¡¡¡¡ µÃµç×Ó0.06 mol
2n mol H+¡ún mol H2¡¡¡¡¡¡¡¡¡¡¡¡ µÃµç×Ó0.3 mol£0.06 mol£½0.24 mol
Ëã³ön(H2)£½0.12 mol¡¡¡¡ (2·Ö)¡¡¡¡ V(H2)£½2.688 L¡¡¡¡¡¡¡¡¡¡¡¡ (1·Ö)
0.1 mol Al¡ú0.1 mol Al3+ ¡¡¡¡¡¡¡¡Ê§µç×Ó0.3 mol
22£®(Õã½¾ÅËùÖصãÖÐѧ¸ßÈýÄ꼶µ÷Ñп¼ÊÔ))ÏÖÓÐÒ»°üÂÁÈȼÁÊÇÂÁ·ÛºÍÑõ»¯Ìú·ÛÄ©µÄ»ìºÏÎÔÚ¸ßÎÂÏÂʹ֮³ä·Ö·´Ó¦£¬½«·´Ó¦ºóµÄ¹ÌÌå·ÖΪÁ½µÈ·Ý£¬½øÐÐÈçÏÂʵÑé(¼ÆËãpHʱ¼Ù¶¨ÈÜÒºÌå»ýûÓб仯)£º
¢ÙÏòÆäÖÐÒ»·Ý¹ÌÌåÖмÓÈë100 mL 2.0 mol¡¤L-1µÄNaOHÈÜÒº£¬¼ÓÈÈʹÆä³ä·Ö·´Ó¦ºó¹ýÂË£¬²âµÃÂËÒºµÄpH£½14£»
¢ÚÏòÁíÒ»·Ý¹ÌÌåÖмÓÈë140 mL 4.0 mol¡¤L-1µÄHClÈÜÒº£¬Ê¹¹ÌÌåÈ«²¿Èܽ⣬²âµÃ·´Ó¦ºóËùµÃÈÜÒºÖÐÖ»ÓÐH+¡¢Fe2+ºÍAl3+ÈýÖÖÑôÀë×ÓÇÒpH£½0¡£
¢Å¼ÆËãÕâ°üÂÁÈȼÁÖÐÂÁµÄÖÊÁ¿ºÍÑõ»¯ÌúµÄÖÊÁ¿¡£
¢Æ¼ÆËãʵÑé¢Ú²úÉúÆøÌåµÄÌå»ý(±ê×¼×´¿ö)¡£
´ð°¸£®¢ÅʵÑé¢ÙÖÐÓÃÈ¥n(NaOH)£½100 mL¡Á(2.0 mol¡¤L-1£1.0 mol¡¤L-1)£½0.1 mol
(1·Ö)
ÎÞÂÛÊÇAl»¹ÊÇAl2O3£¬ÓëNaOHÈÜÒº·´Ó¦ºó¶¼Éú³ÉNaAlO2£¬ÂÁÈȼÁÖÐ
n(Al)£½n(NaOH)¡Á2£½0.2 mol£¬ m(Al)£½5.4 g¡¡¡¡¡¡¡¡ ¡¡(2·Ö£¬Ëã³ö2.7 g¸ø1·Ö)
ʵÑé¢ÚËùµÃÈÜÒºÖУ¬¸ù¾Ý¡°µçºÉÊغ㡱ÓÐn(H+)+2¡Án(Fe2+)+3¡Án(Al3+)£½n(Cl£)
Ôòn(Fe2+)£½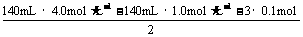 £½0.06 mol¡¡ (2·Ö)
£½0.06 mol¡¡ (2·Ö)
ÂÁÈȼÁÖÐn(Fe2O3)£½n(Fe2+)¡Á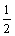 ¡Á2£½0.06 mol£¬m(Fe2O3)£½9.6
g
¡Á2£½0.06 mol£¬m(Fe2O3)£½9.6
g
(2·Ö£¬Ëã³ö4.8 g¸ø1·Ö)
¢Æ¸ù¾ÝÉÏÊö¼ÆËã½á¹û£¬·´Ó¦2Al+Fe2O3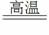 2Fe+Al2O3³ä·Ö½øÐкóËùµÃ¹ÌÌå»ìºÏÎïÖк¬0.08 mol AlºÍ0.12 mol Fe¡£¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
(1·Ö)
2Fe+Al2O3³ä·Ö½øÐкóËùµÃ¹ÌÌå»ìºÏÎïÖк¬0.08 mol AlºÍ0.12 mol Fe¡£¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
(1·Ö)
ʵÑé¢ÚÖÐËùµÃH2ÔÚ±ê×¼×´¿öÏÂÌå»ýΪ
V(H2)£½n(H2)¡Á22.4 L¡¤mol£1£½[n(Al)¡Á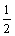 ¡Á
¡Á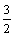 +n(Fe)¡Á
+n(Fe)¡Á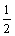 ]¡Á22.4 L¡¤mol£1£½2.688 L
]¡Á22.4 L¡¤mol£1£½2.688 L
(2·Ö)
»òÕß
È¡ÂÁÈȼÁµÄÒ»°ëÓá°µç×ÓÊغ㡱¼ÆË㣺
21£®
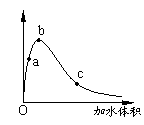 (Õã½¾ÅËùÖصãÖÐѧ¸ßÈýÄ꼶µ÷Ñп¼ÊÔ)Ò»¶¨Î¶ÈÏ£¬½«Ò»¶¨ÖÊÁ¿µÄ±ù´×Ëá¼ÓˮϡÊ͹ý³ÌÖУ¬ÈÜÒºµÄµ¼µçÄÜÁ¦±ä»¯ÈçÓÒͼËùʾ£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ
(Õã½¾ÅËùÖصãÖÐѧ¸ßÈýÄ꼶µ÷Ñп¼ÊÔ)Ò»¶¨Î¶ÈÏ£¬½«Ò»¶¨ÖÊÁ¿µÄ±ù´×Ëá¼ÓˮϡÊ͹ý³ÌÖУ¬ÈÜÒºµÄµ¼µçÄÜÁ¦±ä»¯ÈçÓÒͼËùʾ£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ
A£®a¡¢b¡¢cÈýµãÈÜÒºµÄpH£ºc£¼a£¼b
B£®a¡¢b¡¢cÈýµã´×ËáµÄµçÀë³Ì¶È£ºa£¼b£¼c
C£®ÓÃʪÈóµÄpHÊÔÖ½²âÁ¿a´¦ÈÜÒºµÄpH£¬²âÁ¿½á¹ûƫС
D£®a¡¢b¡¢cÈýµãÈÜÒºÓÃ1mol/LÇâÑõ»¯ÄÆÈÜÒºÖкͣ¬ÏûºÄÇâÑõ»¯ÄÆÈÜÒºÌå»ý£ºc£¼a£¼b
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com