
12.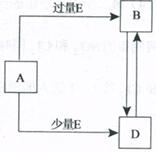 ŅŃÖŖA”¢B”¢D”¢E¾łĪŖ֊ѧ»Æѧ³£¼ūµ„ÖŹ»ņ»ÆŗĻĪļ£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾(²æ·Ö²śĪļĀŌČ„)”£
ŅŃÖŖA”¢B”¢D”¢E¾łĪŖ֊ѧ»Æѧ³£¼ūµ„ÖŹ»ņ»ÆŗĻĪļ£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾(²æ·Ö²śĪļĀŌČ„)”£
(1)ČōAŗĶEĪŖµ„ÖŹĒŅBĪļÖŹĪŖÓɼ«ŠŌ¼üŠĪ³ÉµÄ·Ē¼«ŠŌ·Ö×Ó”£
BµÄµē×ÓŹ½ĪŖ£ŗ”””””” £¬MµÄŌ×ÓŠņŹż±ČA“ó76£¬ŌņMĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµŚ”””” ÖÜĘŚ”””” ×唣ŹŌŠ“³öMµÄ×īøß¼ŪŃõ»ÆĪļÓėÅØŃĪĖį·“Ó¦µĆµ½µ„ÖŹĘųĢåCµÄ»Æѧ·“Ó¦·½³ĢŹ½£ŗ””””””””””””””””””””””””””””
 (2)ČōA”¢B”¢D”¢E¾łĪŖøßČŪµćµÄĪļÖŹĒŅE”¢DĪŖµ„ÖŹ£¬Š“³öA”śBµÄ»Æѧ·½³ĢŹ½£ŗ””””””””””””””””””””””””
”””””””””£DµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼£ŗ””””””””””””””””””””””””””
ӣ
(2)ČōA”¢B”¢D”¢E¾łĪŖøßČŪµćµÄĪļÖŹĒŅE”¢DĪŖµ„ÖŹ£¬Š“³öA”śBµÄ»Æѧ·½³ĢŹ½£ŗ””””””””””””””””””””””””
”””””””””£DµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼£ŗ””””””””””””””””””””””””””
ӣ
(3)ČōAĪŖæÉČÜŠŌĒæ¼ī(MOH)£¬EĪŖĶ¬Ö÷×åŌŖĖŲŠĪ³ÉµÄ³£¼ū·Ē½šŹō»ÆŗĻĪļ£¬ĒŅøĆ»ÆŗĻĪļÖŠĮ½ŌŖĖŲµÄÖŹĮæ±ČĪŖl£ŗ1£¬ŹŌŠ“³öA”śBµÄ»Æѧ·½³ĢŹ½£ŗ””””””””””””””””””””””””
“š°ø (1)O”Ć”ĆC”Ć”ĆO”””””” Įł£¬¢ōA””
 PbO2+4HCl£½PbCl2+Cl2”ü+2H2O
PbO2+4HCl£½PbCl2+Cl2”ü+2H2O
(2)SiO2+3C”””””””””” SiC+2CO”””” +14
(3)MOH+SO2£½MHSO3
11. (ÖŲĒģŹŠĪåĒų2009½ģøßČżĮŖæ¼) Š“³ö³żČ„ĻĀĮŠĪļÖŹÖŠµÄŌÓÖŹ(ĄØŗÅÄŚĪŖŌÓÖŹ)Ź±·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
(1)Na2CO3¹ĢĢå(NaHCO3)”””””””””””””””””””””””””””””””” £»
(2)SiO2(Al2O3)”””””””””””””””””””””””””””””””””””””””””” ”£
“š°ø£ŗ
(1)2NaHCO3
 ””Na2CO3 + CO2”ü
+ H2O””
””Na2CO3 + CO2”ü
+ H2O””
(2)Al2O3 + 6HCl £½2AlCl3 + 3H2O””
10. ĻĀĮŠ±ķŹöÕżČ·µÄŹĒ”””””””””””””””””””””””””””””””””””” ””””””””””””””””””(”””” )””””””””””””””””””””””””””””””””
A£®ČĖŌģøÕÓńČŪµćŗÜøߣ¬æÉÓĆ×÷øß¼¶ÄĶ»š²ÄĮĻ£¬Ö÷ŅŖ³É·ÖŹĒSiO2
B£®»Æѧ¼Ņ²ÉÓĆĀźč§ŃŠ²§Ä¦²Į¹ĢĢå·“Ó¦Īļ½ųŠŠĪŽČܼĮŗĻ³É£¬Āźč§µÄÖ÷ŅŖ³É·ÖŹĒAl2O3
C£®ĢįĒ°½Ø³ÉµÄČżĻæ“ó°ÓŹ¹ÓĆĮĖ“óĮæĖ®Äą£¬Ė®ÄąŹĒ¹čĖįŃĪ²ÄĮĻ
D£®ÓĆÓŚĻÖ“śĶØѶµÄ¹āµ¼ĻĖĪ¬µÄÖ÷ŅŖ³É·ÖŹĒøß“æ¶ČµÄ¹č
“š°ø C
9.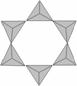
 1798Äź·Ø¹ś»Æѧ¼Ņ¶ŌĀĢÖłŹÆŗĶ×ęÄøĀĢ½ųŠŠ»Æѧ·ÖĪö·¢ĻÖĮĖīė”£ŅŃÖŖĀĢÖłŹÆŹĒŅ»ÖÖ³ŹĀĢÉ«µÄ¹čĖįŃĪ£¬æɱķŹ¾ĪŖBexAly[SimOn](x”¢y”¢m”¢n¾łĪŖ×ŌČ»Źż)£¬ĘäÖŠŅõĄė×Ó²æ·Ö½į¹¹ČēĻĀĶ¼ĖłŹ¾(ŅŃÖŖ””””
±ķŹ¾¹čĖįøłĄė×Ó
1798Äź·Ø¹ś»Æѧ¼Ņ¶ŌĀĢÖłŹÆŗĶ×ęÄøĀĢ½ųŠŠ»Æѧ·ÖĪö·¢ĻÖĮĖīė”£ŅŃÖŖĀĢÖłŹÆŹĒŅ»ÖÖ³ŹĀĢÉ«µÄ¹čĖįŃĪ£¬æɱķŹ¾ĪŖBexAly[SimOn](x”¢y”¢m”¢n¾łĪŖ×ŌČ»Źż)£¬ĘäÖŠŅõĄė×Ó²æ·Ö½į¹¹ČēĻĀĶ¼ĖłŹ¾(ŅŃÖŖ””””
±ķŹ¾¹čĖįøłĄė×Ó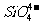 )£¬ĻĀĮŠĖµ·ØæĻ¶Ø²»ÕżČ·µÄŹĒ
)£¬ĻĀĮŠĖµ·ØæĻ¶Ø²»ÕżČ·µÄŹĒ
A. ŅõĄė×Ó»ÆѧŹ½ĪŖ£ŗ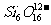
B. ĀĢÖłŹÆæÉÓĆŃõ»ÆĪļŠĪŹ½±ķŹ¾ĪŖ£ŗ3BeO”¤Al2O3”¤6SiO2
C. ĀĢÖłŹÆæɱķŹ¾ĪŖBe3Al2[Si3O12]
D. ĀĢÖłŹÆæÉČÜÓŚĒæ¼īŗĶĒā·śĖį
“š°ø£ŗAC
8. ĻĀĮŠĪļÖŹµÄ±ä»Æ£¬²»ÄÜĶعżŅ»²½»Æѧ·“Ó¦Ķź³ÉµÄŹĒ
A£®CO2”śH2CO3”” ”” B£®SiO2”śNa2SiO3 ”” ””””C£®Na2O2”śNa2CO3”””””” ”” D£®SiO2”śH2SiO3
7. ĮŠĆčŹöÕżČ·µÄŹĒ”””””””””””””””””””” ””””””””””””””””””””””””””””””””””””(”””” )
”””” A£®2004ÄźĪŅ¹śŹ×““ÓĆCO2ŗĻ³ÉæɽµĖÜĮĻ¾Ū¶žŃõ»ÆĢ¼£¬Ź¹ÓĆøĆĖÜĮĻČŌČ»²śÉś°×É«ĪŪČ¾
”””” B£®³¬ĮŁ½ēĮ÷ĢåŹĒ½éÓŚĘųĢ¬ŗĶŅŗĢ¬Ö®¼äµÄŅ»ÖÖדĢ¬”£¹Ź³¬ĮŁ½ēĮ÷ĢåCO2ŹĒŗĻ³ÉµÄŠĀĪļÖŹ
 C£®°Ä“óĄūŃĒæŖ·¢³ö±»³ĘĪŖµŚĪåŠĪĢ¬µÄ¹ĢĢåĢ¼--”°ÄÉĆ×ÅŻÄ”±£¬ĘäŠĪĖĘŗ£Ćą£¬ĆÜ¶Č¼«Š”²¢ÓŠ“ÅŠŌ”£æÉŅŌŌ¤¼ū£¬ÕāÖÖŠĀ²ÄĮĻµÄ»ÆѧŠŌÖŹÓė½šøÖŹÆĶźČ«²»Ķ¬
C£®°Ä“óĄūŃĒæŖ·¢³ö±»³ĘĪŖµŚĪåŠĪĢ¬µÄ¹ĢĢåĢ¼--”°ÄÉĆ×ÅŻÄ”±£¬ĘäŠĪĖĘŗ£Ćą£¬ĆÜ¶Č¼«Š”²¢ÓŠ“ÅŠŌ”£æÉŅŌŌ¤¼ū£¬ÕāÖÖŠĀ²ÄĮĻµÄ»ÆѧŠŌÖŹÓė½šøÖŹÆĶźČ«²»Ķ¬
D£®ÓÉÓŚĒā¼üµÄÓ°Ļģ£¬¼×ĖįÕōĘųµÄĆܶČŌŚ373KŹ±ĪŖ1.335g”¤L-1,ŌŚ293KŹ±ĪŖ2.5 g”¤L-1
“š°ø D
6. ¹ŲÓŚ¹č¼°Ęä»ÆŗĻĪļµÄŠšŹöÖŠ£¬“ķĪóµÄŹĒ”””””””””” (”””” )
 ”””” A£®¹čŹĒĮ¼ŗƵİėµ¼Ģå²ÄĮĻ
”””” A£®¹čŹĒĮ¼ŗƵİėµ¼Ģå²ÄĮĻ
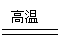 ”””” B£®¶žŃõ»Æ¹čÄÜÓėŹÆ»ŅŹÆ·“Ó¦£ŗSiO2+CaCO3””””””””
CaSiO3+CO2ӟ
”””” B£®¶žŃõ»Æ¹čÄÜÓėŹÆ»ŅŹÆ·“Ó¦£ŗSiO2+CaCO3””””””””
CaSiO3+CO2ӟ
”””” C£®æÉŅŌÓĆ½¹Ģ滹Ō¶žŃõ»Æ¹čÉś²ś¹č£ŗSiO2+2C”””””””””””” Si + 2CO”ü
”””” D£®Ė®ÄąµÄÖ÷ŅŖ³É·ÖŹĒNa2SiO3”¢CaSiO3ŗĶSiO2
“š°ø D
5. ½öŗ¬Ģ¼”¢ŃõĮ½ÖÖŌŖĖŲµÄĘųĢåÖŠ£¬Ģ¼ŗĶŃõµÄÖŹĮæÖ®±ČĪŖ3£ŗ5£¬ŌņøĆĘųĢåæÉÄÜŹĒ”””” (”” ””)””””””””””””””””””””””””””””””””””””””””””””””””””””””””
”””” ¢ŁÓÉCO»ņCO2µ„¶Ą×é³ÉµÄ“æ¾»Īļ”””” ¢ŚÓÉCOŗĶCO2¹²Ķ¬×é³ÉµÄ»ģŗĻĪļ
”””” ¢ŪÓÉCOŗĶO2¹²Ķ¬×é³ÉµÄ»ģŗĻĪļ”””””” ¢ÜÓÉO2ŗĶCO2¹²Ķ¬×é³ÉµÄ»ģŗĻĪļ
”””” A£®¢Ł¢Ś”””””””””””””””””””””” B£®¢Ś¢Ū”””””””””””””””””””””” C£®¢Ū¢Ü”””””””””””””””””””””” D£®¢Ś¢Ü
“š°ø B
4. Ģ¼ÓėÅØĮņĖį¹²ČČ²śÉśµÄĘųĢåXŗĶĶÓėÅØĻõĖį·“Ó¦²śÉśĘųĢåYĶ¬Ź±ĶØČėŹ¢ÓŠ×ćĮæĀČ»Æ±µČÜŅŗµÄĻ“ĘųĘæÖŠ(ČēÓŅĶ¼×°ÖĆ)£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ”” ””””””””””””””””””””””””””””(”” )
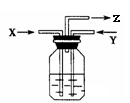 ”””” A£®Ļ“ĘųĘæÖŠ»į²śÉśĢ¼Ėį±µ³Įµķ
”””” A£®Ļ“ĘųĘæÖŠ»į²śÉśĢ¼Ėį±µ³Įµķ
”””” B£®ŌŚZµ¼¹Ü³öĄ“µÄĘųĢåÖŠĪŽ¶žŃõ»ÆĢ¼
”””” C£®ŌŚZµ¼¹ÜæŚÓŠŗģ×ŲÉ«ĘųĢå³öĻÖ
”””” D£®Ļ“ĘųĘæÖŠ»į²śÉśŃĒĮņĖį±µ³Įµķ
“š°ø C
3£®¹čĖįŃĪÓė¶žŃõ»Æ¹čŅ»Ńł,¶¼ŹĒŅŌ¹čŃõĖÄĆęĢå×÷ĪŖ»ł±¾½į¹¹µ„ŌŖ”£¹čŃõĖÄĆęĢåæÉŅŌÓĆĶ¶Ó°Ķ¼±ķŹ¾³É£ŗ
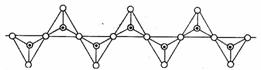
ĘäÖŠ”š±ķŹ¾ŃõŌ×Ó£¬ÖŠŠÄŗŚµć±ķŹ¾¹čŌ×Ó”£¹čŃõĖÄĆęĢåĶعż²»Ķ¬·½Ź½µÄĮ¬½ÓæÉŅŌ×é³Éø÷ÖÖ²»Ķ¬µÄ¹čĖįøłĄė×Ó”£ŹŌČ·¶ØŌŚĪŽĻŽ³¤µÄµ„Į“ŅõĄė×ÓÖŠ(¼ūĶ¼)£¬¹čŌ×ÓÓėŃõŌ×ÓµÄøöŹżÖ®±ČĪŖ
”””” A£®1:2”””””””””” B£®1:3”””””””””” C£®2:5”””””””” D£®2:7
“š°ø£ŗB
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com