
22.(12分)化合物A只含有碳、氢、氧三种元素,相对分子质量为114,氧的质量分数为28%。A的相关反应如下图所示:
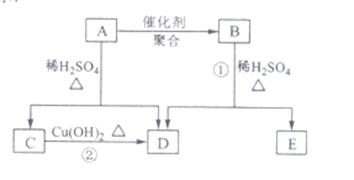
已知R-CH=CHOH(烯醇)不稳定,很快转化为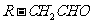 。根据以上信息回答下列问题:
。根据以上信息回答下列问题:
(1)A的分子式为 ;
(2)A的结构简式是 ;
(3)反应②的化学方程式是 ;
(4)反应①的化学方程式是 ;
(5)A的某种同分异构体,同时满足下列两个条件:
(i)具有酸性; (ii)分子所有碳原子均在同一平面。
请写出该同分异构体的结构简式: ;
21.(10分)A B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型。A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子。
(1)C的元素符号是 ;元素F在周期表中的位置 。
(2)B与D一般情况下可形成两种常见气态化合物,假若现在科学家制出另一种直线型气态化合物B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为 ,其固体时的晶体类型是 。
 (3)最近意大利罗马大学的FuNvio Cacace等人获得了极
(3)最近意大利罗马大学的FuNvio Cacace等人获得了极 具理论研究意
具理论研究意 义的C4气态分子。C4分子结构如图所示,已知断裂1molC-C吸收167kJ的热量,生
义的C4气态分子。C4分子结构如图所示,已知断裂1molC-C吸收167kJ的热量,生 成1mol C≡C放出942kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:
。
成1mol C≡C放出942kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:
。
20. (8分)某反应中反应物
(8分)某反应中反应物 与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
 (1)已知KBrO3在反应中得到电子,则该反应的还原剂是
。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
。
 (2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
。
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
。
 (3)根据上述反应可推知
。
(3)根据上述反应可推知
。
 a.氧化性:KBrO3>H3AsO4 b.氧化性:KBrO3<H3AsO4
a.氧化性:KBrO3>H3AsO4 b.氧化性:KBrO3<H3AsO4
 c.还原性:AsH3>X
d.还原性:X>AsH3
c.还原性:AsH3>X
d.还原性:X>AsH3
 (4)将该化学反应方程式配平,并用双线桥标出电子转移的方
(4)将该化学反应方程式配平,并用双线桥标出电子转移的方 向和数目:
向和数目:
 ;
;
19.(10分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(每种电解质电离时只产生一种阳离子与阴离子,而且不重复)。
|
阳离子 |
H+ 、Na+ 、Al3+ 、Mg2+ 、Ba2+ |
|
阴离子 |
OH- 、Cl- 、CO3- 、NO3- 、SO42- |
已知:①A、B两种溶液呈碱性;C、D、E溶液呈酸性。②A溶液与E溶液反应既有气体又有沉淀产生; A溶液与C溶液反应只有气体产生。③B溶液与D溶液反应时会生成两种沉淀。
A溶液与C溶液反应只有气体产生。③B溶液与D溶液反应时会生成两种沉淀。
回答问题:
(1)你能确定的物质的代号及化学式有: ;
请你说明不能具体确定的物质的理由 ;
(2)用离子方程式解释E溶液呈现一定酸碱性的原因 ;
18.两个化学兴趣小组用石墨电极分别电解两份质量均为ω1 g的KNO3溶液,第一组共收集到V1L气体,析出晶体m1g,第二组共收集到V2L气体,析出晶体m2g,则下列有关结论正确的是(气体体积均在标况下测定,晶体不含结晶水)
A.第一组实验过程中转移电子的物质的量为 mol
mol
B.实验所得阴、阳两极气体物质的量之比为1∶2
C.利用上述实验数据不能求出该KNO3溶液得质量分数
D.该实验温度下KNO3的溶解度为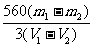 g
g
第Ⅱ卷(共计54分)
17.某溶液中只可能含有下列离子中的几种:K+、NH4+、NO3-、SO42-、SO32-、CO32-,取200mL该溶液分成两等份,进行以下实验:(1)第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;(2)第二份先加足量的盐酸无现象,再加足量的BaCl2,得到2.33g固体;则该溶液中
A.可能含有K+、CO32- B.一定含有K+且c(K+)≥0.1mol/L
C.一定不含有NO3- D.肯定含有NO3-、SO42-、NH4+
16. 已知:2CO(g)+O2(g)=2CO2(g);ΔH=-566 kJ/mol
已知:2CO(g)+O2(g)=2CO2(g);ΔH=-566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g);ΔH=-226 kJ/mol
O2(g);ΔH=-226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为566 kJ/mol
B.右图可表示为CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g);ΔH>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
15. “对氨基苯甲酸丁酯”是防晒霜的主要成分。下列关于“对氨基苯甲酸丁酯”说法正确的是
A.从有机物分类看,它可属于“氨基酸类” B.它的分子式为C11H15NO2
C.它能与盐酸反应,但不能和苛性钠溶液反应 D.丁基(-C4H9)有三种不同结构
14.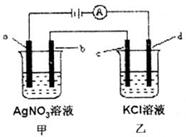 如图所示,a、b、c均为石墨电极,d为碳钢电极,通电
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电
进行电解。假设在电解过程中产生的气体全部逸出,下列说法
不正确的是
A.甲烧杯中溶液pH降低、乙两烧杯中溶液pH均升高
B.当b极增重10.8g时,乙池共产生气体约2.24L(标况)
C.当电解一段时间后,将甲、乙两溶液混合,一定会生成沉淀
D.持续电解,b、c两极的电极反应会发生改变
12.X、Y、Z、W是元素周期表中的短周期主族元素,它们在周期表中的相对位置如下表,则关于它们的说法不正确的是
|
|
X |
|
Y |
|
Z |
|
W |
|
A.它们的原子序数关系是:X+W=Z+Y
B.若X、Y为非金属元素,则它们的氢化物可能都含极性键与非极性键
C.若Z、Y均有稳定的简单离子存在,则离子半径关系是:Z>Y
D.若Y、W均为非金属元素,则Y的氢化物沸点一定高于W的气态氢化物
13下列实验中操作、现象、结论对应关系均正确的一 组是
组是
|
选项 |
操作 |
现象 |
结论 |
|
A |
淀粉和稀硫酸混合共热后,再加入少量新制的氢氧化铜悬浊液,加热到沸腾。 |
产生红色沉淀 |
淀粉水解可以生成葡萄糖 |
|
B |
植物油中加入溴水 |
有白色固体生成 |
植物油分子中含有不饱和烃基 |
|
C |
溴乙烷和氢氧化钠溶液充分反应后,用足量稀硝酸化,再加入硝酸银溶液 |
生成淡黄色沉淀 |
溴乙烷中含有溴离子 |
|
D |
将溴水加入苯中并充分振荡 |
溴水层褪色 |
苯与溴发生了取代反应 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com