
6.常温下,下列各组离子在给定条件下一定能大量共存的是 ( )
A.在pH=0的溶液中:I-、Ca2+、NO3-、NH4+
B.存在大量Fe3+的溶液中:SCN-、Na+、SO42-、Cl-
C.存在大量Al3+的溶液中:AlO2-、Na+、SO42-、Cl-
D.在c(OH-)=1.0ⅹ10-3 mol·L-1的溶液中:Na+、S2-、AlO2-、SO32-
5.用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.常温常压下,22.4LCO2中含有NA个CO2分子
B.标准状况下,1molZn与含2molH2SO4的浓硫酸充分反应,生成气体分子数为NA
C.0.1mol/L的氯化铝溶液中含有的氯离子数为0.3NA
D.标准状况下,2.24L四氯化碳中含有C-Cl键数为0.4NA
4.化学在生产和日常生活中有着重要的应用。下列说法不正确的是 ( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.工业上可用铝热反应大规模炼铁
C.刚玉的主要成分是Al2O3,硬度大
D.电解熔融MgCl2,可制得金属镁
3.下列实验设计及其对应的离子方程式均正确的是 ( )
A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ = Cu2+ + 2Fe2+
B.F2与H2O反应制备O2 :F2 + 2H2O = 2H+ +2 F-+ O2↑
C.将氯气溶于水配置氯水:Cl2 + H2O = 2H+ + Cl- + ClO-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO +
6H+ + 5H2O2 = 2Mn2+
+ 5O2↑ + 8H2O
+
6H+ + 5H2O2 = 2Mn2+
+ 5O2↑ + 8H2O
2.下列叙述中正确的是 ( )
A.稀有气体的晶体中不存在分子间作用力
B.次氯酸分子的结构式为H-O-Cl
C.Na2O和Na2O2所含化学键类型完全相同
D.Br2蒸气被木炭吸附时共价键被破坏
1.化学与生活、社会密切相关。下列说法不正确的是 ( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.垃圾是放错地方的资源,应分类回收利用
12.(2009年灌云质检)有A、B两种常见化合物组成混合物,其焰色反应均为黄色,其相互转化关系如图(其他物质均略去)。
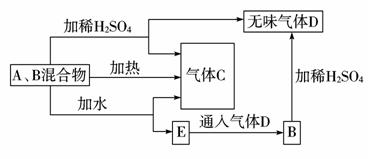
根据以上关系,回答下列问题:
(1)写出A、B、C、D的化学式:A____________,B____________,
C____________,D____________。
(2)写出混合物中加水反应的化学方程式:____________
____________ 。
(3)加热后,若只得到一种固体化合物,则A与B的物质的量之比的最大值为____________。(填数字)
11.(2009年广东质检)实验室可观察到如下实验事实:
向滴有酚酞的水中投入一定量的Na2O2,观察到先有大量气泡产生,溶液变红,过一会儿溶液又变为无色。对上述实验中溶液变红,过一会儿又褪色的原因,甲乙两同学提出了不同的解释:甲同学认为是Na2O2与水反应放出氧气,氧气有氧化性,将酚酞氧化而使溶液褪色;
乙同学则认为是Na2O2与水反应时产生了H2O2,H2O2的强氧化性使酚酞褪色。
(1)乙同学设计了如下实验来证明自己的猜想是正确的:在滴有酚酞的氢氧化钠溶液中滴加3%的H2O2溶液并振荡。
①若乙同学的猜想正确,可观察到的现象是____________。
②甲同学针对乙同学的上述验证实验提出还应增做实验才能更直接证明Na2O2与水反应生成了H2O2,甲同学提出要增加的实验是什么?
(2)试设计简单实验证明甲同学的解释是否正确(画出简易装置图,说明简要步骤).
10.钠在空气中燃烧(如图甲)生成产物的固体物质中除有黄色粉末外,还有黑色固体物质--炭。

(1)请假设黑色固体物质可能产生的原因是:
假设①____________ ;
假设②____________ ;
假设③____________ 。
(2)为确认以上其中一种假设的正误,某同学进行如下推断:由于金属钠与氧的结合能力比碳强,因此黑色炭可能是二氧化碳与金属钠发生置换反应而生成。该同学设计实验如下:
用打孔器钻取一段金属钠,取中间一小块钠放在充满二氧化碳气体的试管(如图乙)中加热,观察到钠燃烧发出黄色火焰,并有黄色固体和黑色固体生成,生成的黄色固体立即变成白色。请回答下列问题:
①用打孔器取用金属钠的原因是____________ ;
②产生以上现象的化学反应为____________ 。
9.(2010年枣庄质量检测)Na2O2几乎能与所有常见的气态非金属氧化物在一定条件下反应,如:
2Na2O2+2CO2=2Na2CO3+O2
Na2O2+CO=Na2CO3
(1)试分别写出Na2O2与SO2、SO23反应的化学方程式:
____________ 。
(2)通过比较知,当非金属处于____________价态时,与氧化物Na2O2反应有O2生成。
(3)等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9[SX)](同温同压下),这时混合气体中N2、O2、CO2物质的量之比为____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com