
24.将100mL 0.2mol/L 的盐酸与100mL 0.3 mol/L 的盐酸混合(假设混合时体积变化忽略不计),求
(1)混合后盐酸溶液的物质的量浓度
(2)若欲将该200mL盐酸溶液浓度重新恢复为0.3mol/L,则需要向其中通入标况下的HCl气体多少升?(体积变化忽略不计)
23.(12分)现从固体KOH出发配制0.1mol/L 的KOH溶液 500mL,回答下列问题:
(1)配制过程中需要用到的玻璃仪器有烧杯.玻璃棒.量筒.胶头滴管.
(2)如果在定容时仰视操作,则所配得溶液的浓度 0.1mol/L(填> , = , <)
(3)若所用的固体KOH中混有NaOH,则所配得溶液的OH-浓度 0.1mol/L
(填> , = , <)
(4)若用250mL的H2SO4溶液恰好能将此500mL 0.1mol/L 的KOH溶液中和,则该硫酸的物质的量浓度为 mol/L
22.(6分)在120℃.1个大气压下,将150mL CH4和He的混合气体中与350mL O2混合,
点燃并充分反应。
(1)若恢复到原条件,则混合气体的总体积为 mL
(2)若再将以上混合气体干燥,得混合气体450mL。则原混合气体中CH4和He的体积
比为
21.(12分)(1)写出以下两种仪器的名称:
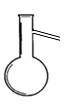 A:
A:  B:
B:
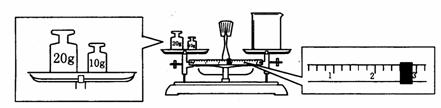
(2)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,烧
杯的实际质量为_________g.
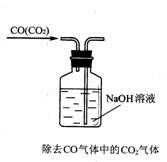
(3)指出下面实验中存在的错误:
20.某氯化镁溶液的密度为1.18g•cm-3,其中镁离子的质量分数为5.11%。300mL该溶液中Cl-离子的物质的量约等于: ( )
A.0.37mol B.0.63mol C.0.74mol D.1.5mol
Ⅱ卷(非选择题 共40分)
19.标况下,两个容积相同的容器中,一个盛有NH3气体,另一个盛有N2和H2的混合气体。若两容器内的气体具有相等的电子数,则混合气体中N2和H2的物质的量之比为( )
A.4:1 B. 1:2 C. 2:1 D.1:4
18.在标准状况下,18gCO和CO2的混合气体的体积为11.2L。则此混合气体中CO和CO2的质量之比是 ( )
A.1:1 B.1:7 C.1:11 D.7:11
17.t℃时,相对分子质量为A的某物质的饱和溶液,其物质的量浓度为Bmol·L-1,密度为ρg·cm-3,则该物质在t℃时溶解度为 ( )
A. g B.
g B.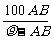 g
g
C.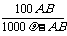 g D.
g D.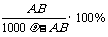 g
g
16.相同条件下,气体A与氧气的质量比为2∶1,体积比为4∶1,气体A的相对分子质量是 ( )
A.16 B.17 C.44 D.64
15.某非金属单质A和氧气发生化合反应生成B。B为气体,其体积是反应掉氧气体积的两倍(同温同压)。以下对B分子组成的推测一定正确的是 ( )
A.有1个氧原子 B.有2个氧原子
C.有1个A原子 D.有2个A原子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com