
3.同系物:⑵⑸或⑵⑻或⑺⑿
同分异构体:⑸⑻或⑻⑿ 同素异形体:⑶⑽
同位素:⑼⑾同一种物质:⑴和⑷,⑵和⑺,⑸和⑿
讲析:根据题目中所涉及的各个概念的含义进行判断可知答案。
新活题网站
1.D 2.C
讲析:1.选项A中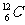 和
和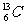 这两种原子,质子数均为6,但质量数不同,故它们为同位素。选项B中O2和O3
这两种原子,质子数均为6,但质量数不同,故它们为同位素。选项B中O2和O3 是氧元素的两种单质,是同素异形体。选项C给出两个有机分子的结构简式,表面上看不同,实际表示的是同一种物质--丙烷。选项D中两个结构简式都表示5个碳原子的烷烃,分子式都为C5H12,故它们互为同分异构体。2.根据生成的四种卤代烃物质的量相等和化学反应中质量守恒定律判断,CH4与Cl2反应的化学方程式为:
是氧元素的两种单质,是同素异形体。选项C给出两个有机分子的结构简式,表面上看不同,实际表示的是同一种物质--丙烷。选项D中两个结构简式都表示5个碳原子的烷烃,分子式都为C5H12,故它们互为同分异构体。2.根据生成的四种卤代烃物质的量相等和化学反应中质量守恒定律判断,CH4与Cl2反应的化学方程式为:
4CH4+10Cl2 CH3Cl+CH2Cl2+CHCl3+CCl4+10HCl
CH3Cl+CH2Cl2+CHCl3+CCl4+10HCl
14. 写名称或结构简式:
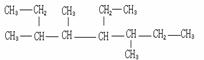 (1)按系统命名法命名下列物质
(1)按系统命名法命名下列物质
①
;
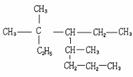
②
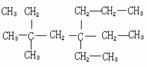 ③
③
15(2003年上海高考试题).合成氨原料可以由天然气制取。其主要反应为CH4(g)+H2O(g) CO(g)+3H2(g)。
CO(g)+3H2(g)。
(1)1m3(标准状况)CH4按上式反应产生H2 mol。
(2)CH4和O2的反应为2CH4(g)+O2(g) 2CO(g)+4H2(g),设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为
。
2CO(g)+4H2(g),设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为
。
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
|
气体 |
CO |
H2 |
N2 |
O2 |
|
体积(L) |
25 |
60 |
15 |
2.5 |
计算该富氧空气中O2和N2的体积比(VO2/VN2)。
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,VH2/VN2=3∶1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为何值?
13. 一氯取代物的同分异构体有2种,二氯取代物的同分异构体有4种的烷烃分子共有的种数是( )
A、乙烷 B、丙烷 C、正丁烷 D、环丁烷
12. 在标准状况下,将0.008mol甲烷和氧气的混合气体点燃,完全燃烧后,将生成的气体通入100mL0.02mol/L的石灰水中,得到0.1g纯净的沉淀。则原混合气体中甲烷和氧气的体积比可能是( )
A、1:7 B、3:5 C、1:2 D、1:3
11. 燃烧等物质的量的下列各组烃,产生相同质量水的一组是( )
A.
丙烷和环丙烷(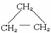 )
)
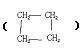
B. 丙烷和环丁烷
C.乙烷和异丁烷 D.2-甲基丁烷和戊烷
10. 关于 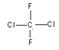 (商品名称为氟里昂-12)的叙述正确的是( )
(商品名称为氟里昂-12)的叙述正确的是( )
A.有两种同分异构体 B.是平面型分子
C.只有一种结构 D.有四种同分异构体
9. 以M原子为中心形成的MX2Y2分子中,X、Y分别只以单键与M结合,下列说法正确的是( ) ( )
A.若MX2Y2分子为平面四边形就有2种同分异构体
B.若MX2Y2分子为平面四边形则无同分异构体
C.若MX2Y2分子为四面体形就有2种同分异构体
D.若MX2Y2分子为四面体形则无同分异构体
8.引燃密闭容器中的己烷和氧气的混合气体,使其进行不完全燃烧,在120℃时测得反应前后气体的压强分别为0.36×105Pa和0.52×105Pa。这一燃烧反应中主要发生的化学反应的化学方程式是( )
A.
C6H14+9O2 CO+5CO2+7H2O
CO+5CO2+7H2O
B.
C6H14+7O2 5CO+CO2+7H2O
5CO+CO2+7H2O
C.
C6H14+8O2 3CO+3CO2+7H2O
3CO+3CO2+7H2O
D.
2C6H14+15O2 8CO+4CO2+14H2O
8CO+4CO2+14H2O
7.如果空气中混入甲烷的体积达到总体积的5%-10%这个范围,点火时就会爆炸。当甲烷与氧气恰好完全反应时,产生最强的爆炸,此时甲烷所占的体积分数是( )
A.2.5% B.7.5% C.9.5% D.10%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com