
7、常用化肥的简单区别方法:“看、溶、烧、嗅”。看外观:氮肥、钾肥大都是白色晶体,磷肥是灰白色粉末。加水:氮肥、钾肥大都溶于水。灼烧:钾肥不能燃烧,在燃烧时可跳动或有爆裂声。加熟石灰搅拌:铵盐加熟石灰能放出具有刺激性的氨气。
6、部分碱和盐在水中的溶解性,见右表。
5、复分解反应发生的条件:生成物中有水或气体或沉淀生成。
4、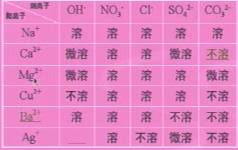 组成里含有碳酸根离子(CO32-)或碳酸氢根离子的盐,都能与盐酸反应生成二氧化碳(观察到有气泡产生,将气体通入澄清石灰水中石灰水变浑浊。)(碳酸盐遇酸沉不住气。)利用这一原理,可以检验物质组成中是否有碳酸根离子或碳酸氢根离子。实验室也是用此原理,选用易得、价廉的石灰石(或大理石)与稀盐酸反应制取二氧化碳。
组成里含有碳酸根离子(CO32-)或碳酸氢根离子的盐,都能与盐酸反应生成二氧化碳(观察到有气泡产生,将气体通入澄清石灰水中石灰水变浑浊。)(碳酸盐遇酸沉不住气。)利用这一原理,可以检验物质组成中是否有碳酸根离子或碳酸氢根离子。实验室也是用此原理,选用易得、价廉的石灰石(或大理石)与稀盐酸反应制取二氧化碳。
3、粗盐,是从海水、盐井水、盐湖水通过晾晒或煮,可蒸发水分而得到含杂质较多的氯化钠晶体。粗盐的提纯过程:粗盐→溶解→过滤→蒸发结晶→食盐。过滤是物质提纯的方法之一,它把不溶性的固体与液体分开。
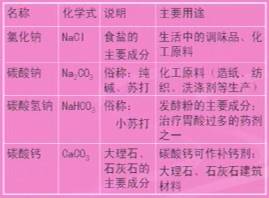
2、生活中几种常见盐的作用及主要用途。
1、有些盐的水溶液具有特殊颜色。①含有Cu2+的稀盐溶液呈现出蓝色,如蓝色的硫酸铜溶液;②含有Fe2+的稀盐溶液呈现出浅绿色,如浅绿色的硫酸亚铁溶液;③含有Fe3+的稀盐溶液呈现黄色,如黄色的氯化铁溶液等。
14、右图中M、N、A、B、C、D各表示一种反应物或一种生成物(水均已略去),已知M中含有Na+,D通常状况下是一种无色的气体。
(1)推断M、N的化学式分别是 Na2CO3、Ca(OH)2 。
(2)写出A→M的化学方程式 2NaOH+CO2=Na2CO3+H2O 。
(分析:关键找突破口,M能与CaCl2反应,则一定有溶液CaCO3生成,又已知M中含有Na+,推出M为Na2CO3。)
第十一讲 盐和化肥
13、右图是实验中各物质的变化关系,氧化铜加入过量的稀盐酸,得到溶液A;氧化铜和铁的混合物通入足量的氢气并加热,得到固体B;溶液A跟固体B反应,得到气体C、溶液D、固体纯净物E。
(1)写出氧化铜与稀盐酸反应的化学方程式。 CuO+2HCl=CuCl2+H2O
(2)气体C是 H2 ,固体E是 Cu 。
(3)溶液D中一定含有的溶质是 FeCl2 。
 (分析:加入过量的稀盐酸,说明溶液A中除有氯化铜外,还有HCl。)
(分析:加入过量的稀盐酸,说明溶液A中除有氯化铜外,还有HCl。)
12、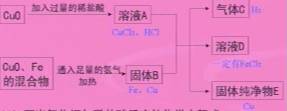 现有A、B、C、D、E五瓶无色溶液,它们分别是盐酸、氯化钠、氧化钙、氢氧化钙和碳酸钠,把它们进行一系列实验,观察到如下现象:①B跟C两溶液混合,产生白色沉淀;②B跟D两溶液混合,产生白色沉淀;③B跟E两溶液混合,产生气泡;④C溶液能使无色酚酞试液变红。分析上述实验现象,推出A、B、C、D、E的化学式分别是 NaCl、Na2CO3、CaOH、CaCl2、HCl 。(找准突破口,本题从第③④上突破,④说明C显碱性,③说明B或E是盐酸或碳酸钠,则C溶液为氢氧化钙。本题还可以把五种溶液两两混合列表举出反应现象,与已知现象比较后得出结论,如B跟C、D混合,都产生白色沉淀,说明B是碳酸钠。)
现有A、B、C、D、E五瓶无色溶液,它们分别是盐酸、氯化钠、氧化钙、氢氧化钙和碳酸钠,把它们进行一系列实验,观察到如下现象:①B跟C两溶液混合,产生白色沉淀;②B跟D两溶液混合,产生白色沉淀;③B跟E两溶液混合,产生气泡;④C溶液能使无色酚酞试液变红。分析上述实验现象,推出A、B、C、D、E的化学式分别是 NaCl、Na2CO3、CaOH、CaCl2、HCl 。(找准突破口,本题从第③④上突破,④说明C显碱性,③说明B或E是盐酸或碳酸钠,则C溶液为氢氧化钙。本题还可以把五种溶液两两混合列表举出反应现象,与已知现象比较后得出结论,如B跟C、D混合,都产生白色沉淀,说明B是碳酸钠。)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com