
10. (2008年秋季湖北省部分重点中学期中联考)
某化学实验小组的同学为了探究和比较SO2和Cl2水的漂白性,设计了如下的实验装置。
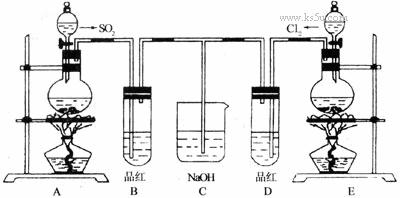
(1)实验室用装置A制备SO2气体,写出A中发生反应的化学方程式: 。某同学在实验时发现打开A中的分液漏斗活塞后,漏斗中液体没流下,你想原因可能是:
(2)实验室用装置E制备Cl2气体,写出E中发生反应的离子方程式: ,指出该反应中的液体反应物在反应中所表现出的性质: 。
 (3)①反应开始后一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
:(填写序号字母)
(3)①反应开始后一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
:(填写序号字母)
I.都褪色 II.都不褪色 Ⅲ.B褪色,D不褪色 Ⅳ.B不褪色,D褪色
②停止通气后,再给B、D两个试管加热,两个试管中的现象分别为B: ,D:

(4)第二个实验小组的同学认为SO2和Cl2水都有漂白性,二者混合后的漂白性会更强,他们将制得的SO2和Cl2同时通入到品红溶液中,结果褪色效果并不像想象的那样快。为了探讨SO2和Cl2按1:1通入的漂白效果,他们设计了如下实验装置:
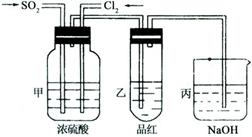
①实验开始后,乙装置中出现的现象:
②用离子方程式表示乙中产生该现象的原因:
|

 答案.(1)H
答案.(1)H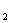 SO
SO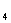 +Na
+Na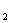 SO
SO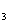 Na
Na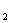 SO
SO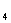 +SO
+SO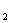 ↑+H
↑+H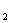 O
O
分液漏斗盖子未打开
|

 (2)MnO
(2)MnO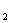 +4H
+4H +2Cl
+2Cl Mn
Mn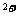 +Cl
+Cl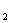 ↑+2H
↑+2H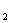 O
O
酸性,还原性
(3)①Ⅰ ②B:由无色变为红色( D:无明显现象
(4)①品红未褪色
②SO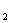 +Cl
+Cl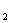 +2H
+2H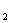 O=4H
O=4H +SO
+SO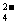 +2Cl
+2Cl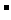

9.根据下图所示实验回答下列问题:

(1)试管C口部的棉团上发生反应的离子方程式是 。
(2)试管B中的实验现象是 ,若将该试管中反应后的溶液加热,可以观察到 。试管C中溶液变浑浊,则证明SO2具有 性。
(3)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的化学方程式是 。
答案(1)SO2 +2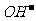 =
=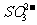 +H2O
+H2O
(2)红色褪去 溶液又恢复红色 氧化
(3)吸收有害气体,防止污染空气
NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O)
8. ( 河南省郸城一高09高三化学尖子生第二考试)把一定量的锌与100 mL 18.5 mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6L(S.T.P.)。将反应后的溶液稀释到1 L,测得溶液的pH=1,则下列叙述错误的是 ( )
 A.气体A是SO2和H2的混合物 B.气体A中SO2和H2的体积比为4:1
A.气体A是SO2和H2的混合物 B.气体A中SO2和H2的体积比为4:1
C.反应中共消耗锌87.5g D.反应中共转移电子3 mol
答案:BC
7.(杭州儒林﹒育英高复学校第三次 )将按等物质的量的SO2和Cl2混合后的气体溶解于适量的蒸馏水中,再滴入含有品红和Ba(NO3)2的混合溶液,则发生的实验现象是 ( ) ①红色溶液很快褪色 ②红色溶液不褪色 ③有白色沉淀生成 ④溶液仍然透明
A.仅①和④ B.仅①和③ C.仅②和③ D.仅②和④
答案:C
6.研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解 过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。下列所得结论正确的是
过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。下列所得结论正确的是
A.铜与浓硫酸反应所得白色固体是CuSO4
B.加BaCl2溶液后所得白色沉淀是BaSO3
C.白色固体中夹杂的少量黑色物质可能是CuO
D.白色固体中夹杂的少量黑色物质中含元素Cu、S
答案:AD
5. 接触法生产H2SO4的过程中,对废气、废液、废渣和“废热”的处理正确的是
①尾气用氨水处理 ②污水用石灰乳处理
③废渣用来造水泥、炼铁 ④设置“废热”锅炉产生蒸气,供热或发电。
A.只有①② B.只有①③④ C.只有①②③ D.全部
答案:D
4.下列实验能证明有SO2存在的是
(1)能使澄清石灰水变浑浊
 (2)能使湿润的蓝色石蕊试纸变红
(2)能使湿润的蓝色石蕊试纸变红
(3)能使品红溶液褪色
(4)通入足量的NaOH溶液中,再滴加BaCl2溶液有白色沉淀生成,该沉淀能溶于盐酸。
(5)通入Br2水中能使Br2水褪色,再加Ba(NO3)2溶液有白色沉淀。
A.都能证明 B.都不能证明
C.(3)(4)(5)能证明 D.只有(5)能证明
答案:D
3.(重庆市五区2009届高三联考)以下每个选项中的两组物质都能反应,且放出同一种气体产物的是
A.铜与稀硫酸,铜与浓硫酸 B.铁与稀硫酸,铁与浓硫酸
C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸 D.硫化钠与稀硫酸,硫化钠与稀盐酸
答案:D
2.用可溶性钡盐检验 离子的存在时,先在待测溶液中加入盐酸,其作用是
离子的存在时,先在待测溶液中加入盐酸,其作用是
A.形成较多的白色沉淀
B.形成的沉淀纯度更高
C.排除 -以外的其它阴离子及Ag+的干扰
-以外的其它阴离子及Ag+的干扰
D.排除Ba2+以外的其它阳离子的干扰
答案:C
1.[天津市汉沽一中2009第五次月考化学.6]常温下单质硫主要以S8形式存在。加热时,S8会转化为S6、S4、S2等。当温度达到750℃时,硫蒸气主要以S2形式存在(占92%)。下列说法中正确的是 ( )
A.S8转化为S6、S4、S2属于物理变化
B.不论哪种硫分子,完全燃烧时都生成SO2
C.常温条件下单质硫为原子晶体
D.把硫单质在空气中加热到750℃即得S2
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com