
21.若NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.0.1mol氯气与金属铁完全反应时,转移电子数为0.2NA
B.100mL 1mol/L NaHCO3溶液含有0.1NA个HCO3-
C.7.1g氯气与足量NaOH溶液反应电子转移数为0.2NA
D.0.1molNa2O2中含有的离子数为0.4NA
20.下列离子方程式书写正确的是 ( )
( )
A.硫化钠溶于水:S2-+ 2H2O 
 H2S
+ 2OH-
H2S
+ 2OH-
B.用铜电极电解NaCl溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
C.氯气通入澄清石灰水中:Cl2+2OH- ===H2O+Cl-+ClO-
D.向石灰水中加入过量NaHCO3溶液:Ca2++OH-+HCO3-==CaCO3↓+H2O
19.关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是 ( )
A.c(NH4+):③>①
B.水电离出的c(H+):②>①
C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)
D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
18.已知I2+SO32-+H2O==2I-+SO42-+2H+。某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液的判断正确的是 ( )
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I-
A.②③④ B.①②③ C.①③ D.①②
0.01mol•L-1NH4Cl溶液中的Ksp小
D.25°C时,在Mg(OH)2的悬浊液加入NaF溶液后,在Mg(OH)2不可能转化成为MgF2
17.已知:25°C时,Ksp[Mg(OH)2]=5.61×10-12,Ksp[MgF2]=7.42×10-11。下列说法正确的是 ( )
A.25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大
C.25°C时,Mg(OH)2固体在20ml0.01 mol•L-1氨水中的Ksp比在20mL
16.反应⑴、⑵分别是从海藻灰和智利硝石中提取碘的主要反应:
2 NaI + MnO2 + 3 H2SO4 = 2 NaHSO4 + MnSO4+2 H2O + I2 ………⑴
2 NaIO3 + 5 NaHSO3 = 2 Na2SO4 + 3 NaHSO4 + H2O + I2 ………⑵
下列说法正确的是 ( )
A.两个反应中NaHSO4均为氧化产物
B.I2在反应⑴中是还原产物,在反应⑵中是氧化产物
C.氧化性:MnO2>SO42->IO3->I2
D.反应(1)、(2)中生成等量的I2时转移电子数之比为1:5
15.可逆反应a A(s)+b B(g) c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是( )
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是( )

A.达平衡后,加入催化剂则C%增大
B.达平衡后,若升温,平衡左移
C.化学方程式中c +d > a + b
D.达平衡后,增加A的量有利于平衡向右移动
14.用酸性氢氧燃料电池为电源进行电解的实验装置示意图如右图所示。下列说法中,正确的是 ( )
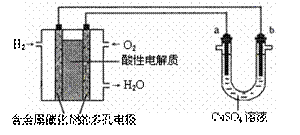
A.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-=4OH-
B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
13.Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl+S+SO2。SOCl2易挥发,在空气中遇水蒸气会产生大量白雾,下列说法不正确的是 ( )
A.电池的负极反应为:Li-e- ==Li+
B.碳电极上的反应:2SOCl2 +4e- ===4Cl- +S +SO2。
C.组装该电池必须在无水、无氧的条件下进行
D.电池工作时Li+向负极移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com