
8.下列叙述中不正确的是( )
A. 符合通式:CnH2n-2的有机物是炔烃
B. 乙炔分子中碳碳叁键的键能不是碳碳单键和碳碳双键的键能之和
C. 等质量的烃中含氢量越高,充分燃烧时,消耗氧气越多
D. 2-丁炔分子中的四个碳原子可能在同一条直线上
7.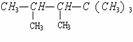 某烯烃与氢气加成后的产物是:
某烯烃与氢气加成后的产物是:
则该烯烃的结构式可能有几种( )
A.1 B.2 C.3 D.4
6.常温、常压下,50mL三种气态烃的混合物与足量的氧气混合后点燃爆炸,恢复到原来的状况时,体积共缩小100mL,则三种烃可能是( )
A.CH4、C2H2、C3H4 B.C2H6、C3H6、C4H6
C.CH4、C3H6、C4H8 D.C2H4、C2H6、C2H2
5.某烃室温时为气态,完全燃烧后,生成的H2O和CO2的物质的量之比为3∶4。该不饱和烃的链状同分异构体的数目是(不考虑-C=C=C-结构)( )
A.2 B.3 C.4 D.5
4.下列各种物质相互反应时,只产生一种气体的是( )
A.电石投入到食盐水中 B.Mg粉投入到溴水中
C.钠投入饱和NH4Cl溶液中 D.炭块投入热的HNO3中
3.用乙炔为原料制取CH2Br-CHBrCl,可行的反应途径是( )
A. 先加Cl2,再加Br2
B. 先加Cl2,再加HBr
C. 先加HCl ,再加HBr
D. 先加HCl ,再加Br2
2.(2001年江苏理科综合题)具有单双键交替长链(如-CH=CH-CH=CH-……)的高分子可能成为导电塑料。2000年诺贝尔化学奖即授予开辟此领域的3位科学家,下列高分子中可能成为导电塑料的是 ( )
A.聚乙烯 B.聚丁二烯
C.聚苯乙烯 D.聚乙炔
1.已知维生素A的结构简式如下图,关于它的叙述中正确的是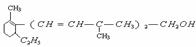 ( )
( )
A. 维生素A是一种烯烃
B. 维生素A的一个分子中有三个双键
C. 维生素A的一个分子中有30个氢原子
D. 维生素A能使溴水褪色,能被酸性KMnO4氧化
1.(1997年全国高考) 1,2-二溴乙烷可作汽油抗爆剂的添加剂。常温下,它是无色液体,密度为2.18g/cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验中可以用所示装置制备1,2-二溴乙烷。图中:分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液;试管d中装有液溴(表面覆盖少量水)
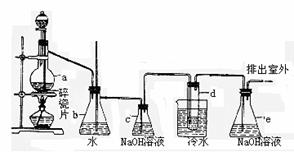 (1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式:
,
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式:
,
。
(2)安全瓶 b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象: 。
(3)容器c中NaOH溶液的作用是 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因。
2.(1997年全国高考) 1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家.C60分子是形如球状的多面体
(如图),
该结构的建立基于以下考虑:
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:
据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所含的双键数为30.
请回答下列问题:
(1)固体C60与金刚石相比较,熔点较高者应是____________,理由是: ______________________________________。
(2)试估计C60跟F2在一定条件下,能否发生反应生C60F60(填“可能”或“不可能”)___________________,并简述其理由:________________________________.
(3)通过计算,确定C60分子所含单键数.
C60分子所含单键数为_______________.
(4)C70分子也已制得,它的分子结构模型可以与C60同样考虑而推知.通过计算确定C70分子中五边形和六边形的数目.
C70分子中所含五边形数为_____ ,六边形数为_________.
测试提高
2.对加成反应和取代反应的正确理解并灵活运用,区分加成反应和加聚反应,并能快速找到高聚物的单体。
纠错训练
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com