
4.(浙江淳安县08届高三上学期三校联考)燃烧1g乙炔(C2H2)生成二氧化碳和液态水,放出热量50kJ, 则这一反应的热化学反应方程式为 ( D )
A.2C2H2(g)+ 5O2(g)=== 4CO2(g)+ 2H2O(l);△H= +50kJ/mol
B.C2H2(g)+ 5/2O2(g)===2CO2(g)+ H2O(l);△H= -1300kJ
C.2C2H2+ 5O2 ===4CO2 + 2H2O ;△H= -2600kJ
D.2C2H2(g)+ 5O2(g)===4CO2(g)+ 2H2O(l);△H = -2600kJ/mol
3.(2008年杭州学军中学高考模拟测试5月)下列说法或表示方法正确的是
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的能量多
B.由C(石墨)→C(金刚石);△H= +1.9 kJ •L-1可知,金刚石比石墨稳定
C.在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则H2燃烧热的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ·mol-1
D.在稀溶液中,H+(aq)+OH-(aq)==H2O(l);△H=-57.3 kJ·mol-1,若将含0.5mol H2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3KJ
2.(2008年杭州学军中学高考模拟测试5月)北京奥运火炬的外壳主要采用高品质的铝合金材料制造,燃烧系统内装环保型燃料--丙烷。下列有关说法中正确的是
A.丙烷是石油裂解气的主要成分
B.丙烷燃烧时的耗氧量比等体积的其他烷烃少
C.燃料燃烧时主要是将热能转化为光能
D.铝合金制作的火炬质量轻、不易腐蚀
1.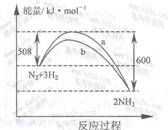 ((宁波市2008年高考模拟考试)右图是198K时N2与H2反应过群中能量变化的曲线图。下列叙述正确的是
((宁波市2008年高考模拟考试)右图是198K时N2与H2反应过群中能量变化的曲线图。下列叙述正确的是
A.该反应的热化学方程式为:
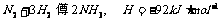
B.b曲线是加入正催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应历程改变,因此反应热也改变
D.在温度、体积均一定的条件下,通入1molN2和3molH2反应后放出的热量为Q1 kJ,
若通入2molN2和6molH2反应后放出的热量为Q2kJ,则184>2Ql>Q2>92
19、 以下现象与电化腐蚀无关的是
以下现象与电化腐蚀无关的是
A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 B、生铁比软铁芯(几乎是纯铁)容易生锈
C、铁质器件附有铜质配件,在接触处易生铁锈 D、银质奖牌久置后表面变暗
18、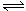 对于平衡体系mA(g) + nB(g) pC(g)
+ qD(g) ;⊿H<0。 有下列判断,其中正确的是
对于平衡体系mA(g) + nB(g) pC(g)
+ qD(g) ;⊿H<0。 有下列判断,其中正确的是
A、若温度不变,将容器的体积增大为原来的两倍,此时A物质的浓度
变为原来的0.48倍,则m + n <p + q
B、若平衡时A、B的转化率相等,说明反应开始时A、B的物的量之比为n: m ;
C、若温度不变而压强增大为原来的两倍,则达到新的平衡时平衡混合物的体积小于原体积的1/2
D、若平衡体系共有a mol气体,再向其中加入b molB,当达到
新平衡时共有(a + b)mol气体,则m + n = p + q
17、第二主族元素R的单质及其相应氧化物的混合物12g,加足量水经完全反应后蒸干,得固体16g,试推测该元素可能为
A、Mg B、Ca C、Sr D、Ba
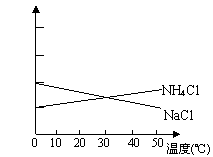
16、联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl.NaCl和NH4Cl共同存在时的溶解度曲线如图所示,以下操作正确的是
|
|
通入气体 |
温度控制 |
|
(A) (B) (C) (D) |
CO2 CO2 NH3 NH3 |
30~40℃ 0~10 ℃ 30~40 ℃ 0~10℃ |
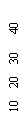
15、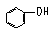 已知酸性强弱顺序为H2CO3> >HCO
已知酸性强弱顺序为H2CO3> >HCO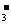 ,下列化学方程式正确的是BC
,下列化学方程式正确的是BC
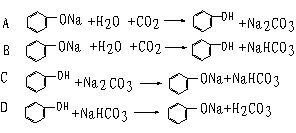
14、下列离子方程式书写正确的是
A、过量氯气通入溴化亚铁溶液中 3Cl2 + 2Fe2 + + 4Br- = 6Cl-+2Fe3++2Br2
B、过量二氧化碳通入偏铝酸钠溶液中 CO2+2H2O+AlO2- = Al(OH)3↓+HCO3-
C、亚硫酸氢铵溶液与等物质的量氢氧化钠混合 NH4+ +HSO3- +2OH- = SO32-+NH3↑+2H2O
D、碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO3-+Ca2++2OH-→CaCO3↓+2H2O+MgCO3↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com