
14.(2008浙大附中理综模拟考试)胡锦涛同志在十七大报告中指出,应加强能源资源节约和生态环境保护,增强可持续发展能力。下列行为与之不相符的是( A )
A.大量使用化学肥料,提高农作物的产量和质量
B.将作物秸秆通过化学反应转化为乙醇用作汽车燃料
C.使用资源节约型、环境友好型的生物降解塑料包装
D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生
13.(舟山中学2008学年第二次月考)已知298K时,2SO2 (g)+ O2(g)
 2 SO3(g)
; △H= - 197kJ/mol,
在相同温度和压强下,向某密闭容器中通人2mol SO2和1mol O2, 达到平衡时热效应量Q1 ,
向另一容积相同的密闭容器中通人1mol SO2和0.5mol O2,达到平衡时放出热量Q2,下列关系式正确的是
2 SO3(g)
; △H= - 197kJ/mol,
在相同温度和压强下,向某密闭容器中通人2mol SO2和1mol O2, 达到平衡时热效应量Q1 ,
向另一容积相同的密闭容器中通人1mol SO2和0.5mol O2,达到平衡时放出热量Q2,下列关系式正确的是
A.Q2 = Q1/2 B.Q2 > Q1/2
C.Q1 = Q2=197 kJ D.Q2 < Q1/2<197/2 kJ
12.(08学年度杭州学军中学高三年级第二次月考)甲醇属于再生能源,可代替汽油作为汽车燃料。下列能正确表示甲醇燃烧热的热化学方程式为(B)
A.CH3OH(l)+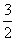 O2(g)=CO2(g)+2H2O(l);△H=+763.3kJ·mol-1
O2(g)=CO2(g)+2H2O(l);△H=+763.3kJ·mol-1
B.CH3OH(l)+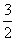 O2(g)=CO2(g)+2H2O(l);△H=-763.3kJ·mol-1
O2(g)=CO2(g)+2H2O(l);△H=-763.3kJ·mol-1
C.CH3OH(l)+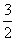 O2(g)=CO2(g)+2H2O(g);△H=-675.3kJ·mol-1
O2(g)=CO2(g)+2H2O(g);△H=-675.3kJ·mol-1
D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);△H=-1526.6kJ·mol-1
11.(08学年度杭州学军中学高三年级第二次月考)已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol。
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol
下列说法正确的是 ( A )
A.碳的燃烧热大于110.5 kJ/mol
B.①的反应热为221 kJ/mol
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
10.(08学年度杭州学军中学高三年级第二次月考)(6 分)某化学兴趣小组,专门研究了氧族元素及其某些化合物的部分性质。查得资料如下:①常温下,硒(Se)和碲(Te)为固体,H2Se和H2Te为气体;
②Te和H2不能直接化合生成H2Te
③氧气、硫、硒、碲与1mol H2反应热如下表所示。
|
物质 |
O2 |
S |
Se |
Te |
|
△H(kJ·mol-1) |
-242 |
-20 |
81 |
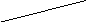 |
请回答下列问题:
(1)写出氧族元素中含有的18个电子的两种氢化物的化学式 、 。
(2)写出硒化氢发生反应的热化学方程式: 。
(3)一定温度下,在容积均为1L(容器容积不可变)的甲、乙两个容器中,分别充入2molSO2、 1molO2和4molSO2、2mol O2,在相同条件下使其反应。最终达到平衡后,甲、乙两容器中SO2转化率分别为50%和a(乙),则此时a(乙)________50%(填“大于”“小于”或“等于”)。
答案(1)H2O2;H2S(各1分)
(2)H2Se(g)= H2(g)+Se(s)△H= -8 kJ·mol-1(2分) (3)大于(2分)
9.(浙江九所重点中学高三年级调研考试)下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
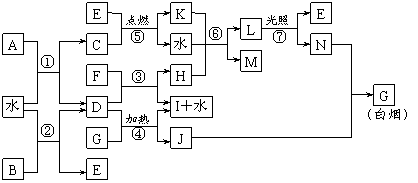
请按要求填空:
⑴G的电子式是_______________;
⑵反应⑥的化学方程式是__________________________________,反应⑤在空气中发生时的现象是________________________________,已知C的燃烧热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是________________________________________。
⑶根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是_________。
答案.⑴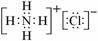 ⑵Ca(ClO)2+CO2+H2O=CaCO3+2HClO 火焰明亮并伴有浓烈黑烟 CH≡CH(g)+
⑵Ca(ClO)2+CO2+H2O=CaCO3+2HClO 火焰明亮并伴有浓烈黑烟 CH≡CH(g)+ O2(g)→2CO2(g)+H2O(l);ΔH=-1300 kJ·mol-1(热化学方程式中数据与本答案不同不给分) ⑶CaO2 (每空2分,共10分。)
O2(g)→2CO2(g)+H2O(l);ΔH=-1300 kJ·mol-1(热化学方程式中数据与本答案不同不给分) ⑶CaO2 (每空2分,共10分。)
8.(杭州市2008年高三第一次高考科目教学质量检测化学) 已知在25℃,101kPa下,l g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ
热量。表示上述反应的热化学方程式正确的是
A .C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(g); △H=-48.40kJ·mol-1
B.C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1); △H=-5518kJ·mol-1
C.C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1) ;△H=+5518kJ·mol-1
D.C8H18(1)+12.5O2(g)=8CO2(g)+9H2O(1); △H=-48.40kJ·mol-1
6.(杭州五校08高三第一次月考)下列说法正确的是
A.C(石墨,s)=C(金刚石,s) ΔH>0,所以石墨比金刚石稳定
B.1 mol H2SO4和 1 mol Ba(OH)2完全反应所放出的热量称为中和热
C.在101kPa 时,1 mol 碳燃烧放出的热量就是碳的燃烧热
D.在化学反应中需要加热的反应就是吸热反应
6.(金丽衢十二校高三第一次联考化学模拟) N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是( D )
A.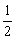 N2H4(g)+
N2H4(g)+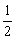 O2(g)====
O2(g)====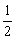 N2(g)+H2O(g);ΔH=+267 kJ·mol-1
N2(g)+H2O(g);ΔH=+267 kJ·mol-1
B.N2H4(g)+O2(g)====N2(g)+2H2O(l);ΔH=-133.5 kJ·mol-1
C.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH=+534 kJ·mol-1
D.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH=-534 kJ·mol-1
5、(温州市十校联合体高三联考)下列说法或表示法正确的是
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)→C(金刚石):ΔH = +119 kJ· mol-1可知,金刚石比石墨稳定
C.在稀溶液中:H+(aq)+OH-aq)-===H2O(l);ΔH=-57.3 kJ· mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)===2H2O(l);ΔH=-285.8 kJ· mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com