
29、[江苏省启东中学2009届高三第一学期第二次月考 ]下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。
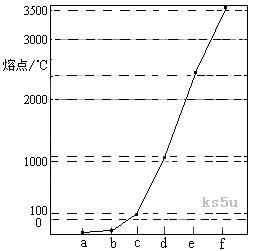
(1)请写出上图中d单质对应元素原子的电子排布式 。
 (2)单质a、f对应的元素以原子个数比1 :1形成的分子(相同条件下对H2的相对密度为13)中含 个
(2)单质a、f对应的元素以原子个数比1 :1形成的分子(相同条件下对H2的相对密度为13)中含 个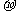 键和 个
键和 个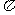 键。
键。
(3)a与b的元素形成的10电子中性分子X的空间构型为 ;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到络离子的化学式为 ,其中X与Ag+之间以 键结合。
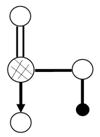
(4)右图是上述六种元素中的一种元素形成的含氧酸的结构:请简要说明该物质易溶于水的两个数原因 。
答案.(1)1s22s22p6 3s2 3p63d104s1(2分) (2)3 2 (各2分)
(3)三角锥形(1分);[Ag(NH3)2]+(1分),配位(2分)
(4)HNO3是极性分子,易溶于极性的水中(1分);HNO3分子中的-OH易与水分子之间形成氢键(1分)

28.[江苏省南通市2009届高三期中检测11月]下列物质固态时熔点的比较正确的是[B ]
A.F2>C12>Br2 B.金刚石>NaCl>02
C.S>NaBr>金刚石 D.Na>CH4>冰
27.[江苏省南通市2009届高三期中检测11月]据某科学杂志报道,国外有一研究发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60印结构。下列叙述不正确的是[ AC]
A.该物质有很高的熔点、很大的硬度 B.该物质形成的晶体属分子晶体
C.该物质分子中Si60被包裹在C60里面 D.该物质的相对分子质量为2400
16.[江苏省南通市2009届高三期中检测11月]下列化学式对应的结构式从成键情况看不合理的是 [ D]

25.[江苏省南通市2009届高三期中检测11月]C1S03H称为氯磺酸,是一种强酸。对于反应:ClS03H+HCOOH=CO+HCl+H2S04有如下判断,其中较合理的是 [ BC]
A.此反应属于氧化还原反应 B.此反应不属于氧化还原反应
C.反应后溶液的pH值变小 D.反应后溶液的pH值增大
24.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]部分中学化学常见元素原子结构及性质如表所示:
|
序 号 |
元素 |
结构及性质 |
|
① |
A |
A是生活中常见金属,它有两种氯化物,相对原子质量相差35.5 |
|
② |
B |
B原子最外层电子数是内层电子数的1/5 |
|
③ |
C |
C单质分子中含化学键数最多,单质稳定,但其原子较活泼 |
|
④ |
D |
D被誉为“信息革命的催化剂”,常用的半导体材料 |
|
⑤ |
E |
通常情况下,E没有正化合价,A、B、C、D都能与E化合 |
|
⑥ |
F |
F在周期表中可以排在IA族,也有人提出排在ⅦA族、ⅣA族 |
(1)如果A与冷的浓硝酸作用发生钝化,工业上冶炼A单质的化学方程式为
____________________________________________
(2)A的氯化物的浓溶液分别滴入冷水、热水中,得到黄色和红褐色液体,区别两种液体的方法是________________________________________________________
(3)B与C简单离子的半径大小为_________________(用离子符号表示)
(4) C和D形成的化合物的熔点很高,是一种无机非金属材料,其晶体类型为_____________
(5) F与E可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方法为:___________________________________________,F与C组成的两种化合物M、N,所含电子数分别与X、Y相等,请写出M的电子式___________,N的化学式___________.
(6)在上述六种元素中,选两种元素组成化合物甲,甲既含有离子键又含有共价键,甲的化学式为___________
答案.(1)(2分)Fe2O3 + 3CO 3CO2 + 2Fe
|
(3) (1分)Mg2+<N3-
(4) (1分)原子晶体
(5) (2分)分别加入MnO2有大量气泡产生的为H2O2 , N2H4
(6) (1分)NH4H
23.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]下列叙述中错误的是
A.能跟酸反应的氧化物,不一定是碱性氧化物
B.凡具有正四面体结构的分子中,其键角均为109°28′
C.有新单质生成的化学反应不一定都是氧化-还原反应
D.原子晶体中一定含有共价键,离子晶体一定含有离子键
22.[江苏省前黄高级中学09届上学期高三化学第二次周练卷 ]冶金工业上常用电解熔融MgCl2而不用电解MgO的方法制取镁,其原因是[C]
A.熔融的MgO不导电 B.MgO分子间作用力很大
C.MgO熔点高 D.MgO属原子晶体
16.(浙江省开化中学08年1月高三模拟)下列说法或表示法正确的是
A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B、由C(石墨)→C(金刚石):ΔH = +119 kJ· mol-1可知,金刚石比石墨稳定
C、在稀溶液中:H++OH-===H2O;ΔH=-57.3 kJ· mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ
D、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)==2H2O(l);ΔH=+285.8 kJ· mol-1
15.(浙江省开化中学08年1月高三模拟)下列变化属于物理变化的是
A.熔融态的氯化钠导电 B.用加热的方法分离氯化钠固体和氯化铵固体
C.在氢氧化铁胶体中加入硫酸镁溶液,析出红褐色沉淀 D.将过氧化钠固体溶于水中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com