
20.[江苏省江安中学2009届高三年级第三次月考 ](12分)奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是:食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
(1)样品处理:准确称取一定量的固体样品奶粉,移入干燥的凯氏烧瓶中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
(2)NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸氨,再经过再经过碱化蒸馏后,氨即成为游离状态,游离氨经硼酸吸收。
(3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?



。 (2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
A、凯氏烧瓶中溶液转移移到容量瓶中时,未洗涤凯氏烧瓶
B、定容时,俯视刻度线
C、定容时,仰视刻度线
D、移液时,有少量液体溅出
(3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为
。
已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7
+ 2HCl + 5H2O = 2NH4Cl
+ 4H3BO3
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。则三聚氰胺中氮的含量为
。
答案. (1)往容量瓶中注入一定量的水,塞紧瓶塞,倒转过来,观察是否漏水,然后再正放,旋转瓶塞1800,又倒转过来,观察是否漏水,若都不漏水,则说明该容量瓶不漏水。
(2)B
(3)10.73%
(4)66.7%
19.[江苏省口岸中学2009届高三年级第二次月考化学试题](6分)5月12日四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂等。
(1)二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与SO2反应制得。请写出反应的离子方程式:
。
(2)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸不稳定可分解,反应的离子方程式为:HClO2 → ClO2↑+ H+ +Cl-+H2O(未配平)。当1 mol HClO2发生分解反应时,转移的电子数是 。
(3)过碳酸钠是一种有多用途的新型氧系固态漂白剂,化学式可表示为Na2CO3·3H2O2,它具有Na2CO3和H2O2的双重性质。过碳酸钠与下列物质均会发生化学反应而失效,其中过碳酸钠只发生了氧化反应的是 。
A.MnO2 B.KMnO4溶液 C.稀盐酸 D.Na2SO3溶液
答案.(1)2ClO3-+SO2=2ClO2+SO42- (2)0.8NA (3)B
18、[江苏省口岸中学2009届高三年级第二次月考化学试题] (11分)人类对氢气的研究更趋深入,“氢能”将是未来最理想的新能源。
(1)实验测得,1g氢气燃烧生成液态水时放出142.9kJ热量,则氢气燃烧的热化学方程式为___________ ________________。
(2)利用核能把水分解制氢气,是目前正在研究的课题。下图是其中的一种流程,其中用了过量的碘。(提示:反应②的产物是O2、SO2和H2O)

完成下列反应的化学方程式:反应①______________;反应②_____________________。此法制取氢气的最大优点是_____________________________。 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
(3)目前有科学家在一定条件下利用水煤气(CO+H2)合成甲醇:
CO(g)+2H2(g)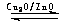 CH3OH(g)。甲醇的物质的量与反应温度的关系如下图所示:
CH3OH(g)。甲醇的物质的量与反应温度的关系如下图所示:
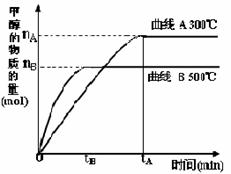
①合成甲醇反应,其反应热△H______0。(填“>”、“<”或“=”)
②据研究,合成甲醇反应体系中通入少量CO2有利于维持催化剂Cu2O的量不变,原因是(用化学方程式表示)_______________________________________。
答案.. (1) 2H2(g)+O2(g)==2H2O(g)△H=-571.6KJ/mol (2分)
(2) ①:SO2+I2+2H2O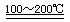 2HI+H2SO4(2分)
②:2H2SO4
2HI+H2SO4(2分)
②:2H2SO4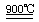 2SO2↑+O2↑+2H2O
(2分) SO2和I2 可循环使用,无污染。(2分)
2SO2↑+O2↑+2H2O
(2分) SO2和I2 可循环使用,无污染。(2分)
③:①:<
(1分) ②:Cu2O+CO Cu+CO2
(2分 不写可逆号扣1分)
Cu+CO2
(2分 不写可逆号扣1分)
17.[江苏省姜堰市姜淮培训中心2009届高三化学周练九]2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球 “最强悍”工程。 “鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜, 并采用新一代的氮化镓铟高亮度LED材料。有关说法正确的是[ C ]
并采用新一代的氮化镓铟高亮度LED材料。有关说法正确的是[ C ]
A.合金的熔点通常比组分金属高,硬度比组分金属小
B.已知Ga处于ⅢA主族,可推知氮化镓化学式为Ga3N2
C.用金属铝与V2O5冶炼钒,铝作还原剂
D.ETFE膜( )是由两种单体缩聚而成的
)是由两种单体缩聚而成的
16. [江苏省姜堰市姜淮培训中心2009届高三化学周练九](14分)近期有两件事引起了人们的极大关注。
[江苏省姜堰市姜淮培训中心2009届高三化学周练九](14分)近期有两件事引起了人们的极大关注。
(1)“问题奶粉”①其问题主要是掺杂了三聚氰胺,该物质的结构如图,该物质的含氮量为 ,蛋白质是由不同氨基酸组成的,根据组成的不同,其含氮量一般在15~17.6%之间变化。而农业用氮肥中包括碳酸氢铵、硝酸铵以及尿素,含氮量依次增加,以尿素最高,理论值为 现代工业合成三聚氰胺主要使用尿素为原料,在加热和一定压力条件下生成该物质及氨和二氧化碳,试写出化学方程式
_______________________
②该物质遇强酸或强碱水溶液水解,氨基逐步被羟基取代,先生成三聚氰酸二酰胺,进一步水解生成三聚氰酸一酰胺,最后生成三聚氰酸。经研究表明三聚氰胺和三聚氰酸在肾细胞中结合沉积从而形成肾结石,堵塞肾小管,最终造成肾衰竭。试写出三聚氰胺生成三聚氰酸的化学方程式 。
(2) “神七问天” ①联氨(N2H4)是航天飞船常用的高能燃料。联氨是一种无色可燃的液体,溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式: 。
②联氨也可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种盐和水,写出其反应的化学方程式 。
③火箭推进器中分别装有联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。已知:12.8 g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量;H2O(l)=H2O (g) DH=+44 kJ·mol-1 2H2O2(l)=2H2O(l)+ O2(g) DH=–196.4 kJ·mol-1则写出表示联氨燃烧热的热化学方程式为 。
答案..(14分)(1)66.7%(2分), 46.7%(2分),
6 (NH2)2CO → C3H6N6 + 6 NH3 + 3 CO2(2分)
②C3H6N6+3H2O=C3N3(OH)3+3NH3
(2) ①N2H4+H2O NH2NH3+(N2H5+)+OH- (2分)
NH2NH3+(N2H5+)+OH- (2分)
(NH2NH3++
H2O NH3NH32++OH- )
NH3NH32++OH- )
② CO(NH2)2+ NaClO+ 2NaOH = N2H4+NaCl+Na2CO3 +H2O (2分)
③N2H4(l)+O2(l)=N2(g)+2H2O(l) ΔH=-621.23 kJ·mol-1 (2分)
w.w.w.k.s.5.u. c.o.m
15.[江苏省姜堰市姜淮培训中心2009届高三化学周练九](8分)汽车内燃机工作时产生的高温会引起N2和O2的反应:N2(g)+O2(g)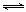 2NO(g),是导致汽车尾气中含有NO的原因之一。某同学为控制污染,对该反应进行研究。
2NO(g),是导致汽车尾气中含有NO的原因之一。某同学为控制污染,对该反应进行研究。
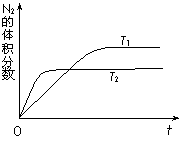 ⑴右图表示在T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图像,根据图像判断反应N2(g)+O2(g)
⑴右图表示在T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图像,根据图像判断反应N2(g)+O2(g)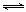 2NO(g)为 (填“吸热”或“放热”)反应。
2NO(g)为 (填“吸热”或“放热”)反应。
⑵2000℃时,向容积为2L的密闭容器中充入10molN2与5mol O2,达到平衡后NO的物质的量为2mol,则2000℃时该反应的平衡常数K= 。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为 。
⑶为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置。净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。
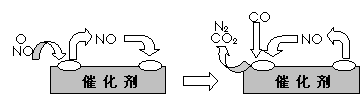
写出上述变化中的总化学反应方程式: 。
答案..(1)吸热(2)1/9,1/7(3)2NO+O2+4CO=4CO2+N2
用烧杯取少量样品,将一颗光亮的铁钉放入烧杯,浸泡一段时间。对可能产生的现象有如下假设:
假设①:有明显现象;
假设②:无明显现象。
(4)基于假设①,结论是铁钉被腐蚀,预期的实验现象是___________________________。
(5)基于假设②,结论是___________________________________________,请设计实验进一步验证该结论,叙述实验操作:_____________________________________
________________________。
答案..(1)碱性(1分) ClO- + H2O  HClO + OH- (2分)
HClO + OH- (2分)
(2)氧化性 漂白性 不稳定性 (任写两个,每空1分)
(3)CO2等酸性气体、光和热 (2分)
(4)铁钉表面出现铁锈(或红褐色固体) (1分)
(5)铁钉可能未被腐蚀,也可能被腐蚀但无明显现象 (1分)
用试管取出少量浸泡后的溶液,滴加足量的稀硫酸酸化,再滴加几滴KSCN溶液。(2分)
13\[江苏省启东中学2009届高三阶段调研测 ].禽流感是一种由甲型流感病毒(H5N1)的一种亚型引起的传染性疾病,被国际兽疫局定为甲类传染病。2005年10月25日国家根据禽流感疫情,在疫区到处洒上了石灰,甚至在树上也洒上了石灰,很是醒目。根据有关的化学知识判断下列说法中不正确的是[ CD ]
A.石灰之所以可以杀灭H5N1亚型高致病性禽流感病毒,是由于石灰与水反应产生的氢氧化钙显强碱性,病毒为蛋白质,可以使蛋白质变性,而使病毒失去活性
B.饱和石灰水中加入生石灰,在温度不变的情况下,pH不变
C.饱和石灰水中加入生石灰,在温度不变的情况下,Ca2+的物质的量不变
D.给饱和石灰水溶液升高温度,c(Ca2+)的浓度不变
14、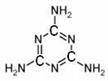 [江苏省启东中学2009届高三第一学期第二次月考 ]化学工作者和社会各界都一直关注食品安全问题,目前国内的“三鹿毒奶粉”事件是不法奶商向原奶中加入了三聚氰胺,其结构简式如右下图。下列关于三聚氰胺的说法不正确的是[ C ]
[江苏省启东中学2009届高三第一学期第二次月考 ]化学工作者和社会各界都一直关注食品安全问题,目前国内的“三鹿毒奶粉”事件是不法奶商向原奶中加入了三聚氰胺,其结构简式如右下图。下列关于三聚氰胺的说法不正确的是[ C ] 
A.含有不饱和碳原子,在一定条件下能发生加成反应
B.不法分子因为三聚氰胺含氮量较高才用其造假
C.分子中所有原子都在同一平面上
 D.在一定条件下能发生氧化反应
D.在一定条件下能发生氧化反应
该消毒液对碳钢制品是否有腐蚀作用?
8.(江苏省海安县2009届高三年级期初调研考试)海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( A )
A.从海水中可得到NaCl,电解熔融NaCl或其水溶液都可制得Cl2
B.因海水中含有镁元素,故不需经过化学变化就可以得到镁单质
C.利用蒸馏原理从海水中提取淡水是海水淡化技术发展的新方向
D.无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能
9\(江苏省栟茶09高三化学测试卷11月).回收的废旧锌锰于电池经过处理后得到锰粉(含MnO2、Mn(OH)2、Fe、乙炔和黑炭等),由锰粉制取MnO2的步骤如下图所示。
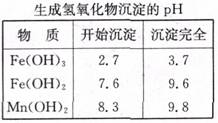
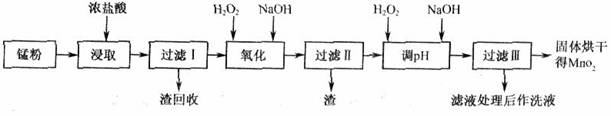 根据上图所示步骤并参考表格数据,回答下列问题。
根据上图所示步骤并参考表格数据,回答下列问题。
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等。MnO2与浓盐酸反应的离子方程式为________________________________。
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是__________________________。
(3)过滤I所得滤液经氧化后,需加入NaOH溶液调节pH约为5.1,其目的是______________________________________。
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离于方程式为__________________________________________。
(5)实验室进行过滤操作时.需要用到的玻璃仪器有___________________________。
7.(江苏省海安县2009届高三年级期初调研考试)下列选项体现了物质物理性质的是( C )
A.纯碱除去油污 B.食醋清洗水垢
C.木炭吸附色素 D.臭氧消毒餐具
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com