
10.[江苏省南通市2009届高三期中检测11月] (6分)气体A由C、H、F、S中的三种元素组成。将标准状况下1.12L气体A在过量的02中完全燃烧,后恢复到原状态,放出25kJ的热量。已知气态生成物全部被过量的Ca(OH)2溶液吸收,可以得到6.95g沉淀。再取相同条件下的1.12L气体A装入一个薄膜袋里,袋和气体的总质量为2.20g。(已知CaS03、CaF2、CaC03)难溶于水)
(1)根据上述数据估算,A的相对分子质量不会大于 。
(2)通过计算、分析可确定A的化学式为 。
(3)薄膜袋的质量为 。
(4)写出该条件下A在02中燃烧的热化学方程式: 。
答案.(1)44
(2)CH3F
(3)O.50g
(4)2CH3F(g)+302(g)→2C02(g)+2HF(g)+2H20(l); △H=一1000kJ·mol一1
9.[江苏省南通市2009届高三期中检测11月] (6分)将1.05g铝和过氧化钠的混合物放入一定量的水中,充分反应后固体无剩余。再向其中加入50mL 1 mol·L一1的盐酸,可恰好使反应过程中产生的沉淀消失。求原混合物中铝、过氧化钠各多少克?
.解:有关反应为:2Na2O2+2H2O=4NaOH+02↑
2Al+2NaOH+2H2O=2NaAl02+3H2↑
NaAlO2+HCl+H20=Al(OH)3↓+NaCl
A1(OH)3+3HCl3+3HCl=AlCl3+3H20
 最终溶液中所含溶质为NaCl、AlCl3,
最终溶液中所含溶质为NaCl、AlCl3,
设NaCl、AlCl3的物质的量分别为x mol,ymol,则Na202、Al的物质的量分别为 ,依题意有:

8.[江苏省南通中学2008学年度第一学期期末复习高三化学1月 ]某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。
(1) 该结晶水合物中含有的两种阳离子是________和________,阴离子是_________。
 (2)试通过计算确定该结晶水合物的化学式。
(2)试通过计算确定该结晶水合物的化学式。
(3)假设过程中向该溶液中加入的NaOH溶液的物质的量浓度为5mol/L,请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。
答案(1)NH4+ Al3+ SO42- (3分)
(2)n(SO42-)=0.2mol
n(NH4+)=0.1 mol n(Al3+)=0.1 mol,
n(H2O)=1.2mol
化学式为NH4 Al (SO4)2·12H2O
[或(NH4)2SO4·Al2(SO4)3·24H2O] (5分)
(3)(2分)
7.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得K2O(10K+2KNO3→6K2O+N2),39.0g钾与10.1g硝酸钾充分反应生成K2O的质量为 g。
⑵某过氧化钾样品中氧的质量分数(杂质不含氧)为0.28,则样品中K2O2的质量分数为 。
⑶超氧化钾和二氧化碳反应生成氧气(4KO2+2CO2→2K2CO3+3O2),在医院、矿井、潜水、高空飞行中用作供氧剂。13.2L(标准状况)CO2和KO2反应后,气体体积变为18.8L (标准状况),计算反应消耗的KO2的质量。
⑷KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比。
答案、.⑴28.2 (2分)。 ⑵96.25%(2分)。 ⑶71 g(2分)。
⑷n(K):n(O)=2:3(2分);n(KO2):n(K2O2) = 2:1(1分),n(KO2):n(K2O) = 4:1(1分)。
6.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]蛋白质主要由氨基酸组成,平均含氮量为16%左右。通用的蛋白质测试方法--凯式定氮法--是通过测出含氮量来估算蛋白质含量,主要原理为:将食品与硫酸和催化剂一起加热,使蛋白质分解,分解的氨用硼酸吸收后再以盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
已知:1mol氨基能产生1mol氨气;
2NH3+4H3BO3→(NH4)2B4O7+5H2O;
(NH4)2B4O7+2HCl+5H2O→2NH4Cl+4H3BO3
某兴趣小组进行了如下实验:
步骤I 称取样品1.500g。
步骤II (略)
步骤Ⅲ 共得到1L吸收了氨的硼酸样品溶液,从中移取10.00mL于250mL锥形瓶中,加入少量水和指示剂,用0.010mol/L的盐酸滴定至终点。
⑴根据步骤Ⅲ填空:
①滴定管用蒸馏水洗涤后,直接加入盐酸进行滴定,则测得样品中氮的质量分数
(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去盐酸的体积 (填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察 。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
⑵滴定结果如下表所示:
|
滴定次数 |
待测溶液的体积(mL) |
标准溶液的体积 |
|
|
初读数(mL) |
末读数(mL) |
||
|
1 |
10.00 |
0.00 |
14.90 |
|
2 |
10.00 |
0.10 |
15.05 |
|
3 |
10.00 |
0.50 |
17.00 |
该样品中氮的质量分数为 。
答案⑴①偏高(2分)。 ②无影响(2分)。 ③锥形瓶内溶液颜色的变化(2分)
⑵13.93%(3分)
5.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]某中学化学教材上有如下介绍:“在氢氧化钠浓溶液中加入氧化钙,加热,制得白色固体就是碱石灰,它是水和二氧化碳的吸收剂”。有两个实验小组决定通过实验来探究碱石灰的组成。
(1)第一小组设计的实验方案如下:

下列关于溶液中n(OH-)、n(Ca2+)、n(Na+)之间的关系式正确的是________
A. n(Na+)+ 2n(Ca2+)= n(OH-) B. 2n(Na+) + 2n(Ca2+)= n(OH-)
C. n(Na+)+ n(Ca2+)= 2n(OH-)
现有4.0g碱石灰,设其中n(Na+)= xmol, n(Ca2+)= ymol,请填写下列空格:
|
碱石灰的可能组成 |
NaOH, CaO |
NaOH,
CaO, Ca(OH)2 |
NaOH, Ca(OH)2 |
NaOH,
Ca(OH)2 H2O |
|
x,y之间关系式(等式或不等式) |
A |
40x+56y﹤4.0﹤ 40x+74y |
B |
C |
把表中A、C的关系式填在下面空格上:
A:__________________________C:______________________ 。
(2)第二小组查得如下资料:氢氧化钙在250℃时不分解,高于250℃时才分解;氢氧化钠在580℃时不分解。他们设计了如下方案并得出相应相关数据:取市售碱石灰4.0g,在250℃时加热至恒重,测得固体质量减少了0.6g,剩余固体在580℃时继续加热至恒重,测得固体质量又减少了0.7g.请通过计算确定该碱石灰各成分的质量分数?(要计算过程)
答案(1)(3分)A A:40x+56y=4.0 C:40x+74y﹤4.0
(2) (3分)NaOH%=13% Ca(OH)2%=72% H2O%=15%
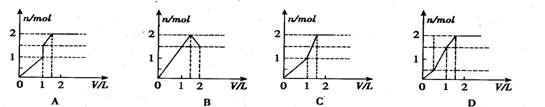
3.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]向含 l mol HCl和l mol MgSO4的混合溶液中加入1 mol/L Ba(OH)2溶液,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图正确的是
4[江苏省南通中学2008学年度第一学期期末复习高三化学 ].amolFeS,bmolFeO投入VL c mol/L的硝酸溶液中充分反应, 产生NO气体,所得澄清溶液可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为 ( B )
A.(a+b)×63g B.(a+b)×189g
C.(a+b)mol D.(Vc -(a+b)/3)mol
2.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]常温下,有甲、乙两份体积均为1L,浓度均为0.1mol/L的氨水,其pH为11。①甲用蒸馏水稀释100倍后,溶液的pH将为a;②乙与等体积、浓度为0.1mol/L的HCl混合,在混合液中:n(NH4+) + n(H+) – n(OH-)=bmol 则a、b正确的答案组合是
A.9-11之间 ;0.1 B.9-11之间 ;0.05
C.12-13之间 ;0.2 D.13 ;0.1
1.[江苏省南通中学2008学年度第一学期期末复习高三化学 ]金属镁溶于一定浓度的硝酸的反应中,产生标准状下的N2O气体5.6L,在所得的溶液中加入适量的氢氧化钠溶液,完全反应后过滤出沉淀,经洗涤并充分灼烧,最后得到固体物质的质量为
A.58g B.29g C.40g D.20g
2.[江苏省兴化市2008-2009学年高三年级第一学期期中调研 ](10分)2008年9月24日,国家重点工程--川维20万吨合成氨项目顺利实现中间交接。合成氨是生产尿素、磷酸铵、硝酸铵等化学肥料的主要原料,工业生产过程是以天然气或煤炭等为原料通过水蒸气重整工艺制得氢气,然后在一定条件下与氮气进行合成制得合成氨。
⑴已知合成氨反应的热化学方程式如下:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H=-92.4KJ/mol

① 当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如上图所示。图中t2起平衡移动的条件可能是 。
其中表示平衡混合物中NH3的含量最高的一段时间是 。
②温度为T℃时,将2amolH2和amolN2放入0 . 5L密闭容器中,充分反应后测得N2的转化率为50﹪。则反应的平衡常数为 (用带a的代数式表示)
⑵科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、压力1.0×105 Pa、反应时间3 h):
|
T/K |
303 |
313 |
323 |
353 |
|
NH3生成量/(10-6 mol) |
4.8 |
5.9 |
6.0 |
2.0 |
相应的热化学方程式如下:
N2(g)+3H2O(1)==2NH3(g)+ 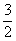 O2(g) △H1=+765.2 kJ·mol-1
O2(g) △H1=+765.2 kJ·mol-1
回答下列问题:
① 试在答题纸对应的图像中用虚线表示在上述反应中使用催化剂后能量的变化情况。
②与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com