
11.(江苏省射阳中学2009届高三第二次月考)I.(2分)下列实验操作、试剂保存方法和实验室事故处理,一定正确的是 (填序号)。
A.不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
B.制备氢氧化铁胶体时,应向沸水中逐滴滴加1-2 mL饱和的FeC13溶液,并继续加
热到液体呈透明的红褐色为止
C.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液滴在用蒸馏水湿润过的pH试纸上,并与标准比色卡比较
D.实验室中,浓硝酸保存在带橡胶塞的棕色细口试剂瓶中
E.除去蛋白质溶液中混有的NaC1,可以先加入AgNO3溶液,然后过滤
F.在进行反应热测定时,为保证实验的准确性,我们可以采取以下具体措施:使用碎
泡沫以起到隔热保温的作用、使用铜质搅拌棒进行搅拌、使用的酸碱正好反应、进
行两到三次实验,取平均值
II.(8分)石灰石的主要成份是碳酸钙,含氧化钙约40~50%,较好的石灰石含CaO约45~53%。此外还有SiO2、Fe2O3、Al2O3及MgO等杂质。测定石灰石中钙的含量时将样品溶于盐酸,加入草酸铵溶液,在中性或碱性介质中生成难溶的草酸钙沉淀 (CaC2O4·H2O),将所得沉淀过滤、洗净,用硫酸溶解,用标准高锰酸钾溶液滴定生成的草酸,通过钙与草酸的定量关系,间接求出钙的含量。涉及的化学反应为: H2C2O4 + MnO4- + H+ → Mn2+ + CO2 ↑+ H2O(未配平)。CaC2O4 沉淀颗粒细小,易沾污,难于过滤。为了得到纯净而粗大的结晶,通常在含Ca2+的酸性溶液中加入饱和 (NH4)2C2O4 ,由于C2O42-浓度很低,而不能生成沉淀,此时向溶液中滴加氨水,溶液中C2O42-浓度慢慢增大,可以获得颗粒比较粗大的CaC2O4沉淀。沉淀完毕后,pH应在3.5~4.5,这样可避免其他难溶钙盐析出,又不使CaC2O4溶解度太大。根据以上材料回答下列问题:
(1)样品溶于盐酸后得到的沉淀物主要是 (写化学式)
(2)沉淀 CaC2O4要加入沉淀剂饱和的 (NH4)2C2O4 溶液,为什么?
(3)工业中通常先用0.1%草酸铵溶液洗涤沉淀,再用冷的蒸馏水洗涤,其目的是:
(4)若开始用去m g样品,最后滴定用去浓度为c mol/L 的KMnO4 溶液V mL,推出
CaO含量与 KMnO4的定量计算关系。ω%=
答案. I AB
II(1)SiO2 (2)保持较大的C2O42-离子浓度,使Ca2+沉淀完全。
(3)降低CaC2O4在水中的溶解度,减少沉淀的损失,降低实验误差。
(4)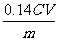 或
或 %
%  w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
10、(淮阳一高09高三一轮复习月考(11月份)一定温度和压强下,乙腈(CH3CN)是极易溶于水的无色液体,这时向质量分数为a的乙腈水溶液中加入等体积的水,所得溶液中乙腈的质量分数为0.4a。若同样条件下乙腈的密度为d1,水的密度为d2,则下列说法正确的是[A]
A、d1 < d2 B、d1 > d2 C、d1 == d2 D、无法确定
0.1mol/L) 中汞元素的主
要存在形态是 。少量
Hg(NO3)2溶于0.001mol/L
的盐酸后得到无色透明溶液,
其中汞元素的主要存在形态
是 。
(2)Hg(NC3)2固体易溶于水,但溶于水时常常会出现浑浊,其原因是 (用离子方程式表示),为了防止出现浑浊,可采取的措施是 。
(3)处理含汞废水的方法很多。下面是常用的两种方法,汞的回收率很高。
①置换法:用废铜屑处理含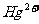 的废水。反应的离子方程式为 。
的废水。反应的离子方程式为 。
②化学沉淀法:用硫化钠处理含Hg(NO3)2的废水,生成HgS沉淀。已知
Ksp(HgS)=1.6X10-52,当废水中c(S2-)=1×10-5mol/L时,c(Hg2+)= 。
答案. (1)HgC142- HgC12
(2)Hg2++2H2O Hg(OH)2+2H+ 在硝酸中配制
(3)①Cu+Hg2+ Cu2++Hg ②1.6×10-47mol/L
9.(江苏省南京市2009届高三年级质量检测)(10分)水体中二价汞离子可以与多种阴离子结合成不同的存在形态。水溶液中二价汞主要存在形态与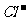 、
、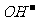 的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=一lgc(
的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=一lgc( ),pCl=一lgc(
),pCl=一lgc(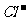 )]。
)]。 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
(1)正常海水( 的浓度大于
的浓度大于
8.(江苏省栟茶09高三化学测试卷11月)(10分)工业上制备BaCl2的工艺流程图如下:

某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查表得
BaSO4(s) + 4C(s) 4CO(g) + BaS(s)
△H1 = 571.2 kJ·mol-1 ①
4CO(g) + BaS(s)
△H1 = 571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2= 226.2 kJ·mol-1 ②
⑴气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
⑵向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,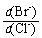 =
。
=
。
[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
⑶反应C(s) + CO2(g) 2CO(g)的△H2= kJ·mol-1。
2CO(g)的△H2= kJ·mol-1。
⑷实际生产中必须加入过量的炭,同时还要通入空气,其目的是
, 。
答案..⑴S2- + H2O HS- +OH- HS- + H2O
HS- +OH- HS- + H2O H2S +OH-(可不写)
H2S +OH-(可不写)
⑵2.7×10-3 ⑶172.5
⑷使BaSO4得到充分的还原(或提高BaS的产量)
①②为吸热反应,炭和氧气反应放热维持反应所需高温
7.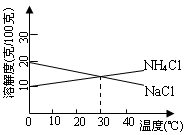 (江苏海门市2008-2009学年高三第一次教学质量调研) NaCl和NH4Cl共同存在时的溶解度曲线如图所示,利用NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,有利于析出NH4Cl。以下说法中正确的是[ C ]
(江苏海门市2008-2009学年高三第一次教学质量调研) NaCl和NH4Cl共同存在时的溶解度曲线如图所示,利用NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,有利于析出NH4Cl。以下说法中正确的是[ C ]
A.0℃时,饱和的NaCl和NH4Cl混合溶液中,
NaCl的物质的量浓度是NH4Cl的2倍
B.30℃时,饱和的NaCl和NH4Cl混合溶液中,
两者的物质的量浓度相等
C.通入的气体可能是NH3,控制在0~10 ℃结晶出NH4Cl
D.通入的气体可能是CO2,控制在30~40 ℃结晶出NH4Cl
6.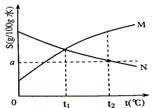 [江苏省口岸中学2008-2009学年度高三年级第一学期第四次调研测试]右图是M、N两种物质的溶解度曲线,在t2℃时往盛有100g水的烧杯中先后加入
[江苏省口岸中学2008-2009学年度高三年级第一学期第四次调研测试]右图是M、N两种物质的溶解度曲线,在t2℃时往盛有100g水的烧杯中先后加入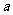 gM和
gM和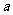 gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌,将混合物的温度降低到t1℃,下列说法正确的是[A]
gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌,将混合物的温度降低到t1℃,下列说法正确的是[A]
A.t1℃时,M、N的溶质质量分数一定相等
B.t1℃时,M、N的溶解度相等,得到M、N的饱和溶液
C.t2℃时,得到M的饱和溶液、N的不饱和溶液
D.t2℃时,M、N的物质的量浓度一定相等
5.
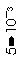
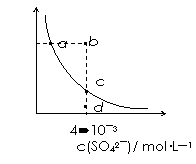 [江苏省口岸中学2008-2009学年度高三年级第一学期第四次调研测试]常温下,Ksp(CaSO4)=9´10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是[ C]
[江苏省口岸中学2008-2009学年度高三年级第一学期第四次调研测试]常温下,Ksp(CaSO4)=9´10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是[ C]
A.常温下CaSO4饱和溶液中,c(Ca2+)、c(SO42-)对应曲线上任意一点
B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于
3´10-3 mol·L-1
C.a点对应的Ksp等于c点对应的Ksp
D.d点溶液通过蒸发可以变到c点w.w.w.k.s.5.u. c.o.m
4.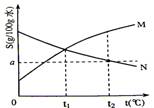 [江苏省姜堰市姜淮培训中心2009届高三化学周练九]右图是M、N两种物质的溶解度曲线,在t2℃时往盛有100g水的烧杯中先后加入
[江苏省姜堰市姜淮培训中心2009届高三化学周练九]右图是M、N两种物质的溶解度曲线,在t2℃时往盛有100g水的烧杯中先后加入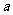 gM和
gM和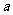 gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌,将混合物的温度降低到t1℃,下列说法正确的是[ D ]
gN(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌,将混合物的温度降低到t1℃,下列说法正确的是[ D ]
A.t1℃时,M、N的溶解度相等,得到M、N的饱和溶液
B.t2℃时,得到M的饱和溶液、N的不饱和溶液
C.t2℃时,M、N的物质的量浓度一定相等
D.t1℃时,M、N的溶质质量分数一定相等
3.[江苏省南通市2009届高三期中检测11月]40℃时,等质量的两份饱和石灰水,一份冷却至1℃,另一份加少量CaO并保持温度仍为40℃,这两种情况都不改变的是[ C]
A.Ca(OH)2的溶解度 B.溶液的质量
C.溶质的质量分数 D.溶液中Ca2+数目
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com