
6.[江苏省前黄高级中学09届上学期高三化学第二次周练卷 ](18分)铝镁合金已成为飞机制造、化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。w.w.w.k.s.5.u. c.o.m
[方案一]
[实验方案]将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
实验中发生反应的化学方程式是 。
[实验步骤]
(1)称取5.4g铝镁合金粉末样品,溶于V mL 2.0 mol/L NaOH溶液中。为使其反应完全,则NaOH溶液的体积V ≥ 。
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
(填“偏高”、“偏低”或“无影响”)。
[方案二]
[实验方案]将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01 105Pa)的体积。
105Pa)的体积。
[问题讨论]
(1)同学们拟选用下列实验装置完成实验:


①你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满。)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶。请你帮助分析原因 。
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 。
 w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m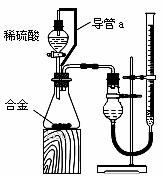
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸 滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。
①装置中导管a的作用是 。
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为__________mL。
答案.[方案一]2Al+2NaOH+2H2O=2NaAlO2+3H2↑(2分)(1)97mL(2分)(2)偏高(1分)
[方案二](1)①EDG(2分)
②锌与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大(2分)③ACD(3分)
(2)①使分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下;滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差。(4分) ②V1-V2 (2分)
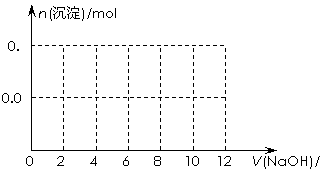
5. [江苏省前黄高级中学09届上学期高三化学第二次周练卷 ](10分)图为一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。试回答:
[江苏省前黄高级中学09届上学期高三化学第二次周练卷 ](10分)图为一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。试回答:
(1) A点时已参加反应的AlCl3和 NaOH的物质的
量之比为1比 。
(2) OA段曲线所表示的反应的离子方程式是
___________________。AB段曲线所表示的反应的离子方程式是___________________。
 (3)
B处溶液中存在的浓度最大的离子是 (填离子符号)。向B处生成的溶液中通入二氧化碳,可见到的现象是
。
(3)
B处溶液中存在的浓度最大的离子是 (填离子符号)。向B处生成的溶液中通入二氧化碳,可见到的现象是
。
(3) 向含有0.1mol NH4Al(SO4)2溶液中逐滴加入5mol·L-1NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有有刺激性气味的气体逸出;最后白色沉淀逐渐减少并最终消失。请在右图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。
答案.(1) 3(1分);
(2) Al3++3OH-=Al(OH)3↓(2分);Al(OH)3+OH-=AlO2-+2H2O(2分);
(3) Na+(1分);生成白色沉淀(1分)。
 (4) (3分)
(4) (3分)
4.[江苏省前黄高级中学09届上学期高三化学第二次周练卷 ](12分)蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下:
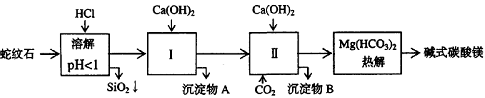
(1) 蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是________。
(2) 进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)Ca(OH)2不能过量, w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
若Ca(OH)2过量可能会导致 溶解、 沉淀。
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
开始沉淀pH |
1.5 |
3.3 |
9.4 |
(3) 从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_________ (填入物质的化学式),然后__________________________________ (依次填写实验操作名称)。
(4) 物质循环使用,能节约资源。上述实验中,可以循环使用的物质是______________(填写物质化学式)。
(5) 现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):①样品称量 ②高温分解 ③______________________________
④_____________________________ ⑤MgO称量
(6) 18.2g产品完全分解后,产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中:
a=_________、b=_________、c=_________。
答案.、(12分)(1)Fe3+ Al3+;(2)Al(OH) 3、Mg(OH)2;(3)NaOH,过滤、洗涤、灼烧;
(4)CO2;(5)③测出CO2的质量;④测出水蒸汽的质量;(6)3、1、3。
3.[江苏省前黄高级中学09届上学期高三化学第二次周练卷 ](12分);图中字母所代表的物质均为中学化学常见物质。其中A是日常生活中不可缺少的物质,也是化工生产上的重要原料;常温下C、D、H为气体单质。单质E、M、N为金属,N是地壳中含量最大的金属元素。Y是红褐色沉淀。这些物质在一定条件下存在如下转化 关系,其中有些反应物或生成物已经略去。试回答下列问题:

(1) 工业上,在电解A溶液的设备中将阴极区和阳极区用 隔开。
(2) Z→L反应的名称是 ,K的电子式为 。
(3) 写出B→F的离子方程式 。
(4) 写出K与CO2反应的化学方程式 。
(5) Y与NaClO和B混合溶液作用,是制备绿色水处理剂(Na2MO4)的一种方法,请写出有关反应的离子方程式 。
答案. (1)阳离子交换膜(2分);
(2)(4分);铝热反应, 
 (2分);
(2分);
 (2分);
(2分);
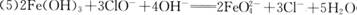 (2分);
(2分);
2.[江苏省前黄高级中学09届上学期高三化学第二次周练卷 ](10分)平达喜是常用的中和胃酸的药物,它的化学成分是铝和镁的碱式碳酸盐,其中氢元素的质量分数为0.040。取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全。若在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g。试通过计算推测该碱式盐的化学式。
答案.、(10分)n(CO32-)=0.005mol(2分),n(OH-)=0.08mol(2分),
n[Mg(OH)2]==0.03mol(2分),n(Al3+)=001mol(2分),
碱式盐中含有结晶水(1分),碱式盐的化学式为:Al2Mg6(OH)16CO3·4H2O(1分)。
1. [江苏省前黄高级中学国际分校09姐上学期综合练习三]最近,美国普度大学的研究人员开发出一种利用铝镓合金加水制造氢气的新工艺。这项技术具有广泛的能源潜在用途,包括为汽车提供原料、潜水艇提供燃料等。该技术通过向铝镓合金注水,铝生成氧化铝,同时生成氢气。合金中镓(Ga,ⅢA)是关键成分,可阻止铝形成致密的氧化膜。下列关于铝、镓的说法正确的是
[江苏省前黄高级中学国际分校09姐上学期综合练习三]最近,美国普度大学的研究人员开发出一种利用铝镓合金加水制造氢气的新工艺。这项技术具有广泛的能源潜在用途,包括为汽车提供原料、潜水艇提供燃料等。该技术通过向铝镓合金注水,铝生成氧化铝,同时生成氢气。合金中镓(Ga,ⅢA)是关键成分,可阻止铝形成致密的氧化膜。下列关于铝、镓的说法正确的是
A.铝的金属性比镓强 B.铝的熔点比镓低
C.Ga(OH)3与Al(OH)3性质相似,一定能与NaOH溶液反应
D.铝、镓合金与水反应后的物质可以回收利用冶炼铝
23.(江苏省南京市2009届高三年级质量检测)(10分)无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上制备无水AlCl3的方法是:将一定粒度的铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按一定配比投入焙烧炉中加热至800℃,再将焙烧过的物料投入到氯化炉中,然后通入Cl2和O2,于950℃在石油焦还原剂的存在下,Al2O3跟Cl2反应,生成气态的AlCl3经冷却后得到氯化铝粗产品(杂质的成分是FeCl3)。尾气中含有大量CO和少量Cl2,用碱液或Na2SO4溶液除去Cl2,并回收CO。精制AlCI3粗产品一般用升华法。在升华器内,加入NaCl固体,同时加入少量某种物质X,将FeCl3杂质还原成Fe作为废渣除去,再经升华就得到精制的AlCl3。回答下列问题:
(1)氯化炉中通入O2的目的是 。
(2)氯化炉中Al2O3、C12和C反应的化学方程式是 。
(3)用Na2SO3溶液处理尾气时发生反应的离子方程式是 。
(4)精制AlCl3粗产品时,需加入少量物质X。X可能是下列物质中的 。(填
字母)
A.FeCl2固体 B.Fe粉 C.Al粉
(5)精制无水AlCl3合格品中,AlCl3的质量分数不得低于96%。现称取16.25g精制后的无水 AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g。试计算该样品中AlCl3的质量分数(写出计算过程)。
答案 (1)跟C反应,提供反应所需要的热量。(1分)
高温
(2)A12O3+3C12+3C 2A1C13+3CO(1分)
(3)SO32-+C12+H2O SO42-+2C1-+2H+(1分)
(4)C(1分)
(5)解:2FeC13 - 2Fe(OH)3 - Fe2O3 (2分)
2×162.5 160
 0.16g
0.16g
 (2分)
(2分)
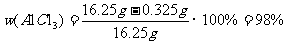 (2分)
(2分)
22.(江苏省前黄高级中学2008-2009学年第一学期高三期中试卷)(14分)明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:

根据上述图示,完成下列填空:
⑴.明矾石焙烧后用稀氨水浸出。配制500 mL稀氨水(每升含有39.20 g氨)需要取浓氨水(每升含有251.28 g氨)______mL,用规格为______mL量筒量取。
⑵.氨水浸出后得到固液混合体系,过滤,滤液中除K+、SO42-外,还有大量的NH4+。检验NH4+的方法是_______________________________________________________________。
⑶.写出沉淀物中所有物质的化学式_____________________。
⑷.滤液I的成分是水和________________。
⑸.为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,完善下列步骤:
①.称取钾氮肥试样并溶于水,加入足量________溶液,产生白色沉淀。
②._______、_______、________(依次填写实验操作名称)。
③.冷却、称重。
⑹.若试样为m g,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为:________mol(用含m、n的代数式表示)。
答案(1)78.00,100。
(2)取滤液少量于试管中,加入浓NaOH溶液,加热,生成的气体能使湿润的红色石蕊试纸变蓝的气体(2分) 。
(3)Al(OH)3、Al2O3、Fe2O3。
(4)K2SO4、(NH4)2SO4
(5)①BaCl2或Ba(OH)2 ②过滤、洗涤、干燥(或烘干)。
(6)mol。(2分)
21.(江苏省前黄高级中学2008-2009学年第一学期高三期中试卷)在a LAl2(SO4)3和(NH4)2SO4的混合溶液中加入bmol的BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到cmolNH3,则原溶液中的Al3+的浓度(mol/L)为[ B]
A. B. C. D.
20.(江苏如皋市搬经镇中2009届高三第一学期期中)有一包镁粉和氧化镁的混合物,由实验测得其中氧元素质量分数为32﹪,则其中氧化镁的质量分数是[ D ]
A、20﹪ B、40﹪ C、48﹪ D、80﹪
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com