
11.(08南师附中最后预测)常温下,有甲、乙两份体积均为l L,浓度均为0.1mol/L的氨水,其pH为11。①甲用蒸馏水稀释100倍后,溶液的pH将为a;②乙与等体积、浓度为0.2mol/L的盐酸混合,在混合溶液中:n(NH4+)+n(H+)-n(OH-)=bmol。则a、b正确的答案组合是
A.9-11之间; 0.1 B.9-11之间; 0.2
C.12-13之间; 0.2 D.13; 0.1
10.已知甲酸钠(HCOONa)溶液呈碱性。室温下用pH相同、体积相同的盐酸与甲酸(HCOOH)溶液分别进行如下实验,下列相关叙述正确的是
A.分别加入等体积水稀释,盐酸中c(H+)比甲酸中c(H+)小
B.分别用等物质的量浓度的NaOH溶液中和,盐酸比甲酸消耗的碱液少
C.分别跟等质量铝粉反应,盐酸比甲酸的起始反应速率快
D.分别跟过量的锌粒反应,盐酸比甲酸产生氢气的量多
9.在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法正确的是
A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大
B.甲烧杯中的酸过量
C.两烧杯中参加反应的锌等量
D.反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小
8. (08天津)醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
(08天津)醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的
pH<7
7.已知25℃时有关弱酸的电离平衡常数:
|
弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
|
电离平衡常数(25℃) |
1.8×l0_5 |
4.9×l0_10 |
K1=4.3×l0_7 K2=5.6×l0_11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合后,所得溶液中
c(Na+)>c(CN-),则a一定大于b
C.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+ c(H+)=c(OH-)+ c(HCO3-) +2c(CO32-)
6.已知酸式盐NaHB在水溶液中存在下列反应:
①NaHB == Na+ + HB-,②HB-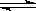 H++B2-,③HB-+H2O
H++B2-,③HB-+H2O 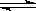 H2B+OH-
H2B+OH-
且溶液中c(H+)>c(OH-),则下列说法一定正确的是
A.NaHB为强电解质 B.H2B为强酸
C.H2B为弱电解质 D.HB-的电离程度小于HB-的水解程度
5.25℃时,水的电离达到平衡:H2O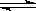 H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
A 向水中加人稀氨水,平衡逆向移动,c(OH―)降低
B 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C 向水中加人少量固体CH3COONa,平衡逆向移动,c(H+)降低
D 将水加热,Kw增大,pH不变
4.在常温下,纯水中存在电离平衡H2O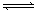 H++OH-,若要使水溶液的酸性增强,并使水的电离程度增大,应加入的物质是
H++OH-,若要使水溶液的酸性增强,并使水的电离程度增大,应加入的物质是
A.NaHSO4 B.KAl(SO4)2 C.NaHCO3 D.CH3COONa
3.在体积均为1L,pH均等于2的盐酸和醋酸溶液,分别投入0.23g Na,则下图中比较符合反应事实的曲线是

2.(镇江市09第二次调研测试)醋酸是电解质,下列事实能说明醋酸是弱电解质的组合是
①醋酸与水能以任意比互溶 ②醋酸溶液能导电
③醋酸溶液中存在醋酸分子 ④0.1 mol·L-1醋酸的pH比0.1 mol·L-1盐酸pH大
⑤醋酸能和碳酸钙反应放出CO2 ⑥0.1 mol·L-1醋酸钠溶液pH=8.9
⑦大小相同的锌粒与相同物质的量浓度的盐酸和醋酸反应,醋酸产生H2速率慢
A.②⑥⑦ B.③④⑤⑥ C.⑨④⑥⑦ D.①②
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com