
56.(江苏海门市2008-2009学年高三第一次教学质量调研)某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是[ B]

A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
55.(江苏海门市2008-2009学年高三第一次教学质量调研)(10分)离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。


(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。
|
①所有的离子方程式均可以表示一类反应 |
|
|
②酸碱中和反应均可表示为:H++OH-=H2O |
|
|
③离子方程式中凡是难溶性酸碱盐均要用“↓” |
|
答案..(10分)(每空2分) (1) ③⑤; (2)见右图; w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
(3) ①如2Na+2H2O=2Na++2OH-+H2↑;
②如CH3COOH+NH3×H2O=CH3COO-+NH4++H2O;
③如Al3++3H2O=Al(OH)3+3H+;
54.(江苏海州高级中学2009届高三化学第三次综合测试)能在溶液中大量共存,加入(NH4)2Fe(SO4)2·6H2O晶体后仍能大量存在的离子组是[ B ]
A.Na+、H+、Cl-、NO3- B.Na+、Mg2+、Cl-、SO42-
C.K+、Ba2+、OH-、I- D.Cu2+、S2-、Br-、ClO-
53. (江苏海州高级中学2009届高三化学第三次综合测试)下列离子方程式书写正确的是[ B ]
(江苏海州高级中学2009届高三化学第三次综合测试)下列离子方程式书写正确的是[ B ]  w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
A.石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓
B.NH4HSO3溶液与足量的NaOH溶液混合加热:
NH4++HSO3-+2OH- NH3·H2O+SO32-+H2O
NH3·H2O+SO32-+H2O
C.酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+6H+=3I2+3H2O
D.AgNO3溶液中加入过量的氨水:Ag++NH3·H2O=AgOH +NH4+
52.(江苏海州高级中学2009届高三化学第三次综合测试) (10分)(1)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。
该反应中还原产物是______;若反应过程中转移了0.3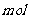 电子,则氧化产物的质量是______
电子,则氧化产物的质量是______ 。
。
(2)将a mol Cl2 通入含b mol FeBr2的溶液中,当0< a / b≤1/2 时,反应的离子方程式为:
2Fe2+ + Cl2 = 2Fe3+ + 2Cl- ,写出另2个可能发生的离子方程式。
① 当 a / b =1时____________________________________________;
② 当a / b≥3/2时____________________________________________。
③ (3)观察如下反应,总结规律,然后完成下列问题:
①Al(OH)3 +H2O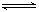 Al(OH)4- + H+ ②NH3+H2O
Al(OH)4- + H+ ②NH3+H2O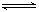 NH4+ + OH_
NH4+ + OH_
(A)已知B(OH)3是一元弱酸,试写出其电离方程式__________________________________
(B)N2H4是二元弱碱,试写出其第二步电离方程式____________ ________________
答案..(1)NO 4.8g (2分) (2) ①2Cl2 + 2Fe2+ + 2Br- = 4Cl- + 2Fe3+ + Br2
②3Cl2 + 2Fe2+ + 4Br- =2Fe3+ + 2Br2 + 6Cl-
(3)B(OH)3+H2O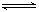 B(OH)4- + H+ N2H5+ +H2O
B(OH)4- + H+ N2H5+ +H2O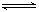 N2H62+ + OH_
N2H62+ + OH_
51.[江苏省江安中学2009届高三年级第三次月考 ]下列有关离子大量共存的说法正确的是[ D ]
A. S2-、Na+、Fe3+、SO42-能大量共存
B.水电离产生c(H+)=1×10-12mol/L的溶液中,可能有Mg2+、Na+、Cl-、HCO3大量共存
C.澄清透明的溶液中,可能有Ba2+、Cl-、Al3+、SO42-大量共存
 D.在K+、AlO2-、Cl-、SO42- 溶液中加入过量Na2O2后仍能大量共存
D.在K+、AlO2-、Cl-、SO42- 溶液中加入过量Na2O2后仍能大量共存
50.[江苏省江安中学2009届高三年级第三次月考 ]某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使红色石蕊试纸变蓝。由该实验能得到的正确结论是[ B ]

A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
49.[江苏省江安中学2009届高三年级第三次月考 ]某白色固体可能由①NH4Cl②AlCl3③NaCl④AgNO3⑤KOH中的一种或几种组成,将此固体投入水中得到澄清溶液,该溶液可使酚酞呈红色。若向该溶液中加入稀硝酸至过量,有白色沉淀生成。对原固体组成的判断不正确的是[ B ] A.可能存在② B.至少有②⑤ C.无法确定是否有③ D.至少存在①④⑤
48.[江苏省口岸中学2008-2009学年度高三年级第一学期第四次调研测试]下列反应的离子方程式书写正确的是 [ AC] w.w.w.k.s.5.u. c.o.m
A.用氨水吸收少量SO2气体:2NH3·H2O+SO2=2NH4++SO32-+H2O
B.NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++SO42-+Ba2+十OH-===BaSO4↓+H2O
C.在H2O2中加入酸性KMnO4溶液:2MnO4-+5H2O2+6H+====2Mn2+ +5O2↑+8H2O
D.溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br
+OH-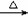 CH2=CH2↑+Br-+H2O
CH2=CH2↑+Br-+H2O
47.[江苏省口岸中学2008-2009学年度高三年级第一学期第四次调研测试]在KIO3、KHSO3的酸性混合溶液中加入少量KI和淀粉,不停地搅拌,有下列反应发生: ① IO3-+ 5I-+ 6H+ → 3I2 + 3H2O ② I2 + 2HSO3-+ H2O → 2I- + 2SO42-+ 4H+
当反应进行到15min时,溶液突然变为蓝色,随之又很快消失。这一反应被称做时钟反应,有人用它来解释生物钟现象。下列有关说法不正确的是[ C]
A.在整个反应过程中,起催化作用的物质是KI
B.上述两个反应中,反应速率较快的是②
C.时钟反应的快慢由反应②决定
D.“溶液突然变为蓝色,随之又很快消失”这一现象与①②的反应速率有关
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com