
2.铁的氢氧化物
|
化学式 |
Fe(OH)2 |
Fe(OH)3 |
|
颜色 状态 |
白色固体 |
红褐色固体 |
|
溶解性 |
难溶于水,易溶于酸 |
难溶于水,易溶于酸 |
|
稳定性 |
不稳定,易被氧化 |
较稳定,受热会分解 |
|
与H+反应 |
Fe(OH)2+2 H+=Fe2++H2O |
Fe(OH)3+3 H+=Fe3++3H2O |
|
转化关系 |
4Fe(OH)2+O2+ 2H2O=
4Fe(OH)3 |
[思考]
(a)配制FeSO4溶液时,需加入稀硫酸和铁粉,其作用分别防止水解、防止Fe2+被氧化。
(b)制取Fe(OH)2时,为什么要用新制的FeSO4溶液?为什么要将吸有NaOH溶液的胶头滴管插入液面以下?防止Fe2+被氧化,形成Fe(OH)3沉淀
(c)若不用此法,还可用什么方法制得Fe(OH)2沉淀?
(d)烧过菜的铁锅未及时洗干净(残液中含NaCl),第二天便出现红棕色锈斑[Fe(OH)3失水的产物],试用有关的电极反应式和化学方程式表示Fe(OH)3的生成过程。
正极:O2+2H2O+4e-=4OH-、负极:Fe-2e-= Fe2+
总反应:2Fe+ O2+2H2O=2Fe(OH)2
Fe(OH)2的氧化:4Fe(OH)2+O2+ 2H2O= 4Fe(OH)3
总结:用可溶性碱分别与Fe2+、Fe3+反应可制得Fe(OH)2和Fe(OH)3。通过哪些方法可避免生成Fe(OH)2中会有Fe(OH)3?
提示:关键在于无孔不入的O2及Fe3+存在。4Fe(OH)2 + O2 + 2H2O == 4Fe(OH)3↓
①驱氧法:如用同煮沸过的NaOH溶液和亚铁盐溶液。
②隔氧法:如用长滴管吸取NaOH溶液后插入亚铁盐溶液面下加入;又如在液面上加某些合适的有机溶剂液封。
③还原法:在FeSO4溶液中加入Fe钉,或者用Fe与稀H2SO4反应新制的FeSO4溶液,生成的H2又可驱赶O2。
铁的氧化物和氢氧化物
1.铁的氧化物
填写下表:
|
化学式 |
FeO |
Fe2O3 |
|
|
俗 称 |
/ |
铁红 |
磁性氧化铁 |
|
颜色状态 |
黑 |
红 |
黑 |
|
溶解性 |
难溶于水 |
||
|
铁的化合价 |
+2 |
+3 |
+2和+3 |
|
与H+反应 |
FeO+2H+=Fe2++H2O |
Fe2O3+6H+=2Fe3++3H2O |
Fe3O4+8H+= Fe2++2Fe3++4H2O |
|
与稀HNO3反应 |
3FeO+10H++ NO3-= 3Fe3++NO↑+5H2O |
Fe2O3+6H+=2Fe3++3H2O |
|
|
与CO或H2反应 |
|
|
|
|
铝热反应 |
|
|
|
[思考]在烧制砖瓦时,用粘土做成的坯经过烘烧后,铁的化合物转化成Fe2O3而制得红色砖瓦。若烘烧后期从窑顶向下慢慢浇水,窑内会产生大量的还原性气体,它们把该红色物质还原为黑色的化合物Fe3O4,同时还有未烧的碳粒而制得了青色砖瓦。
3.重点掌握根据氧化还原的原理进行有关铁及其化合物的相关计算。培养分析、综合、归纳问题的能力和解决问题的能力。
2.掌握铁的氢氧化物的性质和制备。
1.掌握铁的氧化物的性质。
61.{江苏省赣榆高级中学09高三年级十二月 }下列各组离子在指定条件下,一定能大量共存的是[ C ]
A.能使红色石蕊试纸显蓝色的溶液:K+、Fe2+、SO42-、NO3-、Cl-
B.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br-
C.水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl-
D.加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、NO3-
60.{江苏省赣榆高级中学09高三年级十二月 }有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是[ C ]
A.氧化剂与还原剂的物质的量之比为1:8
B.该过程说明Fe( NO3)2溶液不宜加酸酸化
C.若有l mol NO3-发生氧化反应,则转移8mol e-
D.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+
59.{江苏省赣榆高级中学09高三年级十二月 }下列离子反应方程式正确的是 [ D ]
 A.用两个铜电极电解食盐水:2Cl-+2H2O 2HO-+H2↑+Cl2↑
A.用两个铜电极电解食盐水:2Cl-+2H2O 2HO-+H2↑+Cl2↑
B.李永刚用腐蚀法制作印刷线路板:Fe3++Cu====Fe2++Cu2+
C.Ca(HCO3)2溶液中加过量KOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O
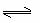 D.AlCl3溶液呈酸性的原因:Al3++3H2O
Al(OH)3+3H+
D.AlCl3溶液呈酸性的原因:Al3++3H2O
Al(OH)3+3H+
58.(江苏海门市2008-2009学年高三第一次教学质量调研)下列有关离子大量共存的说法正确的是[ A ]  w.w.w.k.s.5.u. c.o.m
w.w.w.k.s.5.u. c.o.m
A. H+、Fe2+、SO42-、NO3-因发生氧化还原反应而不能大量共存
B.水电离产生c(H+)=1×10-12mol/L的溶液中,可能有Mg2+、Na+、Cl-、HCO3大量共存
C.澄清透明的无色溶液中,可能有ClO-、MnO4-、Al3+、SO42-大量共存
D.在含大量Fe3+的溶液中,可能有NH4+、Na+、Cl-、SCN-大量共存
57.(江苏海门市2008-2009学年高三第一次教学质量调研)用离子方程式表示的下列过程一定正确的是[ BC]
A.澄清石灰水在空气中变质:OH-+CO2=HCO3-
B.FeSO4溶液在空气中变质:4Fe2++O2+4H+=4Fe3++2H2O
C.AlCl3溶液加入氨水中:Al3++3NH3·H2O = Al(OH)3↓+3NH4+
D.Ca(HCO3)2溶液加入KOH溶液中:Ca2+ + HCO3-+OH-=CaCO3↓+ H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com