
1.(2009年启东模拟)下列说法中不正确的是( )
A.人类历史上使用最早的合金是青铜
B.司母戊鼎是我国目前已发现的最重的青铜器
C.目前世界上使用量最大的合金是铝合金
D.目前世界上用途最广的合金是钢
22.(8分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材
料可以回收再利用,而且对周边环境不构成任何污染.PETG的结构简式为:

(Ⅱ)RCOOR′+R″OH―→RCOOR″+R′OH(R、R′R″表示烃基)
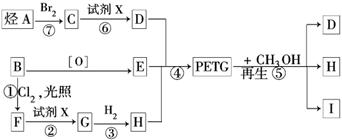 这种材料可采用以下路线合成:
这种材料可采用以下路线合成:
试回答下列问题:
(1)反应②⑥加入的试剂X是________,反应①-⑦中属于取代反应的是________.
(2)写出物质I的结构简式:____________________________________________.
(3)写出反应⑥的化学方程式:___________________________________________
______________________________________________________________________.
(4)合成PETG时各单体的物质的量的比例关系是:
n(D)∶n(E)∶n(H)=________(用m、n表示).
 解析:PETG的单体为:HOCH2CH2OH、
解析:PETG的单体为:HOCH2CH2OH、
 反应③为氢气与苯环的加成反应,故H为
因此D
反应③为氢气与苯环的加成反应,故H为
因此D
为 HOCH2CH2OH,A为乙烯,C为1,2二溴乙烷.⑤为酯交换反应(一种取代反
应).
答案:(1)NaOH溶液 ①②④⑤⑥
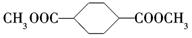
(2)
(3)CH2BrCH2Br+2NaOHHOCH2CH2OH+2NaBr
(或:CH2BrCH2Br+2H2ONaOH△HOCH2CH2OH+2HBr)
(4)m∶(m+n)∶n
21.(11分)下面是新设的一组垃圾箱及说明:
|
厦门市生活垃圾分类 |
||
|
可回收垃圾 |
不可回收垃圾 |
有害垃圾 |
|
1.纸类 2.玻璃 3.金属 4.塑料 5.橡胶 6.纺织品 |
1.厨房垃圾 2.灰土 3.杂草 4.枯枝 5.花卉 |
1.日光灯管 2.电池 3.喷雾罐 4.指甲油瓶 5.药品药瓶 6.涂改液瓶 |
(1)小明在整理房间时,清理出如下物品,它们应分别放入哪个垃圾箱(请填序号):
A.废作业本;B.汽水易拉罐;C.生锈铁钉;D.矿泉水瓶;E.烂苹果;F.涂改液瓶
应放入“可回收垃圾箱”的是________;应放入“不可回收垃圾箱”的是
________;应放入“有害垃圾箱”的是________.
(2)小明用盐酸除去铁钉上的锈(主要成分为氧化铁),以重新使用它,请写出除锈的
化学方程式:____________________________.
(3)废铜有二种回收方法:
方法一:Cu+4HNO3=== Cu(NO3)2+2X↑+2H2O(X是一种大气污染物)
方法二:铜在空气中加热生成氧化铜,氧化铜再与盐酸反应生成氯化铜和水.
①方法一中,X的化学式为:________;方法二的优点是:___________________;
②请写出从氯化铜溶液中提取铜的化学方程式:___________________________;
该反应属于化学反应的基本类型是________.
(4)请从可回收垃圾的类型中,举出一例说说化学的研究成果给社会进步带来的贡
献: _________________________________________________________________
______________________________________________________________________
______________________________________________________________________.
解析:(1)生活垃圾的处理应根据垃圾的成分分类处理,有些可回收再利用,有些不
可回收的要进行处理.
(2)除铁钉上的铁锈可用稀盐酸.
(3)方法一中HNO3被铜还原,由方程式可知应为NO2,会对空气造成污染,方法二
不会产生污染性气体,从CuCl2溶液中提取Cu,可用废铁屑置换,CuCl2+
Fe===FeCl2+Cu.
(4)可结合题给表中的垃圾类型,联想与可回收垃圾有关的化学应用成果回答,这是
一个开放性问题,可从以下几个方面回答:①三大合成材料的制造、应用,②金属
的制造、应用,③玻璃,④纸张的制造、回收等.
答案:(1)A、B、C、D E F
(2)Fe2O3+6HCl===2FeCl3+3H2O
(3)①NO2 没有污染物生成
②Fe+CuCl2===Cu+FeCl2 置换反应
(4)①三大合成材料的制造、应用,防治污染;②金属的制造、开采、应用、合金、
保护、回收;③玻璃等无机材料;④纸张的发展、特种纸的开发、纸的制造和回收
(任选一例)
20.(8分)汽车的发明与使用,是人类智慧的杰出体现,它为人们的生活和生产带来了
极大的方便,同时由此引发的环境污染问题也越来越引起人们的关注,人们开始研
究新的清洁燃料.
(1)新型环保出租车采用LPG+汽油的双燃料系统,其尾气中的有毒气体成分较普
通车型下降80%左右,缓解了汽车尾气排放给城市环境造成的污染问题.下列物质
中不属于上述有害气体的是________.
A.CO2和H2 B.NO2和NO
C.CO和SO2 D.C粒和含铅化合物
(2)为了减少大气污染,许多城市推广使用汽车清洁燃料.目前使用的清洁燃料主要
有两类:一类是压缩天然气,另一类是液化石油气.这两类燃料的主要成分都是
________.
A.碳水化合物 B.碳氢化合物
C.氢气 D.醇类
(3)我国推广使用乙醇汽油,它是在汽油中加入适量乙醇形成的混合燃料.下列叙述
中正确的是________.
A.使用乙醇汽油能减少有害气体的排放,是一种改善环境的清洁能源
B.燃料中的乙醇可以通过粮食发酵或化工合成等方法制得
C.乙醇汽油是一种新型化合物
D.燃烧乙醇汽油可以减少对大气的污染是因为它不含硫元素和氮元素
(4)氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车
备受青睐.我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世
界先进水平,并加快向产业化的目标迈进.氢能具有的优点包括________.
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
解析:(1)汽车尾气主要是NOx、CO、碳粒、含铅化合物和SO2,CO2与H2不属于
有害气体.
(2)两类燃料的主要成分均为碳原子数较小的烃.
(3)乙醇汽油是一种混合物,其含硫、氮量低,故污染少,乙醇可通过淀粉水解或乙
烯与水合成制得.
(4)氢能作为燃料的优点是:来源丰富(水),单位质量的氢燃烧时放热量大,氢气燃
烧的唯一产物是水,不产生污染.其缺点是:现有的制取氢气方法耗能大,制取的
成本太高,另外氢气的熔沸点太低,给储存和运输带来困难.
答案:(1)A (2)B (3)AB (4)A
19.(11分)2008年5月12日,我国汶川发生大地震.全国人民“众志成城,抗震救灾”.
(1)“拯救生命是第一位的”.为搜救埋在废墟下的幸存者,调用了许多搜救犬.搜
救犬能根据人体发出的气味发现幸存者.从微观的角度分析搜救犬能发现幸存者的
原因是________.
A.分子的质量很小 B.不同分子性质不同
C.分子不断运动 D.分子间有间隔
(2)地震中许多原有的水源被破坏.新水源需检测和处理后才能成为饮用水.我国规
定水质必须在感官性指标、化学指标、病理学指标等方面均达标方可成为生活饮用
水.
①感官性指标中有一项要求:不得含有肉眼可见物,水应澄清透明.为达到此要求,
净化水时,可以通过加入絮凝剂凝聚、沉降,然后通过________(填操作名称)而实
现.
②化学指标中含有水源的pH和硬度两项.
测定液体pH的方法是___________________________________________________
_______________________________________________________________________.
日常生活中如何区分硬水与软水?请简述实验步骤与现象:
______________________________________________________________________
______________________________________________________________________.
③病理学指标中对细菌的含量有严格的限制.要杀灭细菌可以向水中加入________
等消毒剂,也可以通过________操作,既杀灭细菌,又能得到几乎纯净的水.
(3)为防止灾后疫情的发生,某医疗小分队用溶质质量分数为0.5%的过氧乙酸溶液
对灾民的居住环境进行消毒.要配制溶质质量分数为0.5%的过氧乙酸溶液300 kg,
需溶质质量分数为15%的过氧乙酸溶液______kg,配制的主要步骤是:__________、
__________、__________.
解析:(2)①新水源中加入絮凝剂凝聚、沉降后应过滤除去沉降物.
②测定液体pH要注意应使用干燥的pH试纸;硬水中含Ca2+、Mg2+ 浓度较大,
可用肥皂水鉴别,若产生大量沉淀,则是硬水.
③常用消毒剂有漂白粉、氯气、臭氧等.
(3)根据配制前后溶质质量不变:0.5%×300 kg=15%x,即得x=10 kg
配制的步骤是计算、量取、稀释.
答案:(1)BC
(2)①过滤 ②把干燥的pH试纸放于玻璃片上,用玻璃棒蘸取待测液体点在pH试纸
上,再与标准比色卡对照 取少量样品于试管中,加肥皂水振荡,若出现较多沉
淀则为硬水,否则为软水 ③漂白粉(或氯气、二氧化氯和臭氧等,一种即可) 蒸馏
(3)10 计算 量取 稀释
18.(5分)食盐不仅可用作调味品,还可以被制成一种家用环保型消毒液.有学生设计
了如图所示的制备装置,用石墨作电极电解饱和氯化钠溶液.通电后,装置中将发
生如下反应:
①2NaCl+2H2O―→2NaOH+H2↑+Cl2↑
②Cl2+2NaOH―→NaCl+NaClO+H2O
 (1)消毒液的主要成分是________(填化学式).
(1)消毒液的主要成分是________(填化学式).
(2)已知氢氧化钠在电极a处产生,氯气在电极b处产生,实验
时,这位学生接错了电源正负极,结果,制备的消毒液中有效成
分的含量很低,原因是__________________________________
_____________________________________________________.
(3)装置上端导管的作用是________________________________________________.
解析:题中的氯气必须在b极上产生,在上升过程中与NaOH溶液充分反应,从而
得到消毒液.
答案:(1)NaClO
(2)不能使Cl2与NaOH充分反应
(3)排空H2(或气体,填写“防止爆炸”或“与大气相通”也正确)
17.(9分)(1)最重要的抗生素是________,即________药.
(2)阿司匹林是由________和________反应制得.阿司匹林可与氢氧化钠反应,其化
学方程式为________________________________.
(3)北京某企业食品有限公司生产的鲜橙多,配料:
①水、②糖、③鲜橙浓缩汁、④柠檬酸、⑤维生素C、⑥食用香料、⑦β胡萝卜素(鲜
橙原汁含量≥20%,净含量:1.5 L).其中属于食品添加剂中的着色剂的是________,
属于调味剂的是________,属于营养强化剂的是________,(以上填序号),由于没
有加入________,建议最好不要贮存太久.
解析:(1)、(2)主要考查重要药物的成分及重要功能,
(3)考查食品添加剂的有关应用.
答案:(1)青霉素 消炎
(2)水杨酸 乙酸酐


(3)⑦ ②④⑥ ⑤⑦ 防腐剂
16.光纤通信是一种现代化的通信手段,它可以提供大容量、高速度、高质量的通信服
务.目前,我国正在大力建设高质量的宽带光纤通信网络,即信息高速公路.光
纤通信所使用的光缆,其主要部件为光导纤维.下列说法正确的是 ( )
①制造光导纤维的主要原料是CaCO3;
②制造光导纤维的主要原料是SiO2;
③光导纤维传递光信号的基本物理原理是光的全反射;
④光导纤维传递光信号的基本物理原理是光的折射
A.①④ B.②③ C.①③ D.②④
解析:光导纤维主要原料的成分是SiO2;光导纤维传递光信号的基本物理原理是光
的全反射.②、③正确.
答案:B
15.不久前我国科学家以玉米淀粉为原料,利用现代生物技术生产出乳酸,再经过聚合
反应得到聚乳酸,制成玉米塑料.其最大的特点是可以降解,并具有优良的机械强
度、抗静电作用等特性,应用前景广阔.下列对玉米塑料的理解正确的是 ( )
①玉米塑料为玉米的综合利用提供了新途径
②玉米塑料的推广使用有利于解决白色污染问题
③玉米塑料推广应用后可以提高玉米的附加值
④玉米塑料与普通塑料不同,它不是一种高分子材料
A.①③④ B.①②③ C.①②④ D.②③④
解析:由题意知,玉米塑料是经过聚合反应制得的,所以它是高分子材料.由于其
可以降解,所以它的推广使用有利于解决白色污染问题.玉米塑料的优良特性,使
得玉米的综合利用更广泛,也就提高了玉米的附加值.
答案:B
14.下列说法正确的是 ( )
A.不锈钢中除了铁元素以外还含有多种其他元素,因此属于复合材料
B.玻璃中含有钠、钙等金属元素,所以不属于无机非金属材料
C.塑料的化学成分是有机物,并且是通过人工合成的,所以是复合材料
D.碳纤维增强复合材料是由基体和增强体复合而成的,属于复合材料
解析:不锈钢是一种铁合金,属于金属材料;玻璃、水泥等属于硅酸盐工业产品,
属于传统无机非金属材料,塑料属于合成高分子材料.
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com