
2.下列物质中含有共价键的离子化合物是(A)
A.Ba(OH)2 B.CaCl2 C.H2O D.H2
1.下列说法中正确的是(AD)
A.含有离子键的化合物必是离子化合物 B.具有共价键的化合物就是共价化合物
C.共价化合物可能含离子键 D.离子化合物中可能含有共价键
2.把氮气的电子式写成∶N∶∶∶N∶
[板书]
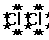
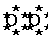

[小结] 由此,我们得出以下结论:即同种或不同种非金属元素化合时,它们的原子之间都能通过共用电子对形成共价键(稀有气体除外)。
以上共价键中的共用电子对都是成键原子双方提供的,共用电子对能不能由成键原子单方面提供呢?我们可通过NH4+的形成及结构进行说明。
已知氨分子和氢离子可结合生成铵根离子。那么,它们是通过什么方式结合的呢?分析氨分子和氢离子的电子式,即可揭开此谜。
[板书]
[讲解]从氨分子的电子式可以看出,氨分子的氮原子周围还有一对未共用电子,而氢离子的周围正好是空的。当氨分子和氢离子相遇时,它们一拍即合,即氢离子和氨分子结合时各原子周围都是稳定结构。这样,在氮原子和氢离子之间又新成了一种新的共价键,氨分子也因氢分子的介入而带正电荷,变成了铵根离子(NH4+),其电子式可表示如下:
[板书]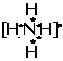
[小结] 像这种共用电子对由成键原子单方提供的共价键,叫做配位键。配位键的性质和共价键相同,只是成键方式不同。
在多数共价键分子中的原子,彼此形成共用电子对后都达到稳定结构,还有一些化合物,它们的分子中并不是所有的原子都达到稳定结构。如BF3分子中的硼离子,外层只有6个电子;PCl5分子中的磷原子共用5对电子后,磷原子外层成了10个电子。同样的情况还有CO、NO2等分子,因此,化学键理论仍在不断发展中。
[板书] 3.共价化合物:只含有共价键的化合物。如:HCl、H2O、CH4、NH3 、CO2
化学键与物质的性质是紧密联系的,共价键都是比较强的化学键,要破坏这些化学键都需要较多的能量,氮分子发生化学反应时要破坏分子内很强的的共价键,由于该共价键很难破坏,因此氮分子化学性质很稳定;再如金刚石完全是由共价键构成的,金刚石熔化时要破坏内部的共价键,因此金刚石的熔点、沸点、硬度等都非常高。
[过渡]在化学上,我们常用一根短线来表示一对共用电子,这样得到的式子又叫结构式。
★ 4、用结构式表示共价键。
以上提到的几种粒子,表示成结构式分别为:
[板书]
H-Cl O=C=O  H-H Cl-Cl O=O
N≡N
H-H Cl-Cl O=O
N≡N 
[过渡]从上节课的学习我们知道,含有离子键的化合物一定是离子化合物。那么,含有共价键的化合物是不是一定是共价化合物呢?下面,我们通过分析氢氧化钠的结构来对此结论进行判断。
[学与问]氢氧化钠是否为离子化合物?判断依据是什么?氢氧化钠是强碱,所以是离子化合物
已知氢氧化钠是由钠离子和氢氧根离子组成的,试用电子式表示氢氧化钠。
[由学生和老师共同完成]
[板书]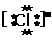

[归纳] 钠离子和氢氧根离子之间是离子键,氧原子和氢原子之间是共价键。
(把离子键和共价键的字样标在氢氧化钠电子式对应位置的下方)
[学与问] 含有共价键的化合物一定是共价化合物。这句话是否正确? 不正确
[讲述] 因此,我们说含有离子键的化合物一定是离子化合物,而含有共价键的化合物不一定是共价化合物。下面,让我们来认识几种化合物的电子式。
[板书] 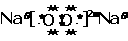


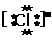
请大家标出其中存在的化学键。
[请一位同学上黑板在相应位置写上离子键、共价键]
[归纳] 通过以上实例及以前的学习,我们可以得出这样的结论:
即在离子化合物中可能有共价键,而在共价化合物中却不可能有离子键。
非金属和非金属原子之间,某些不活泼金属与非金属原子之间,形成的都是共价键。如HCl中的H-Cl键和AlCl3的Al-Cl键。
[归纳·强调]
(1)当一个化合物中只存在离子键时,该化合物是离子化合物
(2)当一个化合中同时存在离子键和共价键时,以离子键为主,该化合物也称为离子化合物
(3)只有当化合物中只存在共价键时,该化合物才称为共价化合物。
(4)在离子化合物中一般既含有金属元素又含有非金属元素;共价化合物一般只含有非金属元素(NH4+例外)
[过渡] 从有关离子键和共价键的讨论中,我们可以看到,原子结合成分子时,原子之间存在着相互作用。这种作用不仅存在于直接相邻的原子之间,而且也存在于分子内非直接相邻的原子之间。前一种相互作用比较强烈,破坏它要消耗比较大的能量,是使原子互相联结成分子的主要因素。我们把这种相邻的原子之间强烈的相互作用叫做化学键。
学了有关化学键的知识,我们就可以用化学键的观点来概略地分析化学反应的过程。如钠与氯气反应生成氯化钠的过程,第一步是金属钠和氯气分子中原子之间的化学键发生断裂(旧键断裂),其中金属钠破坏的是金属键,氯气分子断开的是共价键,它们分别得到钠原子和氯原子;第二步是钠原子和氯原子相互结合,形成钠氯之间的化学键--离子键(新键形成)。分析其他化学反应,也可以得出过程类似的结论。因此,我们可以认为:
[讲解并板书] 一个化学反应的过程,本质上就是旧化学键断裂和新化学键形成的过程。
[讲述] 请大家用化学键的观点来分析,H2分子与Cl2分子作用生成HCl分子的过程。
先是H2分子与Cl2分子中的H-H键、Cl-Cl键被破坏,分别生成氯原子和氢原子,然后氯原子与氢原子又以新的共价键结合成氯化氢分子。
[归纳对比] 离子键和共价键是两种不同类型的化学键,它们之间的区别我们可总结如下:
[投影展示] 离子键与共价键的比较
|
键型 项目 |
离子键 |
共价键 |
|
形成过程 |
得失电子 |
形成共用电子对 |
|
成键粒子 |
阴、阳离子 |
原子 |
|
实质 |
阴、阳离子间的静电作用 |
原子间通过共用电子对所形成的相互作用 |
注:以上内容也可由学生自己填写。
[小结] 本节课我们主要介绍了共价键的实质及化学反应过程的本质。
[课堂练习]
1.把用电子式表示物质写成了用电子式表示其形成过程;
3、把“→”写成“=”。
[板书]



[过渡] 由以上分析可以知道,通过共用电子对可形成化合物的分子,那么,通过共用电子对,能不能形成单质的分子呢?下面,我们以氢分子为例,来讨论这个问题。
[问题] 氢分子是由氢原子构成的,要使每个氢原子都达到两电子稳定结构,氢原子与氢原子之间应怎样合作?
[让一个同学把结果板书于黑板上]
[板书]
H× + ×H -→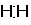
[讲述] 氢原子和氢原子结合成氢分子时,由于两个氢原子得失电子的能力相等,所以其形成的共用电子对位于两原子的正中间,谁也不偏向谁,成键的原子因此而不显电性,这样的共价键叫做非极性共价键,简称非极性键。
[问题] 为什么稀有气体是单原子组成的? 因为稀有气体元素的原子都已达到稳定结构
[探索] 请大家用电子式表示氯气、氧气、氮气。
[易出现的错误是]
2、受离子键的影响,而出现中括号,或写成离子的形式;
[问题] 什么是共价键呢?我们初中所学的共价化合物的知识可以帮助我们找到答案。请大家看以下实验,并描述实验现象。
[电脑演示] 氢气在盛有氯气的集气瓶中燃烧。
氢气在氯气中燃烧,发出苍白色的火焰,集气瓶的瓶口有大量白雾出现。
[讲述] 需要注意的是,该现象不能用“白气”或“白烟”来描述。因为它是氢气与氯气反应生成的氯化氢分子与空气中的水分子结合而成的盐酸小液滴分散在瓶口所形成的现象,应该说是“白雾”。
我们前面学过,氢气与氯气在光照条件下的反应。这是它们在又一条件(即点燃)下反应的反应现象。请大家写出该反应的化学方程式:
[教师板书] H2 + Cl2 = 2HCl
[讲述] 像氯化氢这样以共用电子对形成分子的化合物,叫共价化合物。而原子之间通过共用电子对所形成的相互作用,就叫做共价键。
[板书] 1、原子之间通过共用电子对所形成的相互作用,叫做共价键。
成键微粒:原子。
形成过程:形成共用电子对。
成键实质:原子间通过共用电子对所形成的相互作用。
[电脑演示] 氢原子与氯原子结合成氯化氢分子的过程,我们可用下列动画形象地表示出来。
[问题] 共价键与离子键不同的地方有哪些?
[归纳] 共价键的成键粒子是原子,它们相互之间属不打不相识的关系,而形成离子键的粒子是阴、阳离子,它们之间是周瑜打黄盖--一个愿打,一个愿挨。
从氯原子和氢原子的结构来分析,由于氯和氢都是非金属元素,不仅氯原子易得一个电子形成最外层8个电子的稳定结构,而且氢原子也易获得一个电子,形成最外层两个电子的稳定结构。这两种元素的原子获得电子难易的程度相差不大,所以相遇时都未能把对方的电子夺取过来。这两种元素的原子相互作用的结果是双方各以最外层一个电子组成一个电子对,电子对为两个原子所共用,在两个原子核外的空间运动,从而使双方最外层都达到稳定结构。这种电子对,就是共用电子对。共用电子对受两个核的共同吸引,使两个原子结合在一起。在氯化氢分子里,由于氯原子对于电子对的吸引力比氢原子的稍强一些,所以电子对偏向氯原子一方。因此,氯原子一方略显负电性,氢原子一方略显正电性,但作为分子整体仍呈电中性。象这样共用电子对偏移的共价键叫做极性共价键,简称极性键。
[板书] 2、用电子式表示共价键的形成
以上过程也可以用电子式表示如下:
[板书]
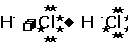
[讲解] 氯化氢分子中,共用电子对仅发生偏移,没有发生电子得失,未形成阴、阳离子,因此,书写共价化合物的电子式不能标电荷。
[练习] 用电子式表示下列共价化合物的形成过程。
(1)CO2 (2)NH3 (3)CH4
[注意] 在用电子式表示共价化合物时,首先需分析所涉及的原子最外层有几个电子;若形成稳定结构,需要几个共用电子对;然后再据分析结果进行书写。
容易出现的问题是:
1、不知怎样确定共用电子对的数目和位置;
22、(本小题15分) 已知椭圆 的长轴长为
的长轴长为 ,离心率为
,离心率为 ,
,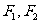 分别为其左右焦点.一动圆过点
分别为其左右焦点.一动圆过点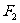 ,且与直线
,且与直线 相切.
相切.
(Ⅰ) (ⅰ)求椭圆 的方程; (ⅱ)求动圆圆心轨迹
的方程; (ⅱ)求动圆圆心轨迹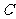 的方程;
的方程;
(Ⅱ) 在曲线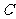 上有四个不同的点
上有四个不同的点 ,满足
,满足 与
与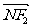 共线,
共线,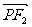 与
与 共线,且
共线,且 ,求四边形
,求四边形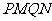 面积的最小值.
面积的最小值.
21、(本小题15分) 已知函数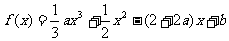 (
( )
)
(Ⅰ) 若 在点
在点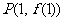 处的切线方程为
处的切线方程为 ,求
,求 的解析式及单调递减区间;
的解析式及单调递减区间;
(Ⅱ) 若 在
在 上存在极值点,求实数
上存在极值点,求实数 的取值范围.
的取值范围.
20、(本小题14分) 已知正项数列 满足
满足 ,
, ,令
,令 .
.
(Ⅰ) 求证:数列 为等比数列;
为等比数列;
(Ⅱ) 记 为数列
为数列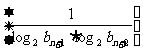 的前
的前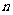 项和,是否存在实数
项和,是否存在实数 ,使得不等式
,使得不等式 对
对 恒成立?若存在,求出实数
恒成立?若存在,求出实数 的取值范围;若不存在,请说明理由.
的取值范围;若不存在,请说明理由.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com