
17.(10分)在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:
C(s)+H2O(g)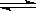 CO(g)+H2(g)
CO(g)+H2(g)
试分析和回答下列问题:
(1)可认定上述可逆反应在一定条件下已达到化学平衡状态的是 (选填序号)。
A 体系的压强不再发生变化 B v正(CO)=v逆(H2O)
C 生成n molCO的同时生成n mol H2 D 1mol H-H键断裂的同时断裂2mol H-O键
(2)若上述化学平衡状态从正反应开始建立,达到平衡后,给平衡体系加压(缩小容积、其它条件不变。下同),则容器内气体的平均相对分子质量面将 (填写不变、变小、变大)。
(3)若上述化学平衡状态从正、逆两反应同时建立[即起始时同时投放C(s)、H2O(g)、CO(g)、H2(g)],达到平衡后,试讨论:
①容积内气体混合物的平均相对分子质量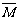 的取值范围是
。
的取值范围是
。
②若给平衡体系加压,请参照起始投放的气体物质的平均相对分子质量(设定为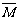 1),分别给出
1),分别给出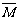 的变化:(填“增大”、“减小”、“不变”)
的变化:(填“增大”、“减小”、“不变”)
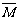 1的取值 1的取值 |
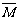 的变化 的变化 |
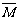 1<12 1<12 |
|
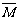 1=12 1=12 |
不变 |
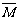 1>12 1>12 |
|
[答案](1)B、D
(2)变大
(3)①2<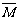 <28
②若
<28
②若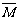 1<12,则
1<12,则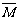 变小;;
变小;;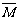 1>12则
1>12则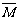 变大。
变大。
16.a mol FeS与b mol FeO投入到VL、c mol/L的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被还原的硝酸可能为( )
①(a+b)×63g ②(a+b)×189g ③(a+b)mol ④Vc-(9a+b)/3mol
A.①④ B.②③
C.①③ D.②④ [答案]D
第Ⅱ卷
(本卷包括5小题,共52分)
15. 某温度下,甲、乙两个烧杯中各盛有100g相同浓度的KCl溶液,现将甲杯蒸发35g水,析出晶体5g;乙烧杯蒸发45g水,析出晶体10g。则原溶液需蒸发多少克水才恰好达到饱和?
A、10g B、15g C、20g D、25g
[答案]D
13.
|
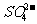 的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为( )
的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为( )
A.5.6 g B.11.2g C.22.4g D.33.6g [答案]C
14下列物质中,既能与NaOH溶液反应,又能与HNO3反应,还能水解的是
①Al2O3 ②H2S ③NaHS ④氨基酸 ⑤对-羟基苯甲酸钠 ⑥乙醇 ⑦纤维素 ⑧蛋白质
A ③④⑤⑥⑦⑧ B ③⑤⑧ C ③⑤⑥⑦⑧ D 全部 [答案]B
12.下图两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间
后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是()
 A.产生气体体积 ①=②
A.产生气体体积 ①=②
B.①中阴极质量增加,②中正极质量减小
C.电极反应式:①中阳极:4OH- - 4e- = 2H2O+O2↑
②中负极:2H++2e-=H2↑
D.溶液的pH变化:① 减小,② 增大
[答案]D
11.由NaHS、MgSO4、NaHSO3组成的混合物中,已知S元素的质量分数w(S)=a%,则O元素的质量分数w(O)为
A 1.75a% B 1-1.75a% C 1.25a% D 无法计算 [答案]B
10. 0.02mol·L-1的HCN溶液与0.02mol·L-1的NaCN溶液等体积混合,已知混合液中[CN-]<[Na+],则下列关系正确的是( )
A.[Na+]>[ ]>[
]>[ ]>[H+] B.[HCN]+[
]>[H+] B.[HCN]+[
 ]=0.04
mol·L-1
C.[Na+]=[
]=0.04
mol·L-1
C.[Na+]=[ ]+[HCN]
D.[
]+[HCN]
D.[ ]>[HCN]
[答案]A
]>[HCN]
[答案]A
9. 用锌、氧化铜、稀硫酸作原料制取铜,有下列两种途径:
(1)
(2)
若用这两种方法制得相同质量的铜时,下列叙述符合实际实验结果的是[ ]
A. 生成的硫酸锌质量相同 C.消耗相同质量的锌
B. 消耗相同质量的硫酸 D.消耗相同质量的氧化铜
[答案]D
8. 将气体A、B置于容积为2L的密闭容器中,发生如下反应:4A(g)+B(g)=2C(g),反应进行到4s末,测得A为0.5mol,B为0.4mol,C为0.2mol,用反应物B浓度的减少来表示该反应的速率可能为( )
A B
B
C D
D [答案]B
[答案]B
7.某有机物分子由 、-CH=CH-两种结构单元组成,且它们自身不能相连,该烃分子中C、H两原子物质的量之比是(
)
、-CH=CH-两种结构单元组成,且它们自身不能相连,该烃分子中C、H两原子物质的量之比是(
)
A 2︰1 B 8︰5 C 3︰2 D 22︰19 [答案]C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com