
26.(3分)由盖斯定律结合下述反应方程式,回答问题:
(1)已知:①C(s)+O2(g)=CO2(g) △H=△H1;
②2CO(g)+O2(g)=2CO2(g) △H=△H2;
③TiO2(s)+2C12(g)=TiCl4(s)+O2(g) △H=△H3;
则TiO2(s)+2C12(g)+2C(s)=TiCl4(s)+2CO(g)的△H 。(列出关于△H1 △H2 △H3 表达式)
25.(6分)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。 (1)放出571.6kJ的热量,表示H2燃烧的热化学方程式为_____ _______。 (2)1.00L 1.00mol·L-1 H2SO4溶液与2.00L 1.00mol·L-1 NaOH溶液完全反应,放出114.6kJ的热量,该反应的热化学方程式为 。
24.按下图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
(1)c(Ag+)(2)c(NO3-)(3)a棒的质量 (4)b棒的质量(5)溶液的pH
A.(1)(3) B.(3)(4) C.(1)(2)(4) D.(1)(2)(5)
23. 可逆反应H2(g)+I2(g) 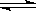 2HI(g)
2HI(g)  H<0 达到平衡后,当改变外界条件如物质浓度、体系压强、温度等而发生下列项目的变化时,能作为平衡一定发生了移动的标志的是
H<0 达到平衡后,当改变外界条件如物质浓度、体系压强、温度等而发生下列项目的变化时,能作为平衡一定发生了移动的标志的是
A.气体的密度变小了 B.反应物和生成物浓度均变为原来的2倍
C.气体的颜色变深了 D.体系的温度发生了变化
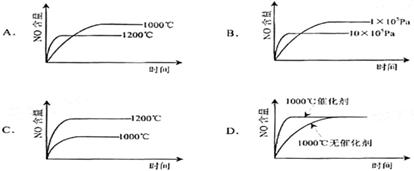
22.已知:4NH3(g)+5O2(g)=4NO(g)+6H2o (g). △H=-1025kJ/mol该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )
21. 下列事实,不能用勒夏特列原理解释的是 ( )
A. 溴水中有下列平衡Br2 + H2O HBr + HBrO,当加入AgNO3溶液后,溶液颜色变浅
B. 对2HI(g) H2(g) + I2(g) ,平衡体系增大压强可使颜色变深
C. 反应CO + NO2 CO2 + NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
D. 合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施(正反应为放热反应)
20.一定条件下,在密闭容器中,能表示反应X(气)+ 2Y(气) 2Z(气)一定达到化学平衡状态的是( )
2Z(气)一定达到化学平衡状态的是( )
① X、Y、Z的物质的量之比为1:2:2 ② X、Y、Z的浓度不再发生变化
③ 容器中的压强不再发生变化 ④ 单位时间内生成n molZ,同时生成2n molY
A.①② B.①④ C.②③ D.③④
19.放热反应2NO(g)+O2 (g)  2NO2 (g)达平衡后,若分别采取下列措施;①增大压强 ②减小NO2的浓度 ③增大O2浓度、④升高温度 ⑤加入催化剂,能使平衡向产物方向移动的是( )
2NO2 (g)达平衡后,若分别采取下列措施;①增大压强 ②减小NO2的浓度 ③增大O2浓度、④升高温度 ⑤加入催化剂,能使平衡向产物方向移动的是( )
A.①②③ B②③④ C③④⑤ D①②⑤
18.某同学为了使反应2HCl + 2Ag 2AgCl +
H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是( )
2AgCl +
H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是( )

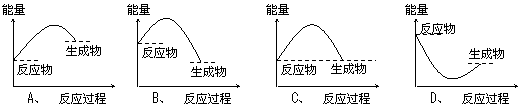
17.下列各图所表示的反应是吸热反应的是( )。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com