
4.张先生看到如下表所示的血液检查结果后,产生以下想法。请指出其中错误的是( )
|
项目 |
测定值 |
单位 |
正常值 |
|
谷丙转氨酶 |
17 |
IU/L |
0-45 |
|
尿素氮 |
14.6 |
mg/dL |
6. 0-23 .0 |
|
血糖 |
223 |
mg/dL |
60-110 |
|
甘油三脂 |
217 |
mg/dL |
50-200 |
|
总胆固醇 |
179 |
mg/dL |
150-220 |
A.谷丙转氨酶较低,可能有肝细胞病变 B.尿素氮含量正常,目前肾脏比较健康
C.血糖过高,肯定会出现尿糖 D.血脂偏高,应少吃油腻食物
3. 下列对甲、乙、丙三个与DNA分子有关的图的说法不正确的是
下列对甲、乙、丙三个与DNA分子有关的图的说法不正确的是
A. 甲图DNA放在含15N培养液中复制2 代,子代含15N的DNA单链占总链的7/8,丙图中
代,子代含15N的DNA单链占总链的7/8,丙图中
①的碱基排列顺序与③不相同
B. 甲图②处的碱基对缺失导致基因突变,限制性内切酶可作用于①部位,解旋酶作用于③部位
C. 丙图中所示的生理过程为转录和翻译,甲图中(A+C)/(T+G)比例不能表现DNA分子的特异性
D. 形成丙图③的过程可发生在拟核中,小麦叶片的维管束鞘细胞中能进行乙图所示生理过程的结构有细胞核、叶绿体、线粒体
2、将菜豆幼苗在含有32P的培养液中培养1小时后,转移到不含32P的培养液中。测定表明,刚移出时植株各部分都含有32P,6小时后32P在下部叶中明显减少,在上部未展开的叶中含量增多,以后数天嫩叶中32P始终维持较高水平。下列有关说法正确的是
A.刚移出时下部叶生长迟缓,P在体内难以再利用
B.移出6小时内苗中P相对含量稳定,不断发生着再利用
C.移出前后P的再利用始终受到调节,P优先分布于生长旺盛部位
D.移出后数天苗中P的相对含量稳定,不会表现出缺乏 症
症
1.2003年诺贝尔生理或医学奖授予了美国Paul Clauterbur 和英国Peter Mansfield,因为他们发明了磁共振技术(MRI),MRI可应用于临床疾病诊断。因为许多疾病会导致组织和器官内水分发生变化,这种变化恰好能在磁共振图象中反映出来。下列有关叙述错误的是
A.构成人体的不同组织和器官含水量是不一样的
B.水在细胞中存在形式及功能是不改变的
C.组织发生病变,会影响组织内的化学变化
D.发生病变的器官,新陈代谢速率往往会发生改变
13.(09海南 )
) 有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。
有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。
 请回答下列问题:
请回答下列问题:
 (1)反应①的化学方程式为
(1)反应①的化学方程式为
 (2)反应②的离子方程式为
(2)反应②的离子方程式为
 (3)写出另外一种实验室制取H的化学方程式
(3)写出另外一种实验室制取H的化学方程式
★ (4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10-2mo1/L ,则生成沉淀所需Pb(NO3)2溶液的最小浓度为
。
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10-2mo1/L ,则生成沉淀所需Pb(NO3)2溶液的最小浓度为
。
★14.海水中溴常以NaBr形式存在,经分析海水中含溴0.07%,则海水中含NaBr的质量百分含量为 _________。从海水中提取溴的方法之一是:
(1)通入Cl2至浓缩的溴化物溶液,然后用空气把生成的溴吹出。
(2)用Na2CO3溶液吸收溴(其中有 的溴的物质的量转化为Br-),同时放出CO2。
的溴的物质的量转化为Br-),同时放出CO2。
(3)向所得含溴化合物溶液中加稀H2SO4,溴又重新析出。
(4)得到的溴中可能夹杂少量的Cl2,再加入FeBr2除去
第一步反应的离子方程式 ____________________________________
第二步反应的化学方程式 ______________________________________
第三步反应中氧化剂的化学式是 ___________________
12.含I2及I-的废液中回收碘的步骤如下图所示:
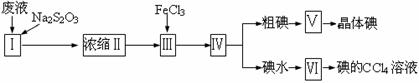
(1)浓缩前加入Na2S2O3使I2还原为I-,其目的是 。
(2)第Ⅲ步操作中发生反应的化学方程式为 。
(3)第Ⅴ步实验操作的名称是 ,第Ⅵ步操作的名称是 。
(4)碘水中加入CCl4后,充分混合后静置分层,CCl4在下层,这是因为 ;如果在太空实验室中混合这两种液体,CCl4就未必在下层,因为 。
 (5)碘的CCl4溶液通过
方法可使碘和CCl4分离。
(5)碘的CCl4溶液通过
方法可使碘和CCl4分离。
11.2003年10月,国家质检总局对全国部分城市食用盐作了抽查,合格率仅为66.7%,不合格主要原因是碘含量不足。
(1)食盐中碘主要存在于______中 A.I2 B.KIO3 C.KI D.NaIO3
(2)国家规定每千克食盐中含有该含碘物质为40-50mg为合格。为检验某碘盐是否合格,某同学称取食盐215g,溶解、酸化、加淀粉及足量的另一种含碘物质,充分反应后溶液呈蓝色,再加0.015mol·L-1的硫代硫酸钠溶液滴定,用去18.mL时,蓝色刚好褪去。有关反应如下: IO3-+5I-+6H+=3I2+3H2O I2+2S2O32-=2I-+S4O62-
请回答:①在第一个反应中,被氧化的碘与被还原的碘的质量比为________________。
②通过计算判断碘盐是否合格?
10.有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3价、+5价两种价态,这种化合物的化学式和应当具有的性质是
A.I2O4 强氧化性 B.I3O5 强还原性 C.I4O9 强氧化性 D.I4O7 强还原性
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
9.甲、乙、丙三种溶液各含有一种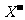 (
(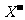 为
为 、
、 或
或 )离子,向甲中加淀粉溶液和新制的氯水变为橙色,将此溶液倒入丙,颜色无明显变化。则甲、乙、丙依次含
)离子,向甲中加淀粉溶液和新制的氯水变为橙色,将此溶液倒入丙,颜色无明显变化。则甲、乙、丙依次含
A.
 、
、 、
、 B.
B. 、
、 、
、 C.
C. 、
、 、
、 D.
D. 、
、 、
、
8.实验室保存下列试剂,有错误的是
A.浓盐酸易挥发,盛在无色密封的玻璃瓶中
B.碘易升华,保存在盛有水的棕色试剂瓶中
C.液溴易挥发,盛放在用水密封的用玻璃塞塞紧的棕色试剂瓶中
D.溴化银保存在棕色瓶中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com