
22Ўў(1)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎ  ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ
(2)1______________________________ЎЎЎЎЎЎЎЎ _________ЎЈ
2____________ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ _____________ЎЎЎЎЎЎ ______ЎЎЎЎ ____ЎЈ
ЎЎЎЎЎЎЎЎ ўЫ____________ЎЈ
ЎЎ (3)ЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЈ
ЎЎ (4)
21Ўў(1)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ»ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ» ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
(2)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
(3)__________________ЎЎЎЎЎЎЎЎЎЎЎЎ __ЎЎЎЎЎЎЎЎ _________ЎЈ
(4)____________Ј» _____________ЎЎЎЎЎЎ ______ЎЎЎЎ ____ЎЈ
20Ўў(1)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ»(2)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ»
ЎЎ (3)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЈ
19Ўў(1)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ Ј»(2)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ»
ЎЎ (3)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЈ»(4)ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЈ
23ЎўПт300 mL KOHИЬТәЦР»әВэНЁИлТ»¶ЁБҝөДCO2ЖшМеЈ¬ід·Ц·ҙУҰәуЈ¬ФЪјхС№өНОВПВХф·ўИЬТәЈ¬өГөҪ°ЧЙ«№ММеЎЈЗл»ШҙрПВБРОКМвЈә
ЎЎ (1)УЙУЪCO2НЁИлБҝІ»Н¬Ј¬ЛщөГөҪөД°ЧЙ«№ММеөДЧйіЙТІІ»Н¬Ј¬КФНЖ¶ПУРјёЦЦҝЙДЬөДЧйіЙЈ¬Іў·ЦұрБРіцЎЈ
(2)ИфНЁИлCO2ЖшМеОӘ2.24L (ұкЧјЧҙҝцПВ)Ј¬өГөҪ11.9 g өД°ЧЙ«№ММеЎЈЗлНЁ№эјЖЛгИ·¶ЁҙЛ°ЧЙ«№ММеКЗУЙДДР©ОпЦКЧйіЙөДЈ¬ЖдЦКБҝёчОӘ¶аЙЩ?ЛщУГөДKOHИЬТәөДОпЦКөДБҝЕЁ¶ИОӘ¶аЙЩ?
ёЯИэ»ҜС§өЪТ»ҙОФВҝјКФҫн
22ЎўДі»ҜС§ҝОНвРЛИӨРЎЧйОӘМҪҫҝНӯёъЕЁБтЛбөД·ҙУҰЗйҝцЈ¬УГПВНјЛщКҫЧ°ЦГПИҪшРРБЛУР№ШКөСйЈә
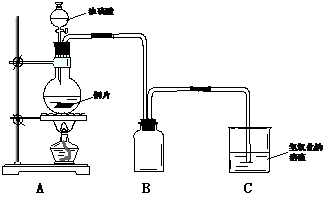
(1)BКЗУГАҙКХјҜКөСйЦРІъЙъөДЖшМеөДЧ°ЦГЈ¬ө«ОҙҪ«өј№Ь»ӯИ«Ј¬ЗлЦұҪУФЪФӯНјЙП°Сөј№ЬІ№ідНкХыЎЈ
(2)КөСйЦРЛыГЗИЎ6.4gНӯЖ¬әН12mL 18molЎӨL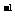 ЕЁБтЛб·ЕФЪФІөЧЙХЖҝЦР№ІИИЈ¬ЦұөҪ·ҙУҰНкұПЈ¬Чоәу·ўПЦЙХЖҝЦР»№УРНӯЖ¬КЈУаЈ¬ёГРЎЧйС§ЙъёщҫЭЛщС§өД»ҜС§ЦӘК¶ИПОӘ»№УРТ»¶ЁБҝөДБтЛбКЈУаЎЈМоРҙПВБРҝХёсЈә
ЕЁБтЛб·ЕФЪФІөЧЙХЖҝЦР№ІИИЈ¬ЦұөҪ·ҙУҰНкұПЈ¬Чоәу·ўПЦЙХЖҝЦР»№УРНӯЖ¬КЈУаЈ¬ёГРЎЧйС§ЙъёщҫЭЛщС§өД»ҜС§ЦӘК¶ИПОӘ»№УРТ»¶ЁБҝөДБтЛбКЈУаЎЈМоРҙПВБРҝХёсЈә
ўЩЗлРҙіцНӯёъЕЁБтЛб·ҙУҰөД»ҜС§·ҪіМКҪЈә________________________________________________________ЎЈ
ўЪОӘКІГҙУРТ»¶ЁБҝөДУаЛбө«ОҙДЬК№НӯЖ¬НкИ«ИЬҪвЈ¬ДгИПОӘФӯТтКЗЈә_____________________
______________________________________________________________________________________________________________________________________ЎЈ
ўЫПВБРТ©Ж·ЦРДЬ№»УГАҙЦӨГч·ҙУҰҪбКшәуөДЙХЖҝЦРИ·УРУаЛбөДКЗ____________ (МоРҙЧЦДёұаәЕЈ¬УРјёёцРҙјёёцЈ¬¶аРҙ»тРҙҙн0·Ц)ЎЈ
AЈ®Мъ·ЫЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ BЈ®BaCl2ИЬТәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ CЈ®Тш·ЫЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎ DЈ®Na2CO3ИЬТә
ЎЎ(3)Из№ыІвөГұкЧјЧҙҝцПВІъЙъSO2өДМе»эОӘ1.792LЈ¬Фтұ»»№ФӯөДБтЛбөДОпЦКөДБҝОӘЎЎЎЎ molЎЈ
(4)УРН¬С§ИПОӘёГКөСйЧ°ЦГҙжФЪІ»ЧгЦ®ҙҰЈ¬ИзәОёДҪшЈәЎЎЎЎЎЎЎЎ ЎЎЎЈ(»ӯіцёДҪшЧ°ЦГ)
21Ўў(12·Ц) AЎўBЎўCЎўDЛДЦЦ¶МЦЬЖЪФӘЛШөДФӯЧУРтКэТАҙОФцҙуЎЈAЎўDН¬ЧеЈ¬BЎўCН¬ЦЬЖЪЈ¬AУлBЧйіЙөД»ҜәПОпјЧОӘЖшМ¬Ј¬ЖдЦРAЎўBФӯЧУёцКэұИОӘ4ЎГ1ЎЈУЙAУлCЧйіЙөДБҪЦЦ»ҜәПОпТТУлұыҫщОӘТәМ¬Ј¬ТТЦРAЎўCФӯЧУёцКэұИОӘ1ЎГ1Ј¬ұыЦРОӘ2ЎГ1ЎЈУЙDУлCЧйіЙөДБҪЦЦ»ҜәПОп¶ЎәНОм¶јОӘ№ММ¬Ј¬¶ЎЦРDЎўCФӯЧУКэЦ®ұИОӘ1ЎГ1Ј¬ОмЦРОӘ2ЎГ1ЎЈ
(1)јЧ·ЦЧУ№№РН_______________ Ј»ТТөДөзЧУКҪ_______________ Ј»
¶ЎЦРҙжФЪөД»ҜС§јьАаРН_______________
(2)РҙіцBФӘЛШЧоёЯјЫСх»ҜОпУл¶Ў·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪЈәЎЎЎЎЎЎЎЎЎЎ _____ЎЈ
(3)AЎўBЎўCЎўDЛДЦЦФӘЛШЦРДіИэЦЦЧйіЙөД»ҜәПОпөДЛ®ИЬТәДЬУлҪрКфВБ·ҙУҰ·ЕіцЗвЖшЈ¬Рҙіц·ҙУҰөД»ҜС§·ҪіМКҪЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
(4)УЙAЎўBЎўCЎўDЛДЦЦФӘЛШРОіЙөД»ҜәПОпЦРЈ¬УРТ»Р©»ҜәПОпөДЛ®ИЬТәіКјоРФЎЈҙУТСС§№эөД»ҜәПОпЦРКФРҙіцТ»ЦЦЈ¬ІўУГАлЧУ·ҪіМКҪұнКҫЖдіКјоРФөДФӯТтЎЈ
ЎЎ ___________Ј»_____________________________ЎЈ
20Ўў(6)Т»¶ЁБҝөДЗвЖшФЪВИЖшЦРИјЙХЈ¬ЛщөГ»мәПОпУГ100mL 3.00mol/LөДNaOHИЬТә(ГЬ¶ИОӘ1.12g/mL)ЗЎәГНкИ«ОьКХЈ¬ІвөГИЬТәЦРә¬УРNaClOөДОпЦКөДБҝОӘ0.0500molЎЈ
(1)ФӯNaOHИЬТәөДЦКБҝ·ЦКэОӘЎЎЎЎЎЎЎЎЎЎЎЎ
(2)ЛщөГИЬТәЦРClЈӯөДОпЦКөДБҝОӘЎЎЎЎЎЎЎЎ molөҘО»
(3)ЛщУГВИЖшәНІОјУ·ҙУҰөДЗвЖшөДОпЦКөДБҝЦ®ұИn(Cl2)Јәn(H2)ЈҪЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
19Ўў (8·Ц) №йДЙХыАнКЗҝЖѧѧϰөДЦШТӘ·Ҫ·ЁЦ®Т»ЎЈФЪС§П°БЛСхЧеФӘЛШөДёчЦЦРФЦКәуЈ¬ҝЙ№йДЙХыАніцИзПВұнЛщКҫөДұнёс(Іҝ·Ц)ЎЈ
|
РФЦК/ФӘЛШ |
8O |
16S |
34Se |
52Te |
|
өҘЦКИЫөг(Ўж) |
ЁC 218.4 |
113 |
ЎЎ |
452 |
|
өҘЦК·Рөг(Ўж) |
ЁC 183 |
444.6 |
685 |
1390 |
|
ЦчТӘ»ҜәПјЫ |
ЁC 2 |
ЁC 2Ўў+ 4Ўў+ 6 |
ЁC 2Ўў+ 4Ўў+ 6 |
ЎЎ |
|
ФӯЧУ°лҫ¶ |
ЦрҪҘФцҙу |
|||
|
өҘЦКУлH2·ҙУҰЗйҝц |
өгИјКұТЧ»ҜәП |
јУИИ»ҜәП |
јУИИДС»ҜәП |
І»ДЬЦұҪУ»ҜәП |
ЗлёщҫЭЙПұн»ШҙрПВБРОКМвЈә





















(1)ОшөДИЫөг·¶О§ҝЙДЬКЗ______________________Ј»
(2)нЪөД»ҜәПјЫҝЙДЬУР__________________Ј»
(3)БтЎўОшЎўнЪөДЗв»ҜОпөДОИ¶ЁРФУЙЗҝЦБИхөДЛіРтКЗ__________________(Мо»ҜС§КҪ)ЎЈ
(4)ЗвОшЛбУРҪПЗҝөД_______(МоЎ°Сх»ҜРФЎұ»тЎ°»№ФӯРФЎұ)Ј¬ТтҙЛ·ЕФЪҝХЖшЦРіӨЖЪұЈҙжТЧұдЦКЎЈ
18ЎўФЪјЧЎўТТЎўұыЎў¶ЎЛДёцЙХұӯАп·Цұр·ЕИл0.1molөДДЖЈ¬Сх»ҜДЖЈ¬№эСх»ҜДЖәНЗвСх»ҜДЖЈ¬И»әуёчјУИл100mLЛ®Ј¬К№№ММеНкИ«ИЬҪвЈ¬ФтјЧЎўТТЎўұыЎў¶ЎөДИЬТәЦРИЬЦКөДЦКБҝ·ЦКэҙуРЎөДЛіРтОӘ
AЈ®јЧЈҫТТЈҫұыЈҫ¶ЎЎЎЎЎЎЎЎЎЎЎЎЎ BЈ®¶ЎЈјјЧЈјТТЈҪұы
CЈ®јЧЈҪ¶ЎЈјТТЈҪұыЎЎЎЎЎЎЎЎЎЎЎЎ DЈ®¶ЎЈјјЧЈјТТЈјұы
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com