
2.(教育部考试中心1996年化学试测题) 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5 77.1℃ C2H5OC2H5(乙醚) 34.5℃ C2H5OH 78.3℃ CH3COOH 118℃ 实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸、边加热蒸馏。得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
⑴反应中加入乙醇是过量的,其目的是:
。
⑵边滴加醋酸、边加热蒸馏的目的是:
。
将粗产品再经下列步骤精制:
⑶为除去其中的醋酸,可向产品中加入 (填字母)。
A 无水乙醇 B 碳酸钠粉末 C 无水醋酸钠
⑷再向其中加入饱和氯化钙溶液,振荡。其目的是:
。
⑸然后再向其中加入无水硫酸钠,振荡。其目的是:
。
最后,将经过上述处理后的液体放入另一干燥的蒸馏瓶内,再蒸馏。弃去低沸点馏分,收集76~78℃沸程之间的馏分即得。
(本题考查了乙酸乙酯的制取、分离和提纯,要熟练掌握已学知识并结合题给信息加以分析,答题时要认真组织语言。)
4.油脂属于酯类,是高级脂肪酸与甘油形成的酯。
油脂一般是混合物,单甘油酯不一定是纯净物而混甘油酯不一定是混合物。油脂难溶与水,密度比水小,易溶与乙醇等有机溶剂。能发生水解反应,酸催化条件下用于制高级脂肪酸和甘油,碱催化条件下称为皂化反应,用于制肥皂。
典型题点击
 1.(1997年全国高考题)已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟基(-OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是
( )
1.(1997年全国高考题)已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟基(-OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是
( )



(本题考查了一些物质中羟基的性质,掌握物质的类别和酸性的强弱是解题的关键。)
3.酯--酸(含氧酸)与醇发生酯化反应而生成的有机物,一般通式RCOOR′(R′≠H),当R与R′均为烷基时称为饱和一元酯,有通式CnH2nO2(n≥2),与饱和一元羧酸互为类别异构。酯难溶与水,密度比水小,易溶与乙醇等有机溶剂,低级酯具有芳香气味。酯能发生水解反应,用稀硫酸作催化剂(须水浴加热),水解程度小为可逆反应,生成对应的酸和醇。用碱作催化剂,因碱与生成的酸中和,水解程度增大,反应趋于完全。
2.羧酸--分子里由烃基与羧基相连构成的化合物,一元羧酸有通式R-COOH,饱和一元羧酸有通式CnH2nO2(n≥1)。大多羧酸与乙酸一样具有酸性,能发生酯化反应形成酯。甲酸分子中存在醛基,有还原性。高级脂肪酸(硬脂酸、油酸)不溶与水。物质的量浓度相等时,酸性由大到小顺序如下:HOOC-COOH、HCOOH、C6H5COOH、CH3COOH、H2CO3。
117.9℃,易溶于水和乙醇,无水乙酸又称冰醋酸。(2)
|
 化学性质,乙酸的官能团是
,简写为-COOH,可以在氧氢键或碳氧键发生断列。①酸性,在水溶液中乙酸能发生电离CH3COOH
CH3COO-+H+,即在氧氢键处断列,具有酸的通性,酸性比碳酸的酸性强。②酯化反应ⅰ条件,加热并用浓H2SO4作催化剂;ⅱ特点,可逆反应,逆反应是酯的水解,浓H2SO4兼起吸水剂的作用,去掉生成物中的水,使反应正向移动,生成更多的酯;ⅲ机理,一般是酸中的羟基(即在碳氧键处发生断列)与醇中羟基的氢结合成水;ⅳ实验装置及操作。
化学性质,乙酸的官能团是
,简写为-COOH,可以在氧氢键或碳氧键发生断列。①酸性,在水溶液中乙酸能发生电离CH3COOH
CH3COO-+H+,即在氧氢键处断列,具有酸的通性,酸性比碳酸的酸性强。②酯化反应ⅰ条件,加热并用浓H2SO4作催化剂;ⅱ特点,可逆反应,逆反应是酯的水解,浓H2SO4兼起吸水剂的作用,去掉生成物中的水,使反应正向移动,生成更多的酯;ⅲ机理,一般是酸中的羟基(即在碳氧键处发生断列)与醇中羟基的氢结合成水;ⅳ实验装置及操作。
1.乙酸(CH3COOH)(1)物理性质:俗名醋酸,无色具有强烈刺激性气味的液体,熔点16.6℃,沸点
10.(1)190;(2)分子中所含碳碳双键较少;(3)15.9L;(4)相对分子质量大小。
讲析:(1) ;
;
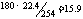 (3)
。
(3)
。
9.
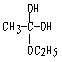 ⑴A、B;C、F;D、E。⑵都有 标记。因为反应中间体在消去一分子H2O时,有两种可能,而乙氧基(OC2H5)是保留的。
⑴A、B;C、F;D、E。⑵都有 标记。因为反应中间体在消去一分子H2O时,有两种可能,而乙氧基(OC2H5)是保留的。
⑶ (或答中间体),因为这个碳原子边有4
 个原子团。(4)CH3COOC2H5+HCl;
个原子团。(4)CH3COOC2H5+HCl;

8.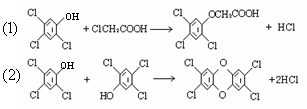
讲析:由2,4,5 三氯苯酚和氯乙酸反应可制造除草剂2,4,5 三氯苯氧乙酸得出结论:该反应是取代反应,羟基中的氢与氯乙酸中的氯结合成氯化氢,其余部分结合成2,4,5 三氯苯氧乙酸。反应(2)同样根据上述结论来写。
7.(1)b 、c;


(2) 或
|

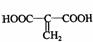 或
或
+Br2→
 (4)
(4)
(其他合理答案也可以!)
讲析:由题给信息①②③可得出该物质含有一个羟基、两个羧基,再根据其化学式写出它的结构。注意:(4)中A的同类别的一个同分异构体也必须有一个羟基、两个羧基。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com