
1.(严州中学2008第二次模拟)硫酸亚铁铵的化学式为(NH4)2Fe(SO4)2·6H2O,商品名为摩尔盐。硫酸亚铁可与硫酸铵生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成摩尔盐后就比较稳定了。
三种盐的溶解度(单位为g/100g水)如下表:
|
温度/℃ |
10 |
20 |
30 |
40 |
50 |
70 |
|
(NH4)2SO4 |
73.0 |
75.4 |
78.0 |
81.0 |
84.5 |
91.9 |
|
FeSO4·7H2O |
40.0 |
48.0 |
60.0 |
73.3 |
- |
- |
|
(NH4)2Fe(SO4)2·6H2O |
18.1 |
21.2 |
24.5 |
27.9 |
31.3 |
38.5 |
实验室欲制备硫酸亚铁铵晶体,设计了如下方案。
(1)完成实验步骤中的填空:
①称取4g铁屑,放入小烧杯,加入15mL10%Na2CO3溶液,小火加热10min以除去_________,倒掉溶液,用蒸馏水把铁冲洗干净,干燥,备用。
②将处理好的铁屑放入小烧杯,加入15 mL 3 mol/L H2SO4溶液,水浴加热至不再有气体生成为止,趁热过滤去剩余铁屑,并用少量热水洗涤烧杯及滤纸,并将滤液和洗涤液一起转移到蒸发皿中,则蒸发皿中溶液的溶质为__________(填名称,不考虑水解), 其物质的量约为________mol。
③加入________g硫酸铵到蒸发皿中,缓缓加热、浓缩至表面出现结晶膜为止、冷却,得硫酸亚铁铵晶体。
(2)回答下列问题:
①硫酸亚铁溶液在空气中易被氧化变质,操作时应注意:步骤②中 ; 步骤③中 。
②加热、浓缩溶液时,不浓缩至干的理由是 。
③硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,试根据有关信息分析其原因 。
④称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液。用未知浓度的KMnO4酸性溶液进行滴定。
A.滴定时,将KMnO4酸性溶液装在_______(填“酸式”或“碱式”)滴定管。
B.已知MnO4-被还原为Mn2+,试写出该滴定过程中的离子方程式:
_______________________________,
C.判断该反应到达滴定终点的现象为 。
D.假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为_______mol/L。
13.据报导,目前我国结核病的发病率有抬头的趋势。抑制结核杆菌的药物除雷米封外,PAS-Na(对氨基水杨酸钠)也是其中一种。它与雷米封可同时服用,可以产生协同作用。已知:
① (苯胺、弱碱性、易氧化)
(苯胺、弱碱性、易氧化)
②
下面是PAS-Na的一种合成路线(部分反应的条件未注明):

按要求回答问题:
⑴写出下列反应的化学方程式并配平
A→B:__________________________________________________________________;
B→C7H6BrNO2:__________________________________________________________;
⑵写出下列物质的结构简式:C:____________________D:______________________;
⑶指出反应类型:I_________________,II_________________;
⑷指出所加试剂名称:X______________________,Y____________________。
12.有机物A与乙酸无论以何种比例混合,只要总质量一定,完全燃烧后产生的水的质量也一定,试回答:
⑴若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为_____________。
⑵若A由四种元素形成的两种官能团组成,相对分子质量与乙酸相等,且分子中氢原子都不与碳原子相连,则A的结构简式为_____________。
⑶若A分子中C、H元素质量分数之和为86.67%,其余为O,且A的相对分子质量小于200,则A的分子式为___________。如果A分子每个碳原子都达到饱和,且能与金属钠反应产生氢气,则A的结构简式为________________________。
11.我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:

这种材料可采用如下图所示的合成路线

(1) 
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1)⑦的反应类型是 。
(2)写出I的结构简式: 。
(3)合成时应控制的单体的物质的量:n(H):n(E): n (D)= (用m、n表示)。
(4)写出反应②的化学方程式:
(5)写出同时符合下列两项要求的E的所有同分异构体的结构简式。
①该同分异构体的苯环上相邻的三个碳原子上都连有取代基。
②该同分异构体在一定条件下能发生银镜反应和水解反应,遇到FeCl3溶液显紫色。
、 、 。

10.1834年德国科学家米希尔里希通过蒸馏苯甲酸和石灰的混合物得到苯。苯是重要的化工原料。结合所学知识完成下列各题。
(1)下列实验结论能够证明凯库勒式与苯的真实结构不相符的是 。
A.在一定条件下1mol苯能与3mol氢气发生加成反应
B.苯不能使酸性KMnO4溶液褪色
C.苯的邻二溴代物没有同分异构体
D.经测定苯为六边形结构,且所有碳碳键完全相同
(2)吉林石化厂苯车间爆炸导致硝基苯泄漏,使松花江遭到严重污染。试写出实验室制取硝基苯的化学反应方程式 。
(3)苯酚也是重要的化工原料,某实验小组以苯为原料制取苯酚,进而合成高分子化合物。请在下列合成反应流程图中填写A、B、C、D、E的结构简式及①、②、③的反应条件。


9.今有A、B、C三种有机物相对分子质量相同。A、B互为同分异构体,A是一种芳香烃,且分子中所有的原子在同一个平面上。B是一种具有立体构型的分子,所有的碳原子地位完全等同,分子中不存在不饱和键,C是烃的含氧衍生物。各取1mol A、C完全燃烧,生成的CO2分别为8mol和4mol。A和苯不论以何种比例相混合,只要混合物总质量一定,完全燃烧时生成的水的量也一定。
⑴A的结构简式为_________________,C的分子式为_______________,
B的分子中所有碳原子构成______________型。
⑵C分子有多种同分异构体,其中有一种含有羧基,不含甲基的物质甲。该分子能发生多种反应,如能生成五元环状物质乙,也能生成最简式与乙相同的两种聚合物丙和丁。
请分别写出这些物质的结构简式。
|
甲 |
乙 (五元环状化合物) |
丙 (经缩聚反应生成) |
丁 (经加聚反应生成) |
|
|
|
|
|
8. A、B都是芳香族化合物,相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。1 molA与1mol某一元羧酸发生酯化反应生成B,B能在一定条件下发生银镜反应而A不能;A中氧元素的质量分数为31.6%,B的溶液有酸性,但不能和FeCl3溶液发生显色反应。请根据上述信息,完成下列填空:
⑴A的分子式是 ,你确定A分子中氧原子数目的理由是
⑵若1molA只能与1molNaOH发生反应,且A苯环上一取代产物只有两种,则A的结构简式为 。
⑶B的同分异构体甚多。其中不属于酚类且1mol能与3molNaOH反应的同分异构体的结构筒式为 (任写一种)。
7. 在相邻的碳原子上连两个或多个-OH或-C=O基团的化合物,用高碘酸(HIO4)处理时,发生碳碳键断裂的氧化反应,由生成物和消耗HIO4的量可推知有机物的结构,例如:(副产物已略去)
 + HIO4 → R1CHO + R2CHO
+ HIO4 → R1CHO + R2CHO
 + HIO4 → R1COOH + R2COOH
+ HIO4 → R1COOH + R2COOH

 + HIO4 →
+ R3CHO
+ HIO4 →
+ R3CHO
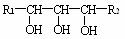 + 2HIO4 → R1CHO
+ HCOOH + R2CHO
+ 2HIO4 → R1CHO
+ HCOOH + R2CHO
(1)当1molCH2OH(CHOH)3CHO用HIO4处理时,将消耗HIO4 mol。
(2)已知:A+3HIO4→2HCOOH+2HCHO,则A的结构简式为 。
(3)若 B+HIO4→HOOC(CH2)4CHO,则B的结构简式为 。
6.已知苯酚能跟碳酸钠溶液反应而溶解于碳酸钠溶液中。在下图所示的转化关系中,括号内编号①-④表示转化所需化学试剂:

(1)用化学式填空:
①是 、②是 、
③是 、④是 、
(2)A的结构简式是 。
5.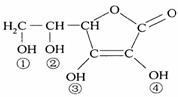 维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如右图。下列有关说法中正确的是( )
维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如右图。下列有关说法中正确的是( )
A.维生素C的分子式为C6H10O6
B.维生素C由于含有酯基而难溶于水
C.维生素C由于含有C=O键而能发生银镜反应
D.维生素C的酸性可能是③、④两个羟基引起的
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com