
35.(18分)航天宇航员在月球表面完成了如下实验:如图所示,在月球表面固定一竖直光滑圆形轨道,在轨道内的最低点,放一可视为质点的小球,当给小球水平初速度v0时,小球刚好能在竖直面内做完整的圆周运动。已知引力常量为G,圆形轨道半径为r,月球的半径为R。求:
(1)月球表面的重力加速度g;
 (2)月球的质量M;
(2)月球的质量M;
(3)若在月球表面上发射一颗环月卫星,其最小发射速度。
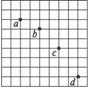
34.(18分)(1)如图所示,在“研究平抛物体运动”的实验中,有一张印有小方格的纸记录轨迹,小方格的边长L=2.5 cm。若小球在平抛运动过程中的几个位置如图中的a、b、c、d所示,则小球平抛的初速度的计算式为v0=__________(用L、g表示),其值为__________ m/s;小球在b点的速度大小为__________ m/s。(取g=10 m/s2,计算结果全部取2位有效数字),
(2)一物理兴趣小组利用学校实验室的数字实验系统探究物体作圆周运动时向心力与角速度、半径的关系。
|
实验序号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
F/N |
2.42 |
1.90 |
1.43 |
0.97 |
0.76 |
0.50 |
0.23 |
0.06 |
|
ω/rad·s-1 |
28.8 |
25.7 |
22.0 |
18.0 |
15.9 |
13.0 |
8.5 |
4.3 |
①首先,他们让一砝码做半径r为0.08m的圆周运动,数字实验系统通过测量和计算得到若干组向心力F和对应的角速度ω,如下表。请你根据表中的数据在图甲上绘出F-ω的关系图像。
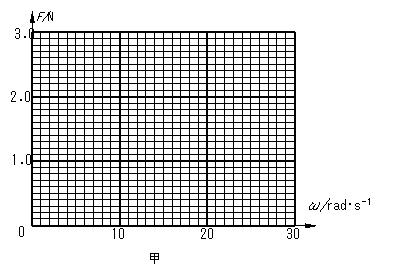 ②通过对图像的观察,兴趣小组的同学猜测F与ω2成正比。你认为,可以通过进一步转换,做出____________关系图像来确定他们的猜测是否正确。
②通过对图像的观察,兴趣小组的同学猜测F与ω2成正比。你认为,可以通过进一步转换,做出____________关系图像来确定他们的猜测是否正确。
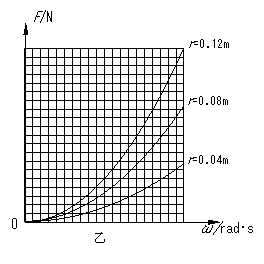
③在证实了F∝ω2之后,他们将砝码做圆周运动的半径r再分别调整为0.04m、0.12m,又得到了两条F-ω图像,他们将三次实验得到的图像放在一个坐标系中,如图乙所示。通过对三条图像的比较、分析、讨论,他们得出F∝ r的结论,你认为他们的依据是______________________________________________________。
④通过上述实验,他们得出:做圆周运动的物体受到的向心力F与角速度ω、半径r的数学关系式是F=kω2r,其中比例系数k的大小为__________。(计算结果取2位有效数字)
33.钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式 。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是 。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。
①提出合理假设。
假设1:该漂白粉未变质,只含 ;
假设2:该漂白粉全部变质,只含 ;
假设3:该漂白粉部分变质, 。
② 设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
|
实验步骤 |
预期现象和结论 |
|
|
① |
取少量上述漂白粉于试管中, |
|
|
② |
|
|
|
③ |
|
|
32.利用从冬青中提取出的有机物A合成抗结肠炎药物Y及其他化学品,合成路线如下图:
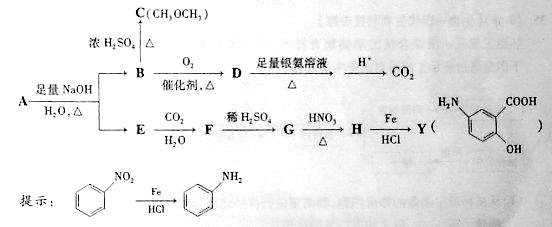
根据上述信息回答:
(1)D不与NaHCO3溶液反应,D中官能团的名称是______,B C的反应类型是____。
C的反应类型是____。
(2)①写出A生成B和E的化学反应方程式 。②写出D与足量银氨溶液反应的化学方程式 。
③写出G生成H的化学反应方程式 。
(3)A的同分异构体I和J是重要的医药中间体,在浓硫酸的作用下I和J分别生产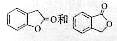 ,鉴别I和J的试剂为
。
,鉴别I和J的试剂为
。
(4)A的另一种同分异构体K用于合成高分子材料,K可由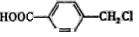 制得,写出K在浓硫酸作用下生成的聚合物的结构简式_______________
制得,写出K在浓硫酸作用下生成的聚合物的结构简式_______________
31.现代循环经济要求综合考虑环境污染和经济效益。请填写下列空白。
(1)实验室里,可用于吸收SO2尾气的一种试剂是 。
(2)高纯氧化铁可作现代电子工业材料。以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、 FeO、SiO2)为原料制备高纯氧化铁(软磁α- Fe2O3)的生产流程示意图:


①步骤I中过滤所得滤渣的主要成分是 。
②步骤II中加入铁粉的目的是 。
③步骤Ⅲ中可选用 试剂调节溶液的pH(填标号)。
A.稀硝酸 B.双氧水
C.氨水 D.高锰酸钾溶液
④写出在空气中煅烧FeCO3,制备高纯氧化铁的化学方程式 。
⑤从滤液C中回收的主要物质的一种用途是 。
30.CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
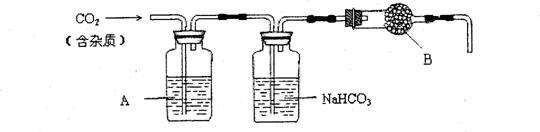
完成下列填空:
1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol.L-1),应选用的仪器是 。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
2)上述装置中,A是 溶液,NaHCO3溶液可以吸收 。
3)上述装置中,b物质是 。用这个实验得到的气体测定CO2的分子量,如果B物质失效,测定结果 (填“偏高”、“偏低”或“不受影响”)。
4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
为了将石蜡和碳酸钙溶出,应选用的试剂是 。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸d 正已烷
5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出 后溶出 。
6)上述测定实验中,连续 ,说明样品已经恒重。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com