
16.(8分)坐落在山东沿海地区的潍坊纯碱厂是我国重点大型企业,其生产工艺沿用我国化学侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
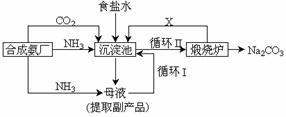
①上述生产纯碱的方法称 ,副产品的一种用途为 。
②沉淀池中发生的化学反应方程式是 。
③写出上述流程中X物质的分子式 。
④使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 (填上述流程中的编号)的循环。
⑤向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 。
A.增大NH4+的浓度,使NH4Cl更多地析出
B.使NaHCO3更多地析出
C.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
15.(12分)粗盐提纯的研究。
[有关资料]
|
化学式 |
CaCO3 |
CaSO3 |
CaC2O4 |
Mg(OH)2 |
|
Ksp |
4.96×10-9 |
4.96×10-9 |
2.34×10-9 |
5.61×10-12 |
某研究性学习小组对粗盐的提纯和检验进行研究,并提出一些新的方案。已知该粗盐样品中主要含有不溶性杂质、Mg2+、Ca2+等(忽略SO42-的存在),该小组设计流程如下:
 [设计除杂过程]
[设计除杂过程]
(1)操作①中需要使用的玻璃仪器有 、 。操作②的名称为 。
(2)混合液A的主要成分是 。(填化学式)
[检验除杂效果]
(3)为检验溶液B中Mg2+、Ca2+是否除尽,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+是否除尽。向其中一支试管中加入 溶液(填化学式),看是否有沉淀生成。
 步骤二:检验Ca2+是否除尽。向另一支试管中加入某溶液,看是否有沉淀生成。效果最好的是
(填字母)。A.Na2CO3 B.Na2SO3 C.Na2C2O4
步骤二:检验Ca2+是否除尽。向另一支试管中加入某溶液,看是否有沉淀生成。效果最好的是
(填字母)。A.Na2CO3 B.Na2SO3 C.Na2C2O4
[获取纯净食盐]
(4)对溶液B加热并不断滴加6 mol·L-1的盐酸溶液,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C,该操作的目的是 。
(5)将溶液C倒入 (填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到 时(填现象),停止加热。
[问题讨论]
(6)在除杂过程中,向粗盐悬浊液中加混合液A,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在 以下。
14.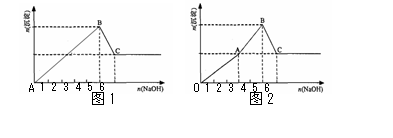 Mg2+和Al3+的混和溶液中逐滴加入NaOH溶液,形成沉淀的情况出现两种图示。图1为小杨同学绘制,图2是小周根据实验结果绘制,查阅沉淀生成和Al(OH)3溶解的pH情况如表。下列说法正确的是
Mg2+和Al3+的混和溶液中逐滴加入NaOH溶液,形成沉淀的情况出现两种图示。图1为小杨同学绘制,图2是小周根据实验结果绘制,查阅沉淀生成和Al(OH)3溶解的pH情况如表。下列说法正确的是
 A. 据图计算得n(Mg2+): n(Al3+)=2:1
A. 据图计算得n(Mg2+): n(Al3+)=2:1
B. 小周实验中,OA段生成两种沉淀
C. 图2中OA段表示仅生成Al(OH)3沉淀,AB段仅生成 Mg(OH)2
D. 结合表中数据和图2分析,AB段可能发生:Mg2++2AlO2-+4H2O =2Al(OH)3↓+Mg(OH)2↓
第II卷(非选择题 共72分)
13.下列溶液中微粒的物质的量浓度关系正确的是
A.浓度均为0.1 mol/L的两种溶液:氨水和盐酸,等体积混合后的溶液:
c(H+)= c(OH-) + c(NH3·H2O)
B.向体积为Va 的0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,Va<Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H+)
C.在NaHB溶液中一定有:c(Na+) + c(H+) =c(HB-) + c(OH-) +2 c(B2-)
D.Na2CO3溶液中:2c(Na+) =c(CO32-) + c(HCO3-) + c(H2CO3)
12. 固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,其工作原理如图所示。下列关于固体燃料电池的有关说法正确的是
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过,其工作原理如图所示。下列关于固体燃料电池的有关说法正确的是
A.电极b为电池负极,电极反应式为O2+4e-=2O2-
B.固体氧化物的作用是让电子在电池内部通过
C.若H2作燃料气,接触面上发生的反应为:H2+2OH--2e-=2H2O
D.若C2H4作燃料气,接触面上发生的反应为:C2H4+6O2--12e-=2CO2+2H2O
11.下列离子方程式正确的是
A.硫化钠的水解反应:S2-+H3O+ HS-+H2O
HS-+H2O
B.在氯化亚铁溶液中加入稀硝酸:3Fe2+ + 4H+ + NO3-=3Fe3+ + NO↑ + 2H2O

 C.向Ca(HCO3)2溶液中加入足量的氢氧化钠溶液: Ca2++HCO3-+OH-=CaCO3↓ + H2O
C.向Ca(HCO3)2溶液中加入足量的氢氧化钠溶液: Ca2++HCO3-+OH-=CaCO3↓ + H2O
D.用铜为电极电解稀硫酸溶液: 2H2O O2↑ + 2H2 ↑高考
10.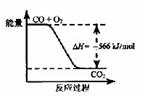 已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+1/2 O2(g) ΔH=-226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是
A.CO的燃烧热为283 kJ
B.上图可表示为CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g ) ΔH>-452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
9.进行化学实验,观测实验现象,通过分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是:
A.在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中含有SO42-
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口,说明此位置指示的是被蒸馏出物质的沸点。
C.将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化
D.浓硝酸在光照条件下变黄,说明浓硫酸不稳定生成有色产物能溶于浓硫酸
8.根据下列短周期元素性质的数据判断,下列说法正确的是
 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径/10-10 m |
0.66 |
1.36 |
1.23 |
1.10 |
0.99 |
1.54 |
0.70 |
1.18 |
|
最高或最低化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
|
|
-3 |
-1 |
|
-3 |
|
A.元素①⑧形成的化合物具有两性 B.元素⑦位于第二周期Ⅴ族
C.元素④⑤形成的化合物是离子化合物 D.元素③的最高价氧化物对应水化物碱性最强
7.在下列给定条件的溶液中,离子一定能大量共存的是
A.PH=1的溶液中:K 、Fe
、Fe 、Cl
、Cl 、NO3-
、NO3-
 B.(NH4)2Fe(SO4)2·6H2O溶液中:Na
B.(NH4)2Fe(SO4)2·6H2O溶液中:Na 、Cu
、Cu 、Cl
、Cl 、H
、H
C.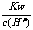 =0.1 mol/L的溶液:Na+、NH+4、SO42-、AlO2-
=0.1 mol/L的溶液:Na+、NH+4、SO42-、AlO2-
D.水电离出的c(H+) =10-12mol·L-1的溶液中:Mg2+、NH4+、HCO3-、S2-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com