
例1、(07山东)某班50名学生在一次百米测试中,成绩全部介于13秒与19秒之间,将测试结果按如下方式分成六组:第一组,成绩大于等于13秒且小于14秒;第二组,成绩大于等于14秒且小于15秒; 第六组,成绩大于等于18秒且小于等于19秒.右图是按上述分组方法得到的频率分布直方图.设成绩小于17秒的学生人数占全班总人数的百分比为
第六组,成绩大于等于18秒且小于等于19秒.右图是按上述分组方法得到的频率分布直方图.设成绩小于17秒的学生人数占全班总人数的百分比为 ,成绩大于等于15秒且小于17秒的学生人数为
,成绩大于等于15秒且小于17秒的学生人数为 ,则从频率分布直方图中可分析出
,则从频率分布直方图中可分析出 和
和 分别为( )
分别为( )
A.0.9,35 B.0.9,45
C.0.1,35 D.0.1,45
例2、(07海南)甲、乙、丙三名射箭运动员在某次测试中各射箭20次,三人的测试成绩如下表:
|
甲的成绩 |
||||
|
环数 |
7 |
8 |
9 |
10 |
|
频数 |
5 |
5 |
5 |
5 |
|
乙的成绩 |
||||
|
环数 |
7 |
8 |
9 |
10 |
|
频数 |
6 |
4 |
4 |
6 |
|
丙的成绩 |
||||
|
环数 |
7 |
8 |
9 |
10 |
|
频数 |
4 |
6 |
6 |
4 |
 分别表示甲、乙、丙三名运动员这次测试成绩的标准差,则有( )
分别表示甲、乙、丙三名运动员这次测试成绩的标准差,则有( )
A、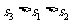 B、
B、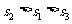 C、
C、 D、
D、
例3、(06江苏)某人5次上班途中所花的时间(单位:分钟)分别为x,y,10,11,9.已知这组数据的平均数为10,方差为2,则|x-y|的值为( )
A、1 B、2 C、3 D、4
例4、(05湖北)某初级中学有学生270人,其中一年级108人,二、三年级各81人,现要利用抽样方法抽取10人参加某项调查,考虑选用简单随机抽样、分层抽样和系统抽样三种方案,使用简单随机抽样和分层抽样时,将学生按一、二、三年级依次统一编号为1,2,…,270;使用系统抽样时,将学生统一随机编号1,2,…,270,并将整个编号依次分为10段。如果抽得号码有下列四种情况:
①7,34,61,88,115,142,169,196,223,250;
②5,9,100,107,111,121,180,195,200,265;
③11,38,65,92,119,146,173,200,227,254;
④30,57,84,111,138,165,192,219,246,270;
关于上述样本的下列结论中,正确的是( )
A、②、③都不能为系统抽样 B、②、④都不能为分层抽样
C、①、④都可能为系统抽样 D、①、③都可能为分层抽样
(三)解答题:
7、(04全国Ⅰ20)从10位同学(其中6女,4男)中随机选出3位参加测验,每位女同学能通过测验的概率均为 ,每位男同学能通过测验的概率均为
,每位男同学能通过测验的概率均为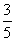 。试求:(I)选出的3位同学中,至少有一位男同学的概率;(II)10位同学中的女同学甲和男同学乙同时被选中且通过测验的概率。
。试求:(I)选出的3位同学中,至少有一位男同学的概率;(II)10位同学中的女同学甲和男同学乙同时被选中且通过测验的概率。
(二)填空题:
5、(07上海)在五个数字 中,若随机取出三个数字,则剩下两个数字都是奇数的概率是 (结果用数值表示);
中,若随机取出三个数字,则剩下两个数字都是奇数的概率是 (结果用数值表示);
6、(06上海)两部不同的长篇小说各由第一、二、三、四卷组成,每卷1本,共8本.将它们任意地排成一排,左边4本恰好都属于同一部小说的概率是 (结果用分数表示)。
(一)选择题:
1、(07福建)如图,三行三列的方阵中有9个数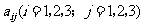 ,从中任取三个数,则至少有两个数位于同行或同列的概率是( )
,从中任取三个数,则至少有两个数位于同行或同列的概率是( )
A、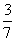 B、
B、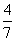

C、 D、
D、
2、(07重庆)从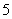 张
张 元,
元, 张
张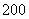 元,
元, 张
张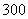 元的奥运预赛门票中任取
元的奥运预赛门票中任取 张,则所取
张,则所取 张中至少有
张中至少有 张价格相同的概率为( )
张价格相同的概率为( )
A、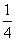 B、
B、 C、
C、 D、
D、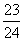
3、(07湖北)连掷两次骰子得到的点数分别为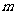 和
和 ,记向量
,记向量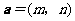 与向量
与向量 的夹角为
的夹角为 ,则
,则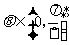 的概率是( )
的概率是( )
A、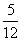 B、
B、 C、
C、 D、
D、
4、(06福建)在一个口袋中装有5个白球和3个黑球,这些球除颜色外完全相同。从中摸出3个球,至少摸到2个黑球的概率等于( )
A、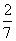 B、
B、 C、
C、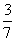 D、
D、
例1、(07辽宁)一个坛子里有编号为1,2,…,12的12个大小相同的球,其中1到6号球是红球,其余的是黑球,若从中任取两个球,则取到的都是红球,且至少有1个球的号码是偶数的概率是( )
A、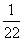 B、
B、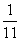 C、
C、 D、
D、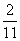
例2、(07四川)已知一组抛物线 ,其中a为2,4,6,8中任取的一个数,b为1,3,5,7中任取的一个数,从这些抛物线中任意抽取两条,它们在与直线x=1交点处的切线相互平行的概率是( )
,其中a为2,4,6,8中任取的一个数,b为1,3,5,7中任取的一个数,从这些抛物线中任意抽取两条,它们在与直线x=1交点处的切线相互平行的概率是( )
A、 B、
B、 C、
C、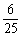 D、
D、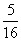
例3、(07宁夏20文)设有关于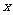 的一元二次方程
的一元二次方程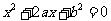 .
.
(Ⅰ)若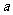 是从
是从 四个数中任取的一个数,
四个数中任取的一个数, 是从
是从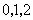 三个数中任取的一个数,求上述方程有实根的概率;
三个数中任取的一个数,求上述方程有实根的概率;
(Ⅱ)若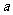 是从区间
是从区间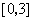 任取的一个数,
任取的一个数, 是从区间
是从区间 任取的一个数,求上述方程有实根的概率.
任取的一个数,求上述方程有实根的概率.
设事件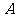 为“方程
为“方程 有实根”.
有实根”.
当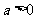 ,
, 时,方程
时,方程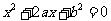 有实根的充要条件为
有实根的充要条件为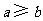 .
.
(Ⅰ)基本事件共12个:
 .其中第一个数表示
.其中第一个数表示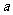 的取值,第二个数表示
的取值,第二个数表示 的取值.
的取值.
事件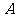 中包含9个基本事件,事件
中包含9个基本事件,事件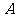 发生的概率为
发生的概率为 .
.
(Ⅱ)试验的全部结束所构成的区域为 .
.
构成事件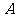 的区域为
的区域为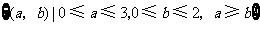 .
.
所以所求的概率为 .
.
21.(12分)材料(选修三课本第44页实验2-2):向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
 Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
Ⅰ.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出与H2O分子互为等电子体的微粒 (填2种)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是 。
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
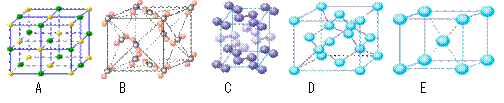
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是 (请用相应的编号填写)。

Ⅱ.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上。
(4) 写出铜原子价电子层的电子排布式 ,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有 (填元素符号)。
(5) 实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有 。
(6) 实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是 。
江苏省泰兴市2010届高三开学初调研测试
20.(10分) FeCl3可用作印刷电路铜板腐蚀剂。为回收废腐蚀液中的铜,必须对废腐蚀液的组成进行分析。某同学取废腐蚀液200mL,分成甲、乙两等份。向甲溶液中滴加AgNO3溶液至不再有沉淀产生,得到沉淀129.15g;向乙溶液中加入10g足量铁粉,充分反应,剩余固体质量4.8g。计算中忽略溶液体积的变化。
⑴写出FeCl3溶液腐蚀印刷电路铜板的离子方程式,并标出电子转移的方向和数目 。
⑵废腐蚀液中含有的Cl-离子的物质的量浓度是 。
⑶计算废腐蚀液中铜离子的物质的量浓度(写出计算过程)。
19. (10分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
(10分)随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
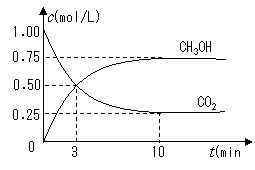
 ⑴.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
⑴.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)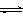 CH3OH(g)+H2O(g);△H=-49.0kJ/mol
CH3OH(g)+H2O(g);△H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示.
①从反应开始到平衡,氢气的平均反应速率v(H2)=___________mol/(L·min).
②该反应的平衡常数表达式为__________________.
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________.
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵.在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2.某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料.已知该反应的阳极反应为:4OH――4e―=O2↑+2H2O,则阴极反应式为________________________________.
有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染.请你判断是否可行并说出理由______________________________________________.
18.(8分)水煤气 (主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得。
己知:C
(s) + H2O(g)  CO (g) +H2 (g);△H
=+131.3kJ•mol-1
CO (g) +H2 (g);△H
=+131.3kJ•mol-1
C (s) + O2(g)=CO (g); △H = -110.5kJ·mo1-1
CO(g) + O2(g) =CO2 (g);△H =-283.0 kJ·mo1-1
H2 (g) + O2 (g) =H2O (g);△H = -241.8kJ·mo1-1
H2 (g) + O2 (g) =H2O (l); △H = -285.8kJ·mo1-1
⑴将2.4 g 炭转化为水煤气,再完全燃烧,整个过程的△H = kJ·mo1-1。
⑵最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中
 提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
在合成塔中,若有4.4kg CO2与足量H2恰好完全反应,可放出4947kJ的热量,试写出合成塔中发生反应的热化学方程式 。
⑶小亮同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积(Ksp)分别为4.96×10-9、2.58×10-9。小亮应该选用的试剂是 ,实验时测定的数据除空气的体积外,还需要测定 。
17.(12分)由白色和黑色固体组成的混合物A,可以发生如下框所示的一系列变化:


(1)写出反应③的化学方程式: 。
反应④的离子方程式: 。
(2)操作②的名称是 。
(3)下列实验装置中可用于实验室制取气体G的发生装置是 (填序号)。
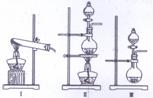
为了得到纯净干燥的气体G,可将气体通入a和b装置,a、b两广口瓶中所装入的溶液依次是a: ,b: 。c、d装置不完整,请在图中补充完整。

(4)气体G有毒,为了防止污染环境,必须将尾气进行处理,请写出d中发生反应的的离子方程式: ;
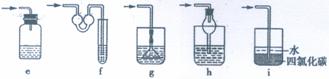
(5)J是一种极易溶于水的气体,为了防止倒吸,下列e-i装置中,可用于吸收J的
是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com