
5.命题: “ 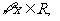
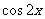 ≤
≤ ”的否定为 ( )
”的否定为 ( )
A.

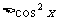 B.
B.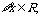
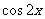
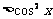
C.
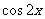

 D.
D.
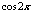 ≤
≤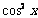
4.将函数f(x)的图象沿x轴向右平移个单位,再将横坐标伸长为原来的2倍(纵坐标不变),得到的图象所对应的函数为y=cosx,则f(x)为 ( )
A.y=cos(2x+) B.y=cos(2x-)
C.y=cos(2x+π) D.y=cos(2x-π)
3.若定义在R上的函数f(x)满足f(+x)=-f(x),且f(-x)=f(x),则f(x)可以是( )
A.f(x)=2sinx B.f(x)=2sin3x
C.f(x)=2cosx D.f(x)=2cos3x
2.已知等差数列{an}满足a2+a4=4,a3+a5=10,则它的前10项的和S10= ( )
A.138 B.13 C.95 D.23
1.角α的终边经过点P(x,-)(x≠0),且cosα=x,则sinα等于 ( )
A.x B. C.x D.-
(二)测定K2CO3质量分数

(1)甲同学用图1所示装置,把xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是
。
(2)乙同学用图2代替图1中的收集装置,则所测K2CO3质量分数 (填“偏大”、“偏小”、“不变”),你的改进方案是 。
(3)丙同学用图3装置测定CO2的质量,该装置存在较多缺陷,从而导致实验误差,请你填写其中的三点缺陷:I ;
Ⅱ
Ⅲ
21.(12分)钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
⑴钾和硝酸钾反应可制得氧化钾K+KNO3→K2O+N2(未配平),每生成9.4gK2O消耗的还原剂有___________g
⑵超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂。请尝试写出超氧化钾与二氧化碳反应的化学方程式
__________________________________________________________________________,为了维持气压稳定可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为____________
⑶KO2加热至600℃部分分解得到产物A。6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比。如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比。
__________________________________________________________________________
(一)补全以下检验混合物中存在K2CO3的实验步骤及相关现象
1.取混合物样品溶于水,分别取少量溶液进行以下实验
2._________________________________________则一定存在K+;
3.___________________________________________________则一定存在CO32-。
17.(6分)
四种短周期元素A、B、C、D,它们原子的电子层数与最外层电子数之比分别为: 3:1, 1:1 , 1:2 和 1:3 。据此回答下列问题:
(1)仅根据上述信息就能够确定的元素是 (选填A、B、C、D)。
(2)在所有满足上述信息的短周期元素中,酸性最强的最高价氧化物的水化物是(填化学式) ;由A、D两元素构成的化合物A2D2的电子式为(用元素符号填写,下同): 。
(3)在满足上述信息的短周期元素中,若B2、CD和由B、C、D形成的化合物X的混合物 mg,在一定条件下与过量氧气充分反应后,将产物通过足量的固体A2D2,最终发现固体质量增重mg,则符合此条件的X的分子组成可用通式____________________来表示。
18.(6分)某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe2(SO4)3,在反应后的溶液中滴加KSCN溶液不显红色。
(1)该反应中,被氧化的元素是____________,氧化剂是____________。
(2)写出该反应的化学方程式并标明电子转移的方向和数目:
___________________________________________________________________________。
19.(12分)下图是明矾(KAl(SO4)2•12H2O)制取硫酸铝和硫酸钾的操作步骤流程图(图中略去了沉淀物的洗涤操作),请在图中圆括号内填入适当的试剂名称,在方括号内填入适当的分离方法,并回答有关问题。

(1)试剂(a)是________________,(b)是______________,(c)是____________;
(2)分离方法①是________________,③是____________________;进行上述操作要用到的玻璃仪器有_______________________________。
(3)按上述操作,不考虑损耗,在理论上158g明矾(摩尔质量474g/mol)最多可以制得硫酸铝晶体(Al2(SO4)3•18H2O)(摩尔质量666g/mol) _____g,至少可以制备K2SO4(摩尔质量174g/mol)_______g。
20.(16分)某校化学小组的同学开展K2CO3和NaCl的固体混合物中K2CO3的检验与质量分数测定的探究实验,他们提出下列实验方案。
16.下列实验现象与结论相符合的是 ( )
A.直接观察焰色反应火焰为浅紫色,则一定不含Na元素
B.铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色;铝热剂中一定不含Fe2O3
C.溶液中滴加盐酸酸化BaCl2溶液出现白色沉淀,则溶液中一定存在SO42-
D.某气体能使品红溶液褪色,则该气体为SO2气体
15.将质量为W1g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1L。向溶液中逐滴加入浓度为a mol·L-1的HC1溶液,过程中有白色沉淀产生后又逐渐溶解,当沉淀恰好消失时所加HC1溶液体积为V2L。将溶液蒸干充分灼烧得到固体W2g。下列关系式中错误的是 ( )
A.24n(A1)+35.5n(Na)=W2-W1
B.n(Na)+3n(A1)=aV2
C.n(Na)+3n(A1)=V1/11.2
D.aV2=V1/22.4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com