
1.昼夜更替:此处需要注意,学生容易理解为自
转产生了昼夜现象,但地球不自转仍有昼夜现象,在一
年中地球公转也会使某一地有一次昼夜变化,只有地球
不停地自转,才会产生昼夜更替现象。
①在晨昏线上各地,太阳高度为0º;
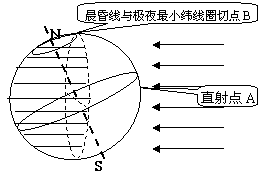 ②太阳直射光线与晨昏线成90º;
②太阳直射光线与晨昏线成90º;
③直射点A与晨昏线和极昼(夜)最小纬线圈切点
B的纬度之和等于90º;
如当太阳直射在北回归线(23º26´N)时,
切点B的纬度为66º34´N。
当太阳直射在20ºS时,切点B的纬度为
70ºN。
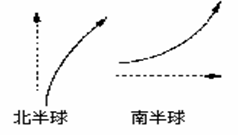
例3:在下面两图中绘出晨昏线。
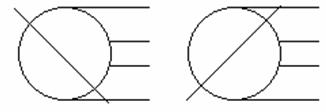
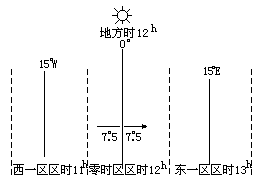 2.地方时与区时:随地球自转,一天中太阳东升西落,太阳经过某地上中天时为此地的地方时12点,因此,不同经线上具有不同的地方时。跨经度15度的区域使用同一时间为区时(本区中央经线上的地方时),全世界所用的同一时间是世界时(0度经线的地方时)。区时经度每隔15度差一小时,地方时经度每隔1度差4分钟。
2.地方时与区时:随地球自转,一天中太阳东升西落,太阳经过某地上中天时为此地的地方时12点,因此,不同经线上具有不同的地方时。跨经度15度的区域使用同一时间为区时(本区中央经线上的地方时),全世界所用的同一时间是世界时(0度经线的地方时)。区时经度每隔15度差一小时,地方时经度每隔1度差4分钟。
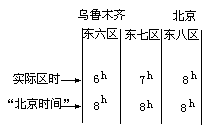
北京时间:东八区的区时,120ºE的地方时。离北京所在的东八区较远的地区,作息时间与北京不同。例如,新疆的乌鲁木齐市,人们一般10点钟上班,14点吃午饭。因为乌鲁木齐在东6区,与北京时差为2小时,如果乌鲁木齐的人们使用东6区的区时,作息时
 间会与北京相同,但乌鲁木齐使用的是东8区的区时“北京时间”,所以他们的作息就在“北京时间”的基础上延迟了2小时。(上图解)
间会与北京相同,但乌鲁木齐使用的是东8区的区时“北京时间”,所以他们的作息就在“北京时间”的基础上延迟了2小时。(上图解)
3、速度:
 线速度:单位时间转过的弧长。赤道周长约4万千米,线速度最大(约为1670km/h),向高纬递减,两极为零。纬度为α°的某地其线速度约为1670km/h × cos α°
线速度:单位时间转过的弧长。赤道周长约4万千米,线速度最大(约为1670km/h),向高纬递减,两极为零。纬度为α°的某地其线速度约为1670km/h × cos α°
角速度:单位时间转过的角度。地球各地角速度(两极为零)相等,为15°/小时。
例2.完成右表,填写地球自转的方向、周期、速度
2、周期:地球自转一周(360º)所需的时间。1恒星日为23时56分4秒。1太阳日为24小时。



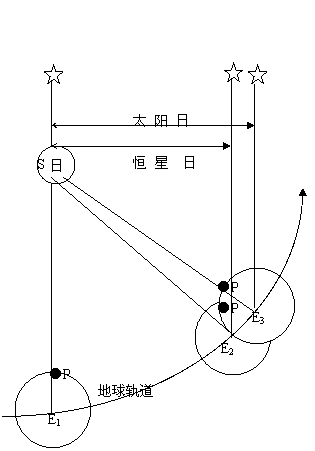 如右图是恒星日和太阳日比较。地球在轨道上有三个不同位置:第一个位置上E1,太阳和某恒在P地同时中天,这是一个恒星日和一个太阳日的共同起点。在第二个位置上E2,地球完成自转一周,恒星再度在P地中天,一个恒星日终了,但正午尚未到来。到第三个位置上E3时,太阳第二次在P地中天(SPE3在同一直线上),从而完成一个太阳日;那时恒星早已越过中天。读这个图必须注意,在太阳系范围内,太阳是中心天体,它的光线是辐散的;恒星无比遥远,它的光线可看作平行的,图中所示三颗星,指的是同一颗恒星。太阳日是日常生活的周期,古人云:日出而作日没而息。
如右图是恒星日和太阳日比较。地球在轨道上有三个不同位置:第一个位置上E1,太阳和某恒在P地同时中天,这是一个恒星日和一个太阳日的共同起点。在第二个位置上E2,地球完成自转一周,恒星再度在P地中天,一个恒星日终了,但正午尚未到来。到第三个位置上E3时,太阳第二次在P地中天(SPE3在同一直线上),从而完成一个太阳日;那时恒星早已越过中天。读这个图必须注意,在太阳系范围内,太阳是中心天体,它的光线是辐散的;恒星无比遥远,它的光线可看作平行的,图中所示三颗星,指的是同一颗恒星。太阳日是日常生活的周期,古人云:日出而作日没而息。
例1、乘船从上海至旧金山,船上乘客观察的现象正确的是( C )
A、恒星日不变,太阳日为24时 B、恒星日不变,太阳日大于24时
C、恒星日不变,太阳日小于24时 D、恒星日不变,太阳日为24时
1、地球自转的方向:自西向东。地轴北端始终指向北极星。

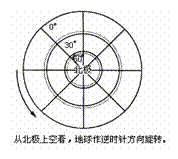

注意:经纬线形状、极点、赤道和旋转方向。在右图方框内以南极为中心作图。
31.(16分)以下是某生物兴趣小组进行的光合作用实验。利用打孔器对爬山虎和石榴的幼嫩叶片打孔,获取一批直径为0.8cm的叶圆片。设法使叶圆片内细胞间隙中的气体排出、叶圆片沉到蒸馏水中,置于黑暗中待用。取4支试管,按下表中“处理”的步骤操作,之后将4支试管同时置于60W的白炽灯下,各试管与白炽灯的距离均为20cm,观察叶圆片上浮的情况。实验结果见下表中的“结果”。
|
试 管 |
1号 |
2号 |
3号 |
4号 |
|
|
处 理 |
溶液(10mL) |
蒸馏水 |
1%NaHCO3 |
蒸馏水 |
1%NaHCO3 |
|
植物种类 |
爬山虎 |
爬山虎 |
石榴 |
石榴 |
|
|
叶圆片数(均沉入水底) |
4 |
4 |
4 |
4 |
|
|
结 果 |
第1片叶圆片上浮的时间 |
/ |
第78分钟 |
/ |
第100分钟 |
|
第4片叶圆片上浮的时间 |
/ |
第140分钟 |
/ |
第211分钟 |
|
|
实验结束时沉没水底的叶圆片数 |
4 |
0 |
4 |
0 |
请分析回答下列问题。
⑴试解释2号和4号试管中的叶圆片上浮的原因:
。
⑵试解释1号和3号试管中的叶圆片到实验结束时仍沉没水底的原因:
。
⑶为什么不同植物的叶圆片在相同条件下上浮所需的时间不同?有的同学认为是由于不同植物的叶圆片重量不同,有的同学认为是由于不同植物的光合作用速率不同,有的同学认为是由于不同植物的叶细胞间隙大小不同(细胞间隙越大积聚气体的速度越快)。同学们利用电子天平测量相同数量的爬山虎和石榴的叶圆片重量,发现两者等重。那么,应如何针对上述问题展开进一步的探究?如果你是小组成员,请你简要说明实验思路。
①
;
②
。
30.(I)、(12分)视网膜母细胞瘤是婴幼儿最常见的眼内恶性肿瘤。视网膜母细胞瘤基因(Rb)是第一个被克隆的抑癌基因,它被定位于人类第13号染色体上。医生Kundson在观察研究中发现,某些家庭中儿童恶性的“视网膜母细胞瘤”发病率比正常人群高1000倍。下表是他记录的甲患者和乙患者的部分信息,基因A表示正常的Rb基因,基因a表示失活的Rb基因。请回答相关问题:
|
患者 |
患者的 T淋巴细胞 |
患者眼部的 癌细胞 |
患者父亲的 T淋巴细胞 |
患者母亲的 T淋巴细胞 |
患者家族其它成员发病情况 |
|
甲 |
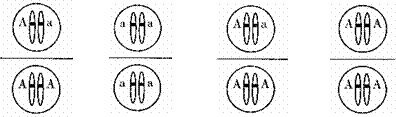 |
|
|
|
有患者 |
|
乙 |
|
|
|
|
无患者 |
(1)人类13号染色体上的基因A通过 过程控制合成了视网膜母细胞瘤蛋白(pRb),保证了正常的细胞凋亡过程,从而抑制了细胞癌变。
(2)甲、乙患者的正常细胞在个体发育的过程中都发生了 ,因而癌细胞的13号染色体上均无正常的视网膜母细胞瘤基因。请根据表中信息分析甲患者家族中视网膜母细胞瘤发病率明显高于正常人群的主要原因是: _____________________________________________________________________________。
(3)甲的父母计划再生育一个孩子,他们向医生进行遗传咨询,医生认为子代的肿瘤再发风险率很高,基因A可能变异而失活的的两个时期是________________________________和__________________________________。为达到优生目的,医生建议他们进行产前诊断,主要是用 的手段对胎儿进行检查。
(II)(16分)下面列出了某人空腹验血后得到的几项指标:
|
项目名称 |
结果 |
参考值 |
|
CHO总胆固醇 |
7.1 |
2.6--5.7mmol/L |
|
TG甘油三酯 |
3.52 |
0.22--1.71
mmol/L |
|
LDL低密度脂蛋白 |
4.22 |
1.27--4.13
mmol/L |
|
GLU葡萄糖 |
8.32 |
3.89--6.11
mmol/L |
(1)葡萄糖是细胞生命活动的_____________________,由于______________________代谢
出现障碍,导致血糖和血脂含量都偏高。
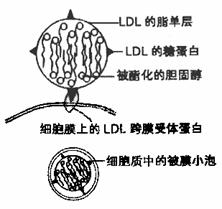
(2)有关资料表明:胆固醇在肝细胞内合成后,与磷脂和蛋白质形成低密度脂蛋白(简
称LDL)释放到血液中。如图所示:LDL颗粒中有很多被酯化的胆固醇分子,由磷脂分子、未酯化的胆固醇和糖蛋白形成的脂单层包围着。当细胞进行膜合成需要胆固醇时,细胞就合成LDL跨膜受体蛋白,并将其嵌插到质膜中。LDL颗粒与受体结合后,形成被膜小泡进入细胞质,最终在溶酶体内LDL被分解成游离的胆固醇而被利用。
当细胞中的胆固醇积累过多时,细胞会停止合成自身的胆固醇,并关闭了LDL受体蛋白的合成途径,暂停吸收外来的胆固醇。如果人编码LDL受体蛋白的基因有遗传缺陷,就会造成血液中LDL含量过高,长时间LDL指标偏高会使人患动脉粥样硬化症危害生命。
①包围LDL颗粒脂单层上的糖蛋白承担着______________________作用,LDL颗粒通过
______________________作用进入细胞。
②细胞合成的LDL跨膜受体蛋白能够嵌插到细胞膜中,说明细胞膜具有_______________
的特点。LDL颗粒能够进入溶酶体是因为被膜小泡与溶酶体发生了______________。
③当细胞中的胆固醇积累过多时,细胞停止合成自身的胆固醇,说明细胞对胆固醇的
合成具有_____________________。LDL指标偏高可能是____________________。
29.(17分)碱存在下,卤代烃与醇反应生成醚(R-O-R‘):

R-X+R‘OH R-O-R‘+ HX
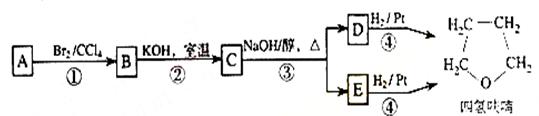 化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下:
化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下:
请回答下列问题:
(1)1 molA和1 molH2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%, 则Y的分子式为___________ A的结构简式为_______________________。
(2)第①②步反应类型分别为 ①___________________②____________________ _。
(3)化合物B具有的化学性质(填写字母代号)是_________________________________。
a可发生氧化反应 b强酸或强碱条件下均可发生消去反应
c可发生酯化反应 d催化条件下可发生加聚反应
(4)写出D和E的结构简式:
D______________________________,E___________________________________ 。
(5)写出化合物C与 NaOH 水溶液共热的化学反应方程式:
___________________________________________________________________________。
(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:
_____________________________________________________________________ 。
28.(15分)七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-一硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Mg(OH)2 |
|
pH值 |
5.2 |
3.2 |
9.7 |
10.4 |
11.2 |
表2 两种盐的溶解度(单位为g/100g水)
|
温度 / ℃ |
10 |
30 |
40 |
50 |
60 |
|
CaSO4 |
0.19 |
0.21 |
0.21 |
0.20 |
0.19 |
|
MgSO4·7H2O |
30.9 |
35.5 |
40.8 |
45.6 |
/ |
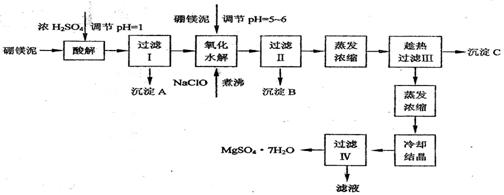 硼镁泥制取七水硫酸镁的工艺流程如下:
硼镁泥制取七水硫酸镁的工艺流程如下:
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5-6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 _______ ,加热煮沸的主要目的是_ _______ __________________________________________。
(2)沉淀B中除MnO2、SiO2外还含有 ___________________ (填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 ____________________ 。
(4)沉淀C的化学式是 _____ ;过滤II需趁热的理由是 _____________ 。
27.(10分)工业上合成氨的化学反应 N2(g)+ 3H2(g)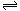 2NH3(g) △H = - 46.2KJ·mol-1、
2NH3(g) △H = - 46.2KJ·mol-1、
△S = -198.3J·mol-1·K-1。在容积为10L的密闭容器中,通入40mol N2和120mol H2在一定条件下进行反应,4S后达到平衡状态,此时N2浓度为2mol/L。通过计算回答下列问题:
⑴ 在温度较高时,该反应 (填“能”或“不能”)自发进行。
⑵ 用N2 表示的4S内化学反应的平均速率是 。
⑶ 在该条件下N2 的最大转化率是 ;此时混合气体中NH3的体积分数是 ____。
⑷ 为了提高氨气的产率,可以选择的方法是 。(填序号,错选扣分)
① 升高温度 ② 增大压强 ③ 使用催化剂 ④ 及时分离出NH3 。
26.(16分)A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A、B两元素的核电荷数之差等于它们的原子最外层电子数之和;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E、F形成的化合物甲、乙、丙、丁、戊、己的组成如下表所示。
|
化合物 |
甲 |
乙 |
丙 |
丁 |
戊 |
己 |
|
化学式 |
A2C |
A2C2 |
B2A2 |
D2C2 |
A2E |
DF |
回答下列问题:
(1)化合物丙的电子式为 。化合物丁存在的化学键类型是 ___。
(2)化合物甲的沸点比戊 (填“高”或“低”),原因是 _______ 。
(3)向含0.2mol乙的水溶液中加入少量MnO2,使乙完全反应,转移的电子数目为____个。
(4)2.0g丙完全燃烧,生成液态甲和B的气态氧化物,放出99.6KJ的热量,请写出表示丙的燃
烧热的热化学方程式 。
(5)用铁作阳极、石墨作阴极,电解甲、己的混合溶液,写出电极反应式:
阳极 阴极 _________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com