
18. (12分)某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4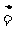 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
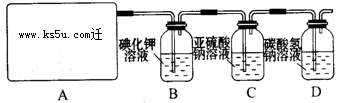
试回答:
(1)该实验中A部分的装置是 (填写装置的序号)。
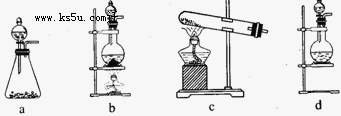
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)写出D装置中发生反应的离子方程式 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:称取漂白粉2.0 g ,研磨后溶解,配制成250 ml 溶液,取25 ml 加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。写出发生反应的离子方程式 。待完全反应后,用0.1 mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为:
2Na2S2O3 + I2 = Na2S4O6 + 2NaI
反应完成时,共用去Na2S2O3 20.0 ml。则该漂白粉中Ca(ClO)2的质量分数为:
17. .(6分)A、B、C、D为四种可溶性的盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO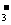 、SO
、SO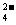 、Cl-、CO
、Cl-、CO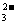 的中的一种。
的中的一种。
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据①②实验事实可推断它们的化学式为:
⑴A ,C
⑵写出足量盐酸与D反应的离子反应方程式:
⑶写出C与Ba(OH)2溶液反应的离子方程式
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
16.现有CuO和Fe2O3组成的混合物a g,向其中加入2 mol·L-1的硫酸溶液50mL,恰好
完全反应。若将a g该混合物在足量H2中加热,使其充分反应,冷却后剩余固体质量( )
A 1.6 a g B (a-1.6) g C (a-3.2) g D a g
第Ⅱ卷
15. 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2)加入100mL硫酸溶液,
充分反应后向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量与加入
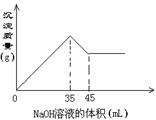 NaOH溶液的体积关系如图所示,则所用硫酸溶液的物质的量浓度为 ( )
NaOH溶液的体积关系如图所示,则所用硫酸溶液的物质的量浓度为 ( )
A.3.50mol/L B.1.75mol/L
C.0.85mol/L D.无法计算
14.下列浓度关系正确的是 ( )
A. 氯水中:c(Cl2)=2[c(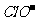 )+c(
)+c(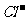 )+C(HClO)]
)+C(HClO)]
B. 氯水中:c(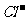 )>c(
)>c(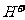 )>c(
)>c(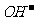 )>c(
)>c(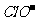 )
)
C. 等体积等浓度的氢氧化钠与醋酸混合:c(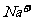 )=c(
)=c(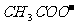 )
)
D. 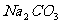 溶液中:c
溶液中:c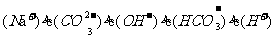
13. 1.92 g Cu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672 mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为 ( )
A.504 mL B.336 mL
C.224 mL D.168 mL
11、下列离子方程式正确的是 ( )
A.碳酸氢钠溶液与少量石灰水反应:HCO3- + Ca2+ + OH- = CaCO3↓+ H2O
B.向硫酸氢钾溶液中加入Ba(OH)2溶液至pH=7:
2H+ + SO42-+ Ba2+ + 2OH-= BaSO4↓ + 2H2O
C.氢氧化铁沉淀可被氢溴酸溶解: 2Fe(OH)3+6H++2Br-=2Fe2++Br2+6H2O
D.次氯酸钙溶液中通人少量SO2气体:Ca2+ + 2ClO- + SO2 + H2O = CaSO3↓+ 2HClO 12.100mL含等物质的量HBr和H2SO3的溶液里通入0.01molCl2,有一半Br-变为Br2。原溶液中HBr和H2SO3的浓度都等于 ( )
A.0.0075mol/L B.0.0018mol/L C.0.075mol/L D.0.08mol/L
10、取相同体积的KI、Na2S、FeBr2溶液,分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温、同压条件下),则KI、Na2S、FeBr2溶液的物质的量浓度之比是( )
A.1∶1∶2 B.2∶1∶3 C.6∶3∶2 D.3∶2∶1
9.下列指定溶液中,各组离子可能大量共存的是 ( )
A.PH=1的溶液中:K+、Fe2+、Cl-、NO3-
B.在强酸性溶液中:Cu2+、ClO-、Cl-、Ba2+
C.在含有大量Fe3+的溶液中:NH4+、Cl-、Na+、AlO2-
D.由水电离的c(H+)=10-13mol·L-1的溶液中:Al3+、K+、NO3-、SO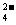
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com