
2.下列反应的离子方程式书写正确的是
A.甲酸与氢氧化钠溶液反应:H+ +OH- ═H2O
B.在Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2+ + OH- + HCO3- ═ CaCO3↓+ H2O
C.三氯化铁溶液(浓)与铜反应:Fe3+ + Cu ═ Fe2+ + Cu2+
D.氯化铝溶液中加入过量氨水:Al3+ + 3NH3·H2O ═ Al(OH)3↓+3NH4+
1.下列说法正确的是(NA表示阿伏加德罗常数的值)
A.在标准状况下,如果5.6L氧气含有n个氧原子,则NA约为4n
B.常温常压下,1 mol甲烷含有的电子数为10NA
C.1mol Cl2与足量烧碱溶液完全反应,转移电子数为2NA
D.1L0.1mol·L-1的醋酸溶液中含有离子与分子数之和为0.1NA
3.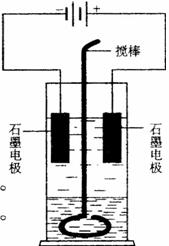 在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答:
(1)阳极上的电极反应式为______________________________。
(2)阴极上的电极反应式为______________________________。
(3)原上层液体是______________________________________。
(4)原下层液体是_____________________________________。
(5)搅拌后两层液体颜色发生变化的原因是________________________。
(6)要检验上层液体中含有的金属离子,其方法是_________________________。现象是___________________。
2.工业上为了处理含有Cr2O72-酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准。请回答下列问题:
(1)两极发生反应的电极反应式:
阳极____________________________,阴极___________________________________。
(2)写出Cr2O72-变为Cr3+的离子方程式:___________________________________。
(3)工业废水中有酸性变为碱性的原因是:__________________________________。
(4)________(填“能”或“不能”)改用石墨电极,原因是___________________。
1. 通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银):n(硝酸亚汞)=2:1,则下列表述正确的是( )
A.在两个阴极上得到的银和汞的物质的量之比n(银) :n(汞)= 2:1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的分子式为HgNO3
D.硝酸亚汞的分子式为Hg2(NO3)2
15.在25℃时,用石墨电极电解2.0L2.5mol/LCuSO4溶液,如有0.20 mol电子发生转移,请回答下列问题:
(1)阴极发生_______反应,电极反应式为________________________________;
(2) 阳极发生______反应,电极反应式为________________________________;
(3)电解后得到的铜的质量是________,得到氧气的体积是_________(标准状况),溶液的pH是______________;
(4)如用等质量的两块铜片代替石墨做电极,电解后两铜片的质量相差_______,电解液的pH ____________。
拓展提高
14.从H+、Na+、Cu2+、Cl--、SO42-五种离子中恰当地组成电解质,按下列要求进行电解: (1)以碳棒为电极,使电解质质量减少,水量不变进行电解,则可采用的电解质是_______________________ ;
(2) )以铂片为电极,使电解质质量不变,水量减少进行电解,则可采用的电解质是_______________________;
(3)以碳棒为阳极,铁棒为阴极,使电解质和水量都减少,进行电解,可采用的电解质是__________________。
13. 右图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )
 A . a为负极、b为正极
A . a为负极、b为正极
B . a为阳极、b为阴极
C 电解过程中,d电极质量增加
D 电解过程中,氯离子浓度不变
12.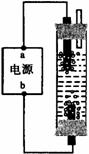 某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是( )
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是( )
A a为正极,b为负极;NaClO和NaCl
B a为负极,b为正极;NaClO和NaCl
C a为阳极,b为阴极;HClO和NaCl
D a为阴极,b为阳极;HClO和NaCl
11.在外界提供相同电量的条件下,Cu2+或Ag+分别按Cu2+ + 2e-- == Cu或Ag -- e-- == Ag+在电极上放电,其析出铜的质量为1.92g,则析出银的质量为( )
A.1.62g B.6.48g C.3.24g D.12.96g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com