
1、双线桥分析法
要点:①双线桥从左指向右连接不同价态的同种元素;
②线上标明电子得失、化合价升降、被氧化、被还原等内容(注意得失电子守恒)。
在中学化学中,常用作氧化剂的物质有: 、 、 、 、 、
等;常用作还原剂的物质有活泼的金属单质如 、 、 ,以及 、
、 等。(见人教版必修1第36页)
(1)根据元素的化合价
[练习]下列微粒:H+、Cu2+、Ag+、Fe2+、Fe3+、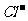 、S2-、
、S2-、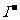 、
、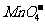 、
、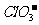 、
、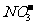 、
、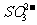 、S、Cl2、Na、H2;其中只有氧化性的是
;只有还原性的
、S、Cl2、Na、H2;其中只有氧化性的是
;只有还原性的
是 ,既有氧化性又有还原性的是 ;
[思考]如果物质中某元素具有最高价,该元素只有 性;物质中元素具有最低价,该元素只有 性;物质中元素具有中间价态,该元素既有 又有 性。对于同一种元素,价态越高,则 性越强,价态越低,则 性越强。
(2)根据氧化还原反应方程式
强还原剂(A)+强氧化剂(B)=弱氧化产物(a)+弱还原产物(b)
则氧化性:B>a,还原性:A>b
氧化剂的氧化性越强,则其对应的 产物的还原性则越 ;还原剂的还原性越强,则其对应的 产物的氧化性则越 。
(3)根据金属活动性顺序表
在金属活动性顺序表中,位置越靠前,其还原性就越 ,其阳离子的氧化性就越 。
(4)根据元素周期表
同周期元素,随着核电荷数的递增,氧化性逐渐 ,还原性逐渐 ;同主族元素,随着核电荷数的递增,氧化性逐渐 ,还原性逐渐 。
(5)根据反应的难易程度
氧化还原反应越容易进行(表现为反应所需条件越低),则氧化剂的氧化性和还原剂的还原性就越 。
不同的还原剂(或氧化剂)与同一氧化剂(或还原剂)反应时,条件越易或者氧化剂(或还原剂)被还原(或被氧化)的程度,则还原剂(或氧化剂)的还原性(或氧化性)就越 ;
(6)其它条件
一般溶液的酸性越强或温度越高,则氧化剂的氧化性和还原剂的还原性就越 ,反之则越弱。
注意:
1物质的氧化性或还原性的强弱只决定于得到或失去电子的 ,与得失电子的 无关。如:Na、Mg、Al的还原性强弱依次为Na>Mg>Al;浓HNO3、稀HNO3的氧化性强弱依次为:浓HNO3 >稀HNO3;
2同一元素相邻价态间不发生氧化还原反应。
|
概 念 |
得失氧的角度 |
化合价变化的角度 |
电子转移的角度 |
|
氧 化
剂 |
在反应中失去氧的物质 |
所含元素化合价降低的物质 |
在反应过程中得到电子的物质 |
|
还 原
剂 |
|
|
|
|
氧化反应 |
物质得到氧的反应 |
物质所含元素化合价升高的反应 |
物质失去电子的反应 |
|
还原反应 |
|
|
|
|
氧化产物 |
---- |
还原剂中所含元素化合价升高以后的对应产物 |
还原剂中失去电子以后的对应产物 |
|
还原产物 |
---- |
|
|
|
氧 化
性 |
---- |
---- |
氧化剂所具有的得到电子的能力 |
|
还 原
性 |
---- |
---- |
还原剂所具有的失去电子的能力 |
判断氧化反应、还原反应及氧化剂和还原剂、氧化产物和还原产物时可抓住下表中的关系:
|
反应物 |
变化特点 |
生成物 |
|
还原剂 |
失、高、氧---氧化反应 |
氧化产物 |
|
氧化剂 |
得、低、还---还原反应 |
还原产物 |
氧化还原反应的实质是电子的 (包括电子的得失或电子对的偏移),特征是反应前后 ;判断某反应是否属于氧化还原反应可根据反应前后 是否发生了变化这一特征。
4、某种笔记本的单价是5元,买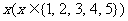 本笔记本需要y元,试用函数的三种表示法表示函数y=f(x)
本笔记本需要y元,试用函数的三种表示法表示函数y=f(x)
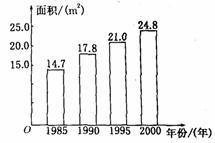
3、据新华社2002年3月12日电,1985年到2000年内,我国农村人均居住面积如下图所示,其中从 年到 年的五年间增长最快。
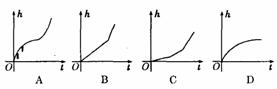
2、从水平位置的球体容器顶部的一个孔向球内以相同的速度注水,容器水面的高度h与注水时间t之间的关系用图象表示为( )
1、下列式子或表格:
①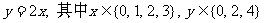 ②
②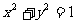 ③
③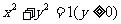
④
|
x |
1 |
2 |
3 |
4 |
5 |
|
y |
90 |
89 |
89 |
85 |
95 |
其中表示y是x的函数的是( )
A、①②③④ B、①②④ C、②③ D、③④
2、如何检验一个图形是否是一个函数的图象?
自主学习
课本P39,例1
总结作函数图象的步骤:(1) (2) (3)
体会数形结合的思想。
完成课本P41练习A1、2 P42 练习B 1、2
P40例2
理解取整函数的含义。
完成课本P42练习A 4
[例题讲解]
例1、在学校的洗衣店中每洗一次衣服(4.5公斤以内)需要付费4元,但在这家店洗衣10次可以免费洗一次。
(1)根据题意填写下表:
|
洗衣次数n |
5 |
9 |
10 |
11 |
15 |
|
洗衣费用c |
|
|
|
|
|
(2)费用c是次数n的函数还是次数n是费用c的函数?
例2、作出下列函数的图象:
(1)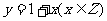 (2)
(2)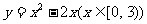
[当堂练习]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com