
9.M(NO3)2热分解化学方程式为:
2M(NO3)2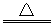 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11200mL的气体,那么M的摩尔质量是(C )
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11200mL的气体,那么M的摩尔质量是(C )
A.64g/mol B.24g/mol C.65g/mol D.40g/mol
8.将标准状况下,将VL A气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为( B )
A.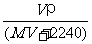 B.
B.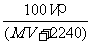
C.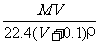 D.100VρM(MV+2240)
D.100VρM(MV+2240)
7.根据阿伏加德罗定律,下列叙述中正确的是( CD )
A.同温同压下两种气体的体积之比等于摩尔质量之比
B.同温同压下两种气体的物质的量之比等于密度之比
C.同温同压下两种气体的摩尔质量之比等于密度之比
D.同温同压下两种气体的物质的量之比等于压强之比
6.1L A气体与0.5L B气体反应,恢复原温度和压强时,生成气体的体积为1L,已知生成物的化学式为X2Y,则A的分子式为( BC )
A.XY2 B.XY C.X2 D.Y2
5.3.6g碳在一定量的氧气中燃烧,反应后生成的气体质量为9.2g。则在标准状况下,生成物CO和CO2的体积比为( C )
A.3:2 B.4:1 C.5:1 D.7:4
4.在等体积的NaCl、MgCl2、AlCl3三种溶液中,分别加入等量的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为( D )
A.1:2:3 B.3:2:1 C.1:1:1 D.6:3:2
3.将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为( D )
A.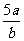 mol/L B.
mol/L B. mol/L C.
mol/L C.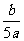 mol/L D.
mol/L D.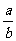 mol/L
mol/L
2.在反应3Cu2S+22HNO3 6Cu(NO3)2+3H2SO4+10NO+8H2O中,1mol还原剂失去原子的物质的量为( C )
6Cu(NO3)2+3H2SO4+10NO+8H2O中,1mol还原剂失去原子的物质的量为( C )
A.6mol B.8mol C.10mol D.12mol
1.与8g SO3中氧原子数相同的是(B )
A.9.6g H2SO4 B.6.6g CO2
C.6.4g SO4 D.6.72L CO(常温、常压)
28.硫酸银的溶解度极小,25℃时,每100g水仅溶解0.836g。
(1)25℃时,在烧杯中放入6.25g硫酸银固体,加200g水,经充分溶解后,所得饱和溶液的体积为200mL,计算溶液中Ag+离子物质的量浓度?
(2)若上述烧杯中加入50.0mL 0.0268mol/L氯化钡溶液,充分搅拌,求溶液中Ag+离子的物质的量浓度。
(3)在(1)题所述的烧杯中需加入多少升 0.0200mol/L氯化钡溶液,才能使原溶液中Ag+浓度降至0.0200mol/L?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com