
5.(09广东理科基础 34)下列有关电池的说法不正确的是
34)下列有关电池的说法不正确的是
 A.手机上用的锂离子电池属于二次电池
A.手机上用的锂离子电池属于二次电池
 B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
 C.甲醇燃料电池可把化学能转化为电能
C.甲醇燃料电池可把化学能转化为电能
 D.锌锰干电池中,锌电极是负极
D.锌锰干电池中,锌电极是负极
 答案:B
答案:B
 解析:锂离子电池可以充用,再次使用,属于二次电池,A项正确;
解析:锂离子电池可以充用,再次使用,属于二次电池,A项正确;
铜锌原电池中铜为正极,故电流为铜流向锌,而电子是由锌流向铜,B项错;
电池的实质即是化学能转化成电能,C项正确;
Zn失去电子生成Zn2+,故作为负极,D项正确
4.(09浙江卷 12)市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li
12)市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li 的高分子材料。这种锂离子电池的电池反应为:
的高分子材料。这种锂离子电池的电池反应为:
 Li+2Li
Li+2Li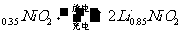
 下列说法不正确的是
下列说法不正确的是
 A.放电时,负极的电极反应式:Li-e
A.放电时,负极的电极反应式:Li-e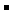 =Li
=Li
 B.充电时,Li
B.充电时,Li 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
 C.该电池不能用水溶液作为电解质
C.该电池不能用水溶液作为电解质
 D.放电过程中Li
D.放电过程中Li 向负极移动
向负极移动

 答案:D
答案:D
3.(09江苏卷 12)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
12)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
 A.该电池能够在高温下工作
A.该电池能够在高温下工作
 B.电池的负极反应为:
B.电池的负极反应为:
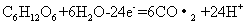
 C.放电过程中,
C.放电过程中, 从正极区向负极区迁移
从正极区向负极区迁移
 D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下
D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下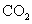 气体
气体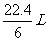
 答案:B
答案:B

 解析:
解析:
A项,高温条件下微生物会变性,所以A错;
B项,负极是葡萄糖失电子生成二氧化碳,所以B对;
C项,原电池内部阳离子应向正极移动,所以C错;
D项,消耗1mol氧气生成1mol二氧化碳,标准状况下体积是22.4L,D错
2.(09安徽卷12) Cu2O是一种半导体材料,基于绿色化学理念设计的制取.Cu2O的电解池示意图如下,点解总反应:2Cu+H2O==Cu2O+H2O
Cu2O是一种半导体材料,基于绿色化学理念设计的制取.Cu2O的电解池示意图如下,点解总反应:2Cu+H2O==Cu2O+H2O 。下列说法正确的是
。下列说法正确的是

 A.石墨电极上产生氢气
A.石墨电极上产生氢气
 B.铜电极发生还原反应
B.铜电极发生还原反应
 C.铜电极接直流电源的负极
C.铜电极接直流电源的负极
 D.当有0.1mol电子转移时,有0.1molCu2O生成。
D.当有0.1mol电子转移时,有0.1molCu2O生成。
 答案:A
答案:A
 解析:由电解总反应可知,Cu参加了反应,所以Cu作电解池的阳极,发生氧化反应,B选项错误;石墨作阴极,阴极上是溶液中的H+反应,电极反应为:2H++2e-=H2↑,A选项正确;阳极与电源的正极相连,C选项错误;阳极反应为2Cu+2
解析:由电解总反应可知,Cu参加了反应,所以Cu作电解池的阳极,发生氧化反应,B选项错误;石墨作阴极,阴极上是溶液中的H+反应,电极反应为:2H++2e-=H2↑,A选项正确;阳极与电源的正极相连,C选项错误;阳极反应为2Cu+2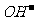 -2e-=Cu2O+H2O,当有0.1mol电子转移时,有0.05molCu2O生成,D选项错误。
-2e-=Cu2O+H2O,当有0.1mol电子转移时,有0.05molCu2O生成,D选项错误。
1.(09广东理科基础 25)钢铁生锈过程发生如下反应:
25)钢铁生锈过程发生如下反应:
 ①2Fe+O2+2H2O=2Fe(OH)2;
①2Fe+O2+2H2O=2Fe(OH)2;
 ②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
 ③2Fe(OH)3=Fe2O3+3H2O。
③2Fe(OH)3=Fe2O3+3H2O。
 下列说法正确的是
下列说法正确的是
 A.反应①、②中电子转移数目相等
A.反应①、②中电子转移数目相等
 B.反应①中氧化剂是氧气和水
B.反应①中氧化剂是氧气和水
 C.与铜质水龙头连接处的钢质水管不易发生腐蚀
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
 D.钢铁在潮湿的空气中不能发生电化学腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
 答案:A
答案:A

 解析:①②反应中消耗O2的量相等,两个反应也仅有O2作为氧化剂,故转移电子数是相等的,A项正确。①中H2O的H、O两元素的化合价没有变,故不作氧化剂,B项错;铜和钢构成原电池,腐蚀速度加快,C项错;钢铁是铁和碳的混合物,在潮湿的空气的中易发生吸氧腐蚀,属于电化学腐蚀,故D项错。
解析:①②反应中消耗O2的量相等,两个反应也仅有O2作为氧化剂,故转移电子数是相等的,A项正确。①中H2O的H、O两元素的化合价没有变,故不作氧化剂,B项错;铜和钢构成原电池,腐蚀速度加快,C项错;钢铁是铁和碳的混合物,在潮湿的空气的中易发生吸氧腐蚀,属于电化学腐蚀,故D项错。
2.金属的防护方法:①改变金属的内部组织结构。合金钢中含有合金元素,使组织结构发生变化,耐腐蚀。如:不锈钢。②在金属表面覆盖保护层。常见方式有:涂油脂、油漆或覆盖搪瓷、塑料等;使表面生成致密氧化膜;在表面镀一层有自我保护作用的另一种金属。
 ③电化学保护法:外加电源的阴极保护法:接上外加直流电源构成电解池,被保护的金属作阴极。牺牲阳极的阴极保护法:外加负极材料,构成原电池,被保护的金属作正极。
③电化学保护法:外加电源的阴极保护法:接上外加直流电源构成电解池,被保护的金属作阴极。牺牲阳极的阴极保护法:外加负极材料,构成原电池,被保护的金属作正极。

击破考点一:考查原电池的基本概念
例1:在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
A.正极附近的SO42 -离子浓度逐渐增大 B.电子通过导线由铜片流向锌片
C.正极有O2逸出 D.铜片上有H2逸出
答案:D
[变式训练1]某原电池总反应的离子方程式为: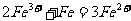 ,不能实现该反应的电池是( )
,不能实现该反应的电池是( )
 A.正极为Cu,负极为Fe,电解质为FeCl3溶液
A.正极为Cu,负极为Fe,电解质为FeCl3溶液
B.正极为Cu,负极为Fe,电解质为Fe(NO3)3溶液
C.正极为Cu,负极为Zn,电解质为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质为CuSO4溶液
答案:C
[变式训练2](2007年高考广东化学卷)科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入以磷酸为电解质的燃料电池发电。电池负极反应为 ( )
A.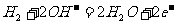 B.
B.
C.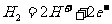 D.
D.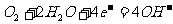
答案:C
击破考点二:电极反应和总反应的书写,常见化学电源
例2:镍氢电池是近年来开发出来的可充电电池,它可以取代会产生污染镉的镍镉电池,镍氢电池的总反应是: H2 + 2NiO(OH)=2Ni(OH)2,根据此反应式判断,下列叙述中正确的是 ( )
A.电池放电时, 电池负极周围溶液的PH值不断增大
B.电池放电时, 镍元素被氧化
C. 电池充电时,氢元素被还原
D. 电池放电时,H2是负极
答案:CD
[变式训练3]碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌锰碱性电池以氢氧化钾溶液为电解液, 电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是 ( )
A.电池工作时,锌失去电子
B.电池正极的电极反应式为: 2MnO2 + H2O(l) +2e- = Mn2O3(s) + 2OH-(aq)
C.电池工作时, 电子由正极通过外电路流向负极
D. 外电路中每通过度0.2mol电子,锌的质量理论上减小6.5g
答案:C
[变式训练4](1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应:_____________________________________;
银片上发生的电极反应:______________________________________。
(2)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:
 ①产生氢气的体积(标准状况);
①产生氢气的体积(标准状况);
②通过导线的电量。(已知NA = 6.02×1023 /mol,电子电荷为1.60×10-19 C)
答案:(1)Zn-2e- = Zn2+; 2H++2e- = H2↑。(2)①锌片与银片减轻,是因与酸反应:
Zn+2H+ = Zn2++H2↑ - 转移2e-
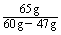 =
= 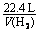 =
=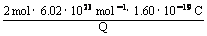
得V(H2) = 4.5 L; Q = 3.8×104 C
击破考点三:电解原理(能量转化,电极反应,活泼电极,惰性电极,浓度变化,恢复,PH变化等。)
例3:如图所示,下列叙述正确的是( )
A.Y为阴极,发生还原反应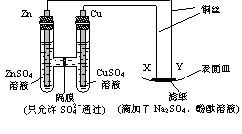
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X与滤纸接触处变红
答案:A
[变式训练5](2007年高考广东化学卷)三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成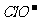 ,把二价镍氧化为三价镍。以下说法正确的是( )
,把二价镍氧化为三价镍。以下说法正确的是( )
A.可用铁作阳极材料
B.电解过程中阳极附近溶液的pH升高
C.阳极反应方程式为:2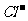 -2e-=Cl2
-2e-=Cl2
D.1 mol二价镍全部转化为三价镍时,外电路中通过了1 mol电子。
答案:CD
击破考点四:电解的有关计算(电解液浓度,电解后的PH,两极产物)
 例4:某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3︰1,用石墨电极电解该混合液。下列叙述不正确的是
例4:某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3︰1,用石墨电极电解该混合液。下列叙述不正确的是
A.阴极自始至终均析出H2 B.阳极先析出Cl2,后析出O2
C.电解最后阶段为电解水 D.溶液pH不断增大,最后为7
答案:D
[解析]电解质溶液中n(Na+):n(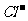 ):n(H+):n(
):n(H+):n(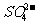 )=3:3:2:1,电解过程明显分为三个阶段:
)=3:3:2:1,电解过程明显分为三个阶段:
第一阶段相当于电解盐酸: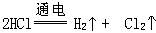
第二阶段相当于电解氯化钠溶液: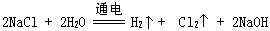
第三阶段相当于电解水: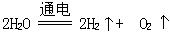
可见只有D不正确。
[变式训练7]在100mlH2SO4与CuSO4的混合液中,用石墨作电极电解一段时间,两极上均收集到2.24L气体(标准状况),则原溶液中Cu2+物质的量浓度为 ( )
A.1molL-1 B.2molL-1 C.3molL-1 D.4molL-1
答案:A
[变式训练8]蓄电池反应如下:负极:Pb+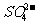 =PbSO4+2e-正极:PbO2+4H++
=PbSO4+2e-正极:PbO2+4H++ 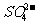 +2e=PbSO4+2H2O若用其电解饱和食盐水制Cl20.05mol电池内消耗H2SO4至少是
( )
+2e=PbSO4+2H2O若用其电解饱和食盐水制Cl20.05mol电池内消耗H2SO4至少是
( )
A. 0.025mol B. 0.05mol C. 0.1mol D. 0.2mol
答案:C
击破考点五:电解的运用(氯碱工业,电解精炼铜,电镀等)
例5:下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
D.电解精炼铜时,同一时间内阳极溶液铜的质量比阴极析出铜的质量小
答案:D
[变式训练9]下列描述中,不符合生产实际的是
A.电解熔融的氧化铝制取金属铝,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在镀件上电镀锌,用锌作阳极
答案:A
 [变式训练10](2007理综山东,电解饱和食盐水)工业上对海水资源综合开发利用的部分工艺流程如下图所示。
[变式训练10](2007理综山东,电解饱和食盐水)工业上对海水资源综合开发利用的部分工艺流程如下图所示。
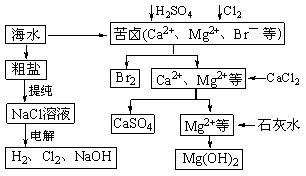
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽。离子膜和隔膜均允许通过的分子或离子是________。电解槽中的阳极材料为__________。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4顺序制备?_____原因是 。
(3)溴单质在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是______________________________________。
答案:(1)阴离子(Na+);钛(或石墨)。 (2)否。如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯
 (3)四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重
(3)四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重
击破考点六:金属腐蚀原理
例6.下列关于金属腐蚀的叙述正确的是 ( )
A.金属在潮湿情况下的腐蚀实质是M+nH2O====M(OH)n+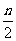 H2↑
H2↑
B.金属的化学腐蚀实质是M-ne- Mn+,电子直接转移给氧化剂
Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的中性环境中,金属的电化学腐蚀主要是吸氧腐蚀
答案:BD
解析:A项金属在潮湿情况下有可能进行析氢腐蚀,也有可能进行吸氧腐蚀,题目只给出了析氢腐蚀实质。C项中,金属铝的化学腐蚀可以在碱性条件下进行,故此选项错。
[变式训练11]下列叙述不正确的是 ( )
A.金属的电化学腐蚀比化学腐蚀更普通 B.钢铁在干燥空气里不易被腐蚀
C.用铝质铆钉铆接铁板,铝铆钉易被腐蚀 D.原电池中电子由正极流入负极
答案:C
解析:金属易发生电化学腐蚀,A正确。在干燥空气中钢铁难于形成电化学腐蚀,B正确。铝质铆钉易与铁板形成原电池两极,Fe作负极易发生腐蚀,C不正确。D正确。
[变式训练12]下列说法正确的是
( )
 A.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀
A.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀
B.原电池反应是导致金属腐蚀的主要原因,故不能用来减缓金属的腐蚀
C.钢铁电化学腐蚀的两种类型主要区别在于水膜的 pH不同,引起的正极反应?不同
D.无论哪种类型的腐蚀,其实质都是金属被氧化
答案:CD
解析:金属的腐蚀就是金属失电子而被氧化的过程,因此D是正确的。依据电化学腐蚀中析氢腐蚀和吸氧腐蚀的原理可知,C也是正确的。原电池反应既可以加快金属的腐蚀,也可用以防止金属的腐蚀。例如不锈钢,镀锌铁等中的Fe均不易腐蚀,所以A、B是不正确的
击破考点七:金属腐蚀快慢的比较
例7:取6根铁钉,6支干净的试管及其他材料,准备如下图
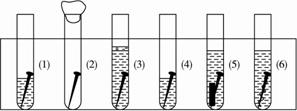
试管(1)放入一根铁钉,再注入蒸馏水,使铁钉和空气及水接触;
试管(2)的试管底放入硅胶(是一种干燥剂),再放入铁钉,用棉花团堵住试管口,使铁钉和干燥空气接触。
试管(3)先放入一根铁钉,趁热倒入煮沸的蒸馏水(赶出原先溶解在蒸馏水中的空气)浸没铁钉,再加上一层植物油,使铁钉不能跟空气接触。
试管(4)中放入铁钉注入食盐水,使铁钉和空气及食盐水接触。
试管(5)放入相连的铁钉和锌片,注入自来水,浸没铁钉和锌片。
试管(6)放入相连的铁钉和铜丝,注入自来水浸没铁钉和铜丝。
把6支试管放在试管架上,几天后观察铁钉被腐蚀的情况。其中 试管内的铁钉未被腐蚀。从铁钉被腐蚀的情况可知引起和促进铁钉腐蚀的条件是 。
答案:(2)(3)(5) 水、空气、电解质溶液、不活泼金属杂质的存在
解析:此题实际是利用原电池形成的条件及原理解释金属腐蚀速率问题。由于(2)(3)两个试管不具备构成原电池的条件,不能发生电化学腐蚀,所以暂未被腐蚀。而试管(5)尽管具备构成原电池的条件,但Zn比铁活泼,在原电池中作负极,使铁变成铁离子的反应难以发生,所以铁也暂未被腐蚀。引起和促进铁钉被腐蚀的条件是:水、空气、电解质溶液和不活泼金属杂质的存在。
 [变式训练13]如图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是
[变式训练13]如图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是

A.④>②>①>③ B.②>①>③>④ C.④>②>③>① D.③>②>④>① 答案:A
解析: 金属腐蚀的快慢判断方法:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防腐蚀措施的腐蚀;同一种金属腐蚀:强电解质>弱电解质>非电解质溶液。②、③实质均为原电池装置,④为电解池装置,Fe作阳极,腐蚀最快。③中Fe为正极,被保护;②中Fe为负极,被腐蚀,①中因铁不纯而发生微电池反应。
[变式训练14] 下列几种金属制品的镀层损坏后,金属腐蚀速率最快的是( )
A.镀铝塑料 B.食品罐头盒(镀锡)
C.白铁水桶(镀锌) D.镀银铜质奖章
答案:B
解析:B、C、D选项中的材料在损坏后,均能形成原电池。其中B中Fe作负极,C中Zn作负极,D中Cu作负极,所以B、C中金属腐蚀加快,其中Fe腐蚀更快
击破考点八:金属的防护
例8:为防止海轮船体的腐蚀,应在船体水线以下位置嵌上一定数量的( )
A.铜块 B.铅块
C.锌块 D.钠块
答案:C
解析:海轮船体由钢板焊接而成,为防止浸埋在海水(电解质溶液)中的船体(Fe)的腐蚀,应选用活泼性比铁强,而又不会与水直接反应的金属Zn嵌入船体,这样紧密接触的两种金属接触海水(电解质溶液)时,将发生原电池反应,较活泼的Zn作为原电池的负极,Zn失去电子被氧化,Zn失去的电子流向Fe,从而抑制Fe失去电子被氧化。定期更换嵌入的Zn块,就起到了防止船体被腐蚀的目的。
[变式训练15 ]为保护地下钢管不受腐蚀,可采取的措施有 ( )
A.与石墨棒相连 B.与直流电源负极连接
C.与直流电源正极连接 D.与锌板相连
答案:BD
解析:本题考查金属腐蚀的一种防护方法--电化学保护法。该法的依据一:牺牲阳极的阴极保护法;依据二:外加电流的阴极保护法。
 [变式训练16]下列金属防护的方法不正确的是
( )
[变式训练16]下列金属防护的方法不正确的是
( )
A.对健身器材涂油漆以防止生锈
B.对某些工具的“机械转动部位”选用刷油漆的方法来防锈
C.用牺牲锌块的方法来保护船身
D.自行车的钢圈上镀上一层铬防锈
答案:B
解析:机械转动部位应涂油脂防锈,油脂既防水又能防止气体对金属的腐蚀,还能使转动部位灵活。
击破考点九: 金属腐蚀的电极反应方程式的书写
例9:钢铁在很弱的酸性或中性条件下发生电化学腐蚀时,正极的反应式为 ( )
A.Fe-2e- Fe2+
B.2H++2e-
Fe2+
B.2H++2e- H2↑
H2↑
C.
 4
4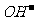 D.Fe-3e-
D.Fe-3e- Fe3+
Fe3+
答案:C
解析:钢铁中含有多种杂质,在考虑钢铁的电化学腐蚀时,为了简化问题,主要讨论碳杂质问题。也就是以Fe为负极,C为正极的原电池反应。在中性条件或弱酸性条件下发生的是吸氧腐蚀。原电池的正极为C,发生的是还原反应,即得电子反应,故A、D选项应排除。在B、C选项中,B项是析氢腐蚀的电极反应式。
[变式训练17]如右图所示,水槽中试管内有一枚铁钉,放置数天后观察:
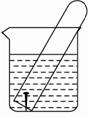
(1)铁钉在逐渐生锈,则铁钉的腐蚀属于 腐蚀。
(2)若试管内液面上升,则原溶液是 性,发生 腐蚀,电极反应:负极: ,正极: 。
(3)若试管内液面下降,则原溶液呈 性,发生 腐蚀,电极反应:负极: ,正极: 。
答案:(1)电化学
(2)弱酸性或中 吸氧 2Fe-4e- 2Fe2+ O2+4e-+2H2O
2Fe2+ O2+4e-+2H2O 4OH-
4OH-
(3)较强的酸 析氢 Fe-2e- Fe2+ 2H++2e-
Fe2+ 2H++2e- H2↑
H2↑
 解析:根据原电池的构成条件,两种不同的材料在有电解质溶液时,若形成闭合回路,即可构成原电池,此时发生的腐蚀属于电化学腐蚀。根据金属腐蚀的条件、原理及结果可知:试管内液面上升,说明试管内压强减小,气体被吸收所致,是铁钉吸氧腐蚀的结果,据此写出电极反应;试管内液面下降,说明试管内气体压强变大,试管内产生了新气体所致,是铁钉的析氢腐蚀的结果,据此写出电极反应。
解析:根据原电池的构成条件,两种不同的材料在有电解质溶液时,若形成闭合回路,即可构成原电池,此时发生的腐蚀属于电化学腐蚀。根据金属腐蚀的条件、原理及结果可知:试管内液面上升,说明试管内压强减小,气体被吸收所致,是铁钉吸氧腐蚀的结果,据此写出电极反应;试管内液面下降,说明试管内气体压强变大,试管内产生了新气体所致,是铁钉的析氢腐蚀的结果,据此写出电极反应。
[变式训练18] 如右图所示,试管中放一铁钉,溶液为氯化钠溶液,数天后观察到的现象有______________。说明铁钉发生了_______________腐蚀,其中正极的电极反应式为__________________,溶液中发生反应的化学方程式为______________
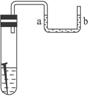
答案:a端液面上升,b端液面下降,铁钉表面有红棕色铁锈生成 吸氧 O2+2H2O+4e-====4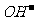 2Fe+O2+2H2O====2Fe(OH)2,4Fe(OH)2+O2+2H2O====4Fe(OH)3
2Fe+O2+2H2O====2Fe(OH)2,4Fe(OH)2+O2+2H2O====4Fe(OH)3
解析:铁钉在NaCl溶液中发生了吸氧腐蚀,使装置中O2减少,气体压强减小,使a端液面上升,b端液面下降。其中Fe作负极,发生反应为:Fe-2e-====Fe2+;正极发生反应为:O2+2H2O+4e-====4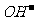 。
。
3

1.吸氧腐蚀和析氢腐蚀的区别
|
电化腐蚀类型 |
吸氧腐蚀 |
析氢腐蚀 |
|
条件 |
水膜酸性很弱或呈中性 |
水膜酸性较强 |
|
正极反应 |
O2 + 4e- + 2H2O == 4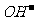 |
2H+ + 2e-==H2↑ |
|
负极反应 |
Fe -2e-==Fe2+ |
Fe -2e-==Fe2+ |
|
总反应方程式 |
4Fe(OH)2+O2+2H2O==4Fe(OH)3 2Fe(OH)3==Fe2O3+3H2O |
Fe + 2H+ = Fe2+
+ H2↑ |
|
腐蚀作用 |
是主要的腐蚀类型,具有广泛性 |
发生在某些局部区域内 |
2.电解原理的应用
(1)电解精炼铜:粗铜作阳极,精铜作阴极,CuSO4溶液作电解质溶液。电解时,发生如下反应:阳极,Cu-2e-=Cu2+,阴极,Cu2++2e-=Cu。阳极泥中存在金、银等不活泼的贵重金属,阴极得到纯铜。
(2)电镀铜:精铜作阳极,镀件金属作阴极,硫酸铜(或其他可溶性铜盐)溶液作电解质溶液,从理论上讲电镀时电解质溶液组成、浓度和质量不变化。电极反应:阳极Cu-2e-=Cu2+,阴极Cu2++2e-=Cu
(3)氯碱工业:阳极2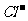 -2e-=Cl2↑, 阴极2H++2e-=H2↑总反应2NaCl+2H2O
-2e-=Cl2↑, 阴极2H++2e-=H2↑总反应2NaCl+2H2O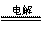 2NaOH+H2↑+Cl2↑(反应条件:直流电)
2NaOH+H2↑+Cl2↑(反应条件:直流电)
(4)冶炼金属:电解熔融电解质,可炼得活泼金属。如:K、Na、Ca、Mg、Al等金属可通过电解其熔融的氯化物或氧化物制得。电源的负极是最强的“还原剂”,可“强迫”活泼金属的阳离子得电子。如电解冶炼铝:阳极反应6O2--12e-=3O2↑,阴极反应4Al3++12e-=4Al,总反应式为:2Al2O3 4Al+3O2↑。
4Al+3O2↑。
[重点提醒]
(1)电化学计算的基本方法
 原电池和电解池的计算包括两极产物的定量计算、溶液pH的计算、相对原子质量和阿伏加德罗常数测定的计算、根据电荷量求产物的量与根据产物的量求电荷量等的计算。不论哪类计算,均可概括为下列三种方法:
原电池和电解池的计算包括两极产物的定量计算、溶液pH的计算、相对原子质量和阿伏加德罗常数测定的计算、根据电荷量求产物的量与根据产物的量求电荷量等的计算。不论哪类计算,均可概括为下列三种方法:
①根据电子守恒法计算:用于串联电路、阴阳两极产物、正负两极产物、相同电荷量等类型的计算,其依据是电路中转移的电子数相等。
②根据总反应式计算:先写出电极反应式,再写出总反应式,最后根据总反应式列比例式计算。
③根据关系式计算:借得失电子守恒关系建立已知量与未知量之间的桥梁,建立计算所需的关系式。
(2)电化学试题的命题点归纳
①二次电池的充电和放电:放电时原电池,充电时电解池;
②电极名称:原电池的电极名称是正和负极,电解池是阳极和阴极;
③反应类型:负极和阳极发生氧化反应,失电子被氧化,正极和阴极发生还原反应,得电子被氧化;
 ④电极反应:负极的反向是阴极,正极的反向是阳极。酸性电池中不能出现OH-,碱性电池中不能出现H+,非溶液电池不会出现H+和
④电极反应:负极的反向是阴极,正极的反向是阳极。酸性电池中不能出现OH-,碱性电池中不能出现H+,非溶液电池不会出现H+和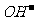 ;
;
⑤溶液和电极附近溶液酸碱性变化:总反应消耗酸(碱),溶液PH增大(减小)。电极反应式中H+(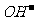 )放电云集
)放电云集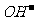 (H+),电极溶液显碱性(酸性)。电极反应消耗H+(
(H+),电极溶液显碱性(酸性)。电极反应消耗H+(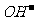 ),酸性(碱性)减弱,生成H+(
),酸性(碱性)减弱,生成H+(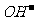 ),酸性(碱性)增强。
),酸性(碱性)增强。
⑥浓度复原:消耗什么补充什么,消耗多少补多少
电解池是将电能转化为化学能的装置,在电解池中,阳极发生氧化反应、阴极发生还原反应,其放电顺序一般为:阳极:活泼性电极>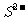 >
>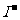 >
>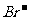 >
>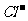 >
>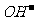 >含氧酸根离子阴极:与金属活动顺序表中金属阳离子的氧化顺序一致
>含氧酸根离子阴极:与金属活动顺序表中金属阳离子的氧化顺序一致
1.(惰性电极)电解电解质溶液的类型
|
类型 |
实例 |
电极反应特点 |
电解对象 |
电解质浓度 |
pH |
溶液复原 |
|
电解水 |
NaOH |
阴:2H++2e-====H2↑ 阳:4 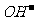 -4e-====2H2O+O2↑ -4e-====2H2O+O2↑ |
水 |
增大 |
增大 |
水 |
|
H2SO4 |
水 |
增大 |
减小 |
水 |
||
|
Na2SO4 |
水 |
增大 |
不变 |
水 |
||
|
电解电解质 |
HCl |
电解质电离出的阴阳离子分别在两极放电 |
电解质 |
减小 |
增大 |
氯化氢 |
|
CuCl2 |
电解质 |
减小 |
- |
氯化铜 |
||
|
放H2生碱 |
NaCl |
阴极:H2O放H2生碱阳极: 电解质阴离子放电 |
电解质 和水 |
生成新电解质 |
增大 |
 氯化氢 氯化氢 |
|
放O2生酸 |
CuSO4 |
阴极:电解质阳离子放电 阳极:H2O放O2生酸 |
电解质 和水 |
生成新电解质 |
减小 |
氧化铜 |
3.原电池原理的应用
(1)利用原电池原理可以制造出各种实用电池,即化学电源,如锌锰干电池、铅蓄电池、锂电池、新型燃料电池等。
(2)原电池原理可用于解决一些实际问题,如加快某些化学反应时的速率(稀硫酸与锌反应时,常滴入几滴硫酸铜溶液);分析金属电化学腐蚀的快慢和防护方法等。
[重点提醒]
(1)由电极装置书写电极反应:找出发生氧化反应和还原反应的物质(或离子),确定正负或阴阳极反应的物质(或放电的离子),利用电荷守恒分别写出电极反应式。
 (2)差值法书写电极反应式:正负(或阴阳)极反应式之和为电池反应的方程式。一般先写出反应的总方程式和较易写出的电极反应式,然后用总方程式减去较易写出的电极反应式得较难写的电极反应式。书写时,无论是总反应式还是电极反应式都既要满足电子转移守恒、电荷守恒,又要满足质量守恒。书写时注意介质通常是定向移动到该电极附近的导电离子如H+、OH-、H2O等等,若氧化(或还原)产物能与之发生复分解反应,则其一般书写在电极方程式中
(2)差值法书写电极反应式:正负(或阴阳)极反应式之和为电池反应的方程式。一般先写出反应的总方程式和较易写出的电极反应式,然后用总方程式减去较易写出的电极反应式得较难写的电极反应式。书写时,无论是总反应式还是电极反应式都既要满足电子转移守恒、电荷守恒,又要满足质量守恒。书写时注意介质通常是定向移动到该电极附近的导电离子如H+、OH-、H2O等等,若氧化(或还原)产物能与之发生复分解反应,则其一般书写在电极方程式中
(3)常见电极反应式
(a)氢、氧燃烧电池(电池的产物负极为H2O,正极则有大量的氢氧根生成):
负极: 正极:
正极: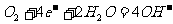
(b)甲烷燃烧电池(电池负极甲烷燃烧失去电子,在碱性条件下生成的CO2与OH-反应生成CO32-和H2O, 而正极是 O2得到电子而成为OH-。)
负极: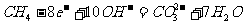 正极:
正极: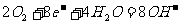
(c)爱迪生蓄电池: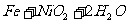

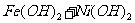
负极: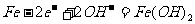
 正极:
正极: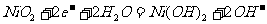
(d)纽扣电池:
负极: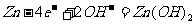 正极:
正极: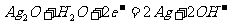
(e)铅蓄电池
负极: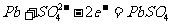
正极:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com