
9. A,X、Y获得两个电子就达到稳定结构,故它们属于VIA族,由于X得到电子放出的热量多,故X形成的离子更稳定,即X的非金属性比Y强;Z、W失去一个电子达到稳定结构,它们属于IA族,W失去电子吸收的能量多,则W比Z难失电子,故金属性Z大于W。形成离子化合物最可能是金属性强的与非金属性强的元素化合,即Z2X。
8. D,由题可知: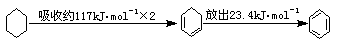 ,因为苯的能量比环己二烯能量低,故苯比环己二烯稳定,故C错;环己二烯加氢是放热过程,A错;苯加氢到环己烷由上图可知是放热过程,B错。
,因为苯的能量比环己二烯能量低,故苯比环己二烯稳定,故C错;环己二烯加氢是放热过程,A错;苯加氢到环己烷由上图可知是放热过程,B错。
7. D,题目中给出的数据意义是:燃烧1g的甲烷放出55.625kJ的热量,应该换算成燃烧1mol甲烷放出的热量为890kJ。热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ·mol-1其他系数与热量相对应的方程式均正确。
D,题目中给出的数据意义是:燃烧1g的甲烷放出55.625kJ的热量,应该换算成燃烧1mol甲烷放出的热量为890kJ。热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ·mol-1其他系数与热量相对应的方程式均正确。
6. C,依据反应热的概念,表示按照方程式系数的物质的量反应时吸收或放出的热量,单位是kJ·mol-1,该方程式表示:1mol碳和1mol水蒸气反应生成1mol一氧化碳气体和1mol氢气,并吸收131.3kJ的热量。特别要指明水的状态。
13.下图所示的装置:
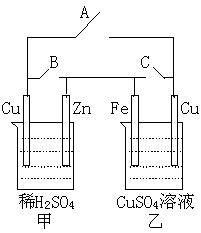
(1)当A键断开,B、C两键闭合时,甲为__________池,乙为__________池。甲池中各电极反应式为______________________________、______________________________。
(2)将乙中两极都换成石墨,硫酸铜溶液换成稀硫酸。断开B、C两键,闭合A键,甲为__________池,乙为__________池。当甲中锌减轻时,乙中共放出气体(标准状况)_______________ml。
答案:1.A 2.C 3.C 4.A 5.C
12. 从H+、Cu2+、Na+、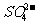 、
、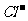 五种离子中恰当地组成电解质,按下列要求进行电解:
五种离子中恰当地组成电解质,按下列要求进行电解:
(1)以石墨为电极,使电解质质量减少,水量不变进行电解,则采用的电解质是__________。
(2)以石墨为电极,使电解质质量不变,水量减少进行电解,则采用的电解质是__________。
(3)以石墨为阳极,铁棒为阴极,使电解质和水质量都减少进行电解,则采用的电解质是__________。
11. 金属腐蚀的本质是__________________________________________。切完咸菜的刀生锈时,发生的是___________腐蚀,此时为______负极,电极反应为______________________,__________为正极,电极反应为____________________________。
金属腐蚀的本质是__________________________________________。切完咸菜的刀生锈时,发生的是___________腐蚀,此时为______负极,电极反应为______________________,__________为正极,电极反应为____________________________。
10. 用石墨作电极,电解1L0.1mol/LCuSO4溶液,电解一段时间后,CuSO4浓度会减少。为了恢复电解液仍为1L0.1mol/L(假定电解过程中,水份无蒸发损失),应向溶液中加入
A.Cu(OH)2 B.无水CuSO4 C.CuCO3 D. CuO
9. 某电解池内盛有硫酸铜溶液,插入两根电极,接通直流电源,欲达到如下要求:①阳极质量不变,②阴极质量增加,③电解液pH减小,则应选用的电极是
A.阴阳两极都是石墨 B.铜作阳极,铁做阴极。
C.铁作阳极,铜做阴极。 D.铂作阳极,铜做阴极。
8. 某电解质溶液pH=a,向其中插入两根惰性电极通电一段时间后再测知溶液的pH=b,若b≤a,该电解质可能是
A.Na2S B.CuSO4 C.NaCl D.Na2SO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com