
6.下列叙述正确的是
 A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
答案:C
6. 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2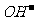 =Zn(OH)2
=Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3-3e-+5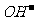 =
=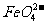 +4H2O
+4H2O
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
答案:C
4.通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银)∶n(硝酸亚汞)=2∶1,则下列表述正确的是 ( )
A.在两个阴极上得到的银和汞的物质的量之比为1∶1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的分子式为HgNO3
D.硝酸亚汞的分子式为Hg2(NO3)2
答案:D
3.在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )

A.碳棒上有气体放出,溶液pH变大
B.a是正极,b是负极
C.导线中有电子流动,外电路中,电流从a极到b极
D.a极上发生了氧化反应
答案:A
2.在理论上可用于设计原电池的化学反应是( )
A.2Al(s)十2NaOH(aq)+2H2O(1)=2NaAlO2(aq)+3H2(g);△H <O
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(aq)+8H2O(1);△H >0
C.CaC2(s)+2H2O(1)→Ca(OH)2(s)+C2H2(g);△H <0
D.FeCl3(aq)十3H2O(1) Fe(OH)3(s)+3HCl(aq);△H >0
Fe(OH)3(s)+3HCl(aq);△H >0
答案:A
1. 下列关于铜电极的叙述,正确的是( )
下列关于铜电极的叙述,正确的是( )
A.铜锌原电池中铜是正极
B.用电解法精炼粗铜时铜作阳极
C.在镀件上电镀铜时可用金属铜作阳极
D.电解稀硫酸制H2、O2时铜作阳极
 答案:A
答案:A
13. AC ,A错。在放热反应中有一些需加热以提供必需的能量来引发反应,如煤的燃烧。C错在有些吸热反应并不需要加热,如Ba(OH)2晶体与NH4Cl的反应,HAc的电离等吸热过程,均不需要加热

12. D因为稀醋酸是弱电解质,在电离时吸热,浓H2SO4溶于水时放热。故中和时放出的热量Q(H2SO4)>Q(HNO3)>Q(HAc),又因放热反应中,△H为负值,即△H=-Q,故△H2<△H3<△H1。
11. C,在100gC中有 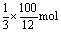 变为CO,有
变为CO,有 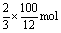 变为CO2,故与C完全燃烧相比,损失的热量就是CO继续燃烧放出的热量,依据热化学方程式,知损失的热量为
变为CO2,故与C完全燃烧相比,损失的热量就是CO继续燃烧放出的热量,依据热化学方程式,知损失的热量为 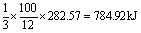

10. C,反应放出或吸收的热量的多少,跟反应物和生成物的聚集状态有密切关系。A中两式仅生成物中水的状态不同,由于生成液态水比生成气态水放热多,所以Q1>Q2;B中两式仅硫的状态不同,由于固态硫变成气态硫要吸收热量,所以Q1>Q2;C中固态碳与氧气完全反应生成二氧化碳,放出的热量Q2应大于不完全燃烧时生成一氧化碳放出的热量Q1;D中二式各物质的量不同,有Q1=2Q2的关系,故本题的答案应为C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com