
(1)КІГҙКЗЦРРД¶ФіЖНјРО?
(2)ОТГЗІЙУГКІГҙ·Ҫ·ЁСРҫҝЦРРД¶ФіЖНјРО?
22Ј®(16·Ц)(2009ЎӨ°ІЗмДЈДв)ДіҝОНв»о¶ҜРЎЧйН¬С§УГИзНјЧ°ЦГҪшРРКөСйЈ¬КФ»ШҙрПВБРОКМвЈә
(1)ИфҝӘКјКұҝӘ№ШKУлaБ¬ҪУЈ¬ФтBј«өДөзј«·ҙУҰКҪОӘ
________________________________________________________________________
________________________________________________________________________ЎЈ
(2)ИфҝӘКјКұҝӘ№ШKУлbБ¬ҪУЈ¬ФтBј«өДөзј«·ҙУҰКҪОӘ________________________________________________________________________Ј¬
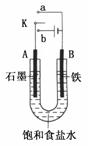
ЧЬ·ҙУҰөДАлЧУ·ҪіМКҪОӘ_____________________________________ЎЈ
УР№ШЙПКцКөСйЈ¬ПВБРЛө·ЁХэИ·өДКЗ(МоРтәЕ)________ЎЈ
ўЩИЬТәЦРNa+ПтAј«ТЖ¶Ҝ
ўЪҙУAј«ҙҰТЭіцөДЖшМеДЬК№КӘИуKIөн·ЫКФЦҪұдА¶
ўЫ·ҙУҰТ»¶ОКұјдәујУККБҝСОЛбҝЙ»ЦёҙөҪөзҪвЗ°өзҪвЦКөДЕЁ¶И
ўЬИфұкЧјЧҙҝцПВBј«ІъЙъ2.24 LЖшМеЈ¬ФтИЬТәЦРЧӘТЖ0.2 molөзЧУ
(3)ёГРЎЧйН¬С§ДЈДв№ӨТөЙПУГАлЧУҪ»»»ДӨ·ЁЦЖЙХјоөД·Ҫ·ЁЈ¬ДЗГҙҝЙТФЙиПлУГИзНјЧ°ЦГөзҪвБтЛбјШИЬТәАҙЦЖИЎЗвЖшЎўСхЖшЎўБтЛбәНЗвСх»ҜјШЎЈ
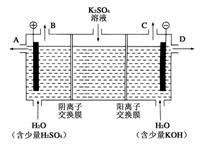
ўЩёГөзҪвІЫөДСфј«·ҙУҰКҪОӘ___________________________________________ЎЈ
ҙЛКұНЁ№эТхАлЧУҪ»»»ДӨөДАлЧУКэ________(МоЎ°ҙуУЪЎұЎўЎ°РЎУЪЎұ»тЎ°өИУЪЎұ)НЁ№эСфАлЧУҪ»»»ДӨөДАлЧУКэЎЈ
ўЪНЁөзҝӘКјәуЈ¬Тхј«ёҪҪьИЬТәpH»бФцҙуЈ¬ЗлјтКцФӯТт____________________________
________________________________________________________________________ЎЈ
ўЫИфҪ«ЦЖөГөДЗвЖшЎўСхЖшәНЗвСх»ҜјШИЬТәЧйәПОӘЗвСхИјБПөзіШЈ¬ФтөзіШХэј«өДөзј«·ҙУҰКҪОӘ________________________________________________________________________
____________________________________ ____________________________________ЎЈ
____________________________________ЎЈ
ҪвОц Јә(1)KУлaБ¬ҪУЈ¬ФтКЗДЈДвМъОьСхёҜКҙөДФӯөзіШЧ°ЦГЎЈ
Јә(1)KУлaБ¬ҪУЈ¬ФтКЗДЈДвМъОьСхёҜКҙөДФӯөзіШЧ°ЦГЎЈ
(2)KУлbБ¬ҪУЈ¬ФтКЗөзҪвұҘәНКіСОЛ®өДЧ°ЦГЎЈ
(3)Сфј«ЙПOHЈӯК§ИҘөзЧУКэДҝУлТхј«ЙПH+өГөҪөзЧУКэДҝПаөИК№БҪИЬТәРОіЙөДH+әНOHЈӯКэДҝПаөИЈ¬№КҪшИлЧуІаИЬТәЦРөДSOЙЩУЪҪшИлУТІаИЬТәЦРөДK+ЎЈ
ҙр°ёЈә(1)FeЈӯ2eЈӯ===Fe2+
(2)2H++2eЈӯ===H2Ўь
2ClЈӯ+2H2O2OHЈӯ+H2Ўь+Cl2Ўь
ўЪ
(3)ўЩ4OHЈӯЈӯ4eЈӯ===2H2O+O2ЎьЎЎРЎУЪ
ўЪH+·ЕөзЈ¬ҙЩҪшЛ®өДөзАлЈ¬OHЈӯЕЁ¶ИФцҙу
ўЫO2+2H2O+4eЈӯ===4OHЈӯ
21Ј®(12·Ц)(2009ЎӨОЯәюДЈДв)ИзНјЛщКҫҪУНЁПЯВ·Ј¬·ҙУҰТ» ¶ОКұјдә󣬻ШҙрПВБРОКМв(јЩЙиЛщМṩөДөзДЬҝЙТФұЈЦӨөзҪв·ҙУҰөДЛіАыҪшРР)Јә
¶ОКұјдә󣬻ШҙрПВБРОКМв(јЩЙиЛщМṩөДөзДЬҝЙТФұЈЦӨөзҪв·ҙУҰөДЛіАыҪшРР)Јә
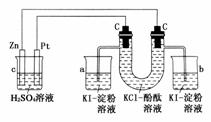
(1)UРО№ЬҝЙ№ЫІмөҪ________Ј¬РҙіцУР№Ш·ҙУҰөД»ҜС§·ҪіМКҪ
________________________________________________________________________ЎЈ
(2)ФЪРЎЙХұӯaЎўbЦР·ЦұрУРКІГҙПЦПуІъЙъ
________________________________________________________________________ЎЈ
(3)Из№ыРЎЙХұӯЦРУР0.508 gөвОціцЈ¬ФтЙХұӯcЦРёәј«өДЦКБҝјхЗб________ҝЛЎЈ
ҪвОцЈәУЙНјКҫҝЙЦӘЧуіШОӘФӯөзіШЈ¬ZnОӘёәј«Ј¬PtОӘХэј«Ј»УТіШОӘөзҪвіШЈ¬UРО№ЬЧуөзј«ОӘСфј«Ј¬УТөзј«ОӘТхј«Ј¬өзҪв·ҙУҰКҪОӘЈә2KCl+2H2OCl2Ўь+H2Ўь+2KOHЈ¬Сфј«·ҙУҰКҪОӘЈә2ClЈӯЈӯ2eЈӯ===Cl2Ј¬Тхј«·ҙУҰКҪОӘЈә2H++2eЈӯ===H2ЎьЎЈ№КФЪaЙХұӯЦР·ўЙъ·ҙУҰCl2+2KI===I2+2KClЈ¬өн·ЫИЬТәұдА¶Й«Ј¬bЙХұӯЦРИЬТәСХЙ«І»ұдЎЈөұУР0.508 gјҙ0.002 mol I2ОціцКұЈ¬Ри0.002 mol Cl2Ј¬ФтөзВ·ЦРЧӘТЖөзЧУОӘ0.004 molЈ¬¶шЙХұӯcЦРёәј«·ҙУҰОӘZnЈӯ2eЈӯ===Zn2+Ј¬№КРиПыәДZn 0.002 molЈ¬јҙ0.13 gЎЈ
ҙр°ёЈә(1)БҪј«ЙПҫщУРЖшМеІъЙъЈ¬UРО№ЬУТұЯ·УМӘИЬТәұдәмЈ¬ЖшМе·ЦұрөјИлaЎўbБҪЦ»РЎЙХұӯЦР
2KCl+2H2O2KOH+H2Ўь+Cl2Ўь
(2)aЙХұӯЦРУРЖшЕЭЈ¬ИЬТәПФА¶Й«Ј¬bЙХұӯЦРУРЖшЕЭЈ¬ИЬТәСХЙ«І»ұдЎЎ(3)0.13
20Ј®(12·Ц)(2009ЎӨРмЦЭДЈДв)јЧИ©КЗТ»ЦЦЦШТӘөД»Ҝ№ӨІъЖ·Ј¬ҝЙАыУГјЧҙјҙЯ»ҜНСЗвЦЖұёЎЈјЧИ©УлЖшМ¬јЧҙјЧӘ»ҜөДДЬБҝ№ШПөИзНјЛщКҫЎЈ
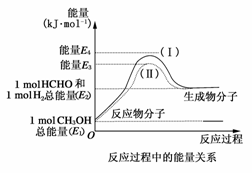
(1)јЧҙјҙЯ»ҜНСЗвЧӘ»ҜОӘјЧИ©өД·ҙУҰКЗ________(МоЎ°ОьИИЎұ»тЎ°·ЕИИЎұ)·ҙ УҰЎЈ
УҰЎЈ
(2)№эіМўсУл№эіМўтөД·ҙУҰИИКЗ·сПаН¬Јҝ________Ј¬ФӯТтКЗ_______________________ЎЈ
(3)РҙіцјЧҙјҙЯ»ҜНСЗвЧӘ»ҜОӘјЧИ©өДИИ»ҜС§·ҙУҰ·ҪіМКҪ___________________________ЎЈ
(4)јЧҙјҙЯ»ҜНСЗвЧӘ»ҜОӘјЧИ©өД№эіМЦРЈ¬Из№ыТӘК№·ҙУҰОВ¶ИО¬іЦФЪ700ЎжЈ¬РиПтМеПөЦРНЁИлҝХЖшЈ¬ФтҪшБПјЧҙјУлҝХЖшөДОпЦКөДБҝАнВЫұИЦөОӘ________[јЩЙиЈәH2(g)+O2(g)H2O(g)Ј»ҰӨHЈҪЈӯa kJЎӨmolЈӯ1Ј¬ҝХЖшЦРСхЖшМе»э·ЦКэОӘ0.2]ЎЈ
ҙр°ёЈә(1)ОьИИЎЎ(2)ПаН¬ЎЎТ»ёц»ҜС§·ҙУҰөД·ҙУҰИИҪцУл·ҙУҰөДЖрКјЧҙМ¬әН·ҙУҰөДЧоЦХЧҙМ¬УР№ШЈ¬¶шУл·ҙУҰөДНҫҫ¶ОЮ№Ш
(3)CH3OH(g)HCHO(g)+H2(g)Ј»ҰӨHЈҪ(E2ЈӯE1)kJЎӨmolЈӯ1
(4)
19Ј®(6·Ц)(2008ЎӨҪӯЛХДПНЁ5ФВ)Л®ГәЖш(ЦчТӘіЙ·ЦЈәCOЎўH2)КЗЦШТӘИјБПәН»Ҝ№ӨФӯБПЈ¬ҝЙУГЛ®ХфЖшНЁ№эігИИөДМјІгЦЖөГЎЈТСЦӘЈә
ўЩC(s)+H2O(g)CO(g)+H2(g)Ј»ҰӨHЈҪ+131.3 kJЎӨmolЈӯ1
ўЪC(s)+O2(g)===CO(g)Ј»ҰӨHЈҪЈӯ110.5 kJЎӨmolЈӯ1
ўЫCO(g)+O2(g)===CO2(g)Ј»ҰӨHЈҪЈӯ283.0 kJ ЎӨmolЈӯ1
ЎӨmolЈӯ1
ўЬH2(g)+O2(g)===H2O(g)Ј»ҰӨHЈҪЈӯ241.8 kJЎӨmolЈӯ1
ўЭH2(g)+O2(g)===H2O(l)Ј»ҰӨHЈҪЈӯ285.8 kJЎӨmolЈӯ1
(1)Ҫ«2.4 gМјЧӘ»ҜОӘЛ®ГәЖшЈ¬ФЩНкИ«ИјЙХЈ¬Хыёц№эіМ өДҰӨHЈҪ________kJЎӨmolЈӯ1ЎЈ
өДҰӨHЈҪ________kJЎӨmolЈӯ1ЎЈ
(2)УЙCOЎўH2ФЪТ»¶ЁМхјюПВ»сөГЖыУНөДМжҙъЖ·--јЧҙјЈ¬јЧҙјөДИјЙХИИОӘЈӯ726.5 kJЎӨmolЈӯ1Ј¬КФРҙіцУЙCOЎўH2ЙъіЙјЧҙјөДИИ»ҜС§·ҪіМКҪ______________________________________ЎЈ
ҪвОцЈә(1)УЙёЗЛ№¶ЁВЙҝЙөГўЪ+ўЫ⇒C(s)+O2(g)===CO2(g)Ј»ҰӨHЈҪЈӯ393.5 kJЎӨmolЈӯ1Ј¬ЛщТФ0.2 molCНкИ«ИјЙХҰӨHЈҪЈӯ78.7 kJЎӨmolЈӯ1ЎЈ
(2)CO(g)+2H2(g)===CH3OH(l)Ј»ҰӨH1
 CH3OH(l)+O2(g)ЁDЎъCO2(g)+2H2O(l)Ј»
CH3OH(l)+O2(g)ЁDЎъCO2(g)+2H2O(l)Ј»
ҰӨHЈҪЈӯ726.5 kJЎӨmolЈӯ1(ИјЙХИИЛ®ОӘТәМ¬)
УЙёЗЛ№¶ЁВЙҝЙөГҰӨH1ЈҪ[Јӯ283.0+(Јӯ285.8)ЎБ2Јӯ(Јӯ726.5)]kJЎӨmolЈӯ1ЈҪЈӯ128.1 kJЎӨmolЈӯ1
ҙр°ёЈә(1)Јӯ78.7
(2)CO(g)+2H2O(g)===CH3OH(l)Ј»ҰӨHЈҪЈӯ128.1 kJЎӨmolЈӯ1
18Ј®(2009ЎӨёЈҪЁАнЧЫ)ҝШЦЖККәПөДМхјюЈ¬Ҫ«·ҙУҰ2Fe3++2IЈӯ2Fe2++I2ЙијЖіЙИзПВНјЛщКҫөДФӯөзіШЎЈПВБРЕР¶ПІ»ХэИ·өДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (ЎЎ)
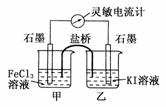
AЈ®·ҙУҰҝӘКјКұЈ¬ТТЦРКҜД«өзј«ЙП·ўЙъСх»Ҝ·ҙУҰ
BЈ®·ҙУҰҝӘКјКұЈ¬јЧЦРКҜД«өзј«ЙПFe3+ұ»»№Фӯ
CЈ®өзБчјЖ¶БКэОӘБгКұЈ¬·ҙУҰҙпөҪ»ҜС§ЖҪәвЧҙМ¬
DЈ®өзБчјЖ¶БКэОӘБгәуЈ¬ФЪјЧЦРИЬИлFeCl2№ММеЈ¬ТТЦРөДКҜД«өзј«ОӘёәј«
ҪвОцЈәУЙ·ҙУҰ2Fe3++2IЈӯ2Fe2++I2ҝЙЦӘЈ¬·ҙУҰҝӘКјКұјЧЦРFe3+·ўЙъ»№Фӯ·ҙУҰЈ¬ТТЦРIЈӯ·ўЙъСх»Ҝ·ҙУҰЈ»өзБчјЖ¶БКэОӘБгЈ¬ЛөГчөҘО»КұјдДЪУЙјЧБчПтТТөДөзЧУКэУлУЙТТБчПтјЧөДөзЧУКэПаөИЈ¬ЙъіЙFe3+өДОпЦКөДБҝУлПыәДөДFe3+ПаөИЈ¬Фт·ҙУҰҙпөҪБЛЖҪәвЧҙМ¬Ј¬ҙЛКұФЪјЧЦРИЬИлFeCl 2№ММеЈ¬ФтЖҪәвПтДж·ҙУҰ·ҪПтТЖ¶ҜЈ¬ТТЦРI2·ўЙъ»№Фӯ·ҙУҰЈ¬ФтТТЦРКҜД«өзј«ОӘХэј«Ј»№КСЎDЎЈ
2№ММеЈ¬ФтЖҪәвПтДж·ҙУҰ·ҪПтТЖ¶ҜЈ¬ТТЦРI2·ўЙъ»№Фӯ·ҙУҰЈ¬ФтТТЦРКҜД«өзј«ОӘХэј«Ј»№КСЎDЎЈ
ҙр°ёЈәD
өЪўтҫн(·ЗСЎФсМвЈ¬№І46·Ц)
17Ј®(2009ЎӨЙПәЈөҘҝЖ)НјЧ°ЦГЦРЈ¬UРН№ЬДЪОӘәмД«Л®Ј¬aЎўbКФ№ЬДЪ·ЦұрКўУРКіСОЛ®әНВИ»Ҝп§ИЬТәЈ¬ёчјУИлЙъМъҝйЈ¬·ЕЦГТ»¶ОКұјдЎЈПВБРУР№ШГиКцҙнОуөДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (ЎЎ)
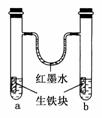
AЈ®ЙъМъҝйЦРөДМјКЗФӯөзіШөДХэј«
BЈ®әмД«Л®ЦщБҪұЯөДТәГжұдОӘЧуөНУТёЯ
CЈ®БҪКФ№ЬЦРПаН¬өДөзј«·ҙУҰКҪКЗЈәFeЈӯ2eЈӯЁDЎъFe2+
DЈ®aКФ№ЬЦР·ўЙъБЛОьСхёҜКҙЈ¬bКФ№ЬЦР·ўЙъБЛОцЗвёҜКҙ
ҪвОцЈәFeУлCј°өзҪвЦКИЬТәРОіЙФӯөзіШЈ¬FeКЗёәј«ЈәFeЈӯ2eЈӯ===Fe2+Ј»CКЗХэј«Ј¬ФЪaЦР·ўЙъОьСхёҜКҙЈ¬aЦРС№ЗҝјхРЎЈ»bЦР·ўЙъОцЗвёҜКҙЈ¬bЦРС№ЗҝФцҙуЈ¬әмД«Л®ЦщТәГжКЗЧуёЯУТөНЎЈ№КСЎBЎЈ
ҙр°ёЈәB
16Ј®(2009ЎӨИ«№ъҫнўт)НјОӘЦұБчөзФҙөзҪвПЎNa2SO4Л®ИЬТәөДЧ°ЦГЎЈНЁөзәуФЪКҜД«өзј«aәНbёҪҪь·ЦұрөОјУТ»өОКҜИпКФТәЈ¬ПВБРКөСйПЦПуЦРХэИ·өДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (ЎЎ)
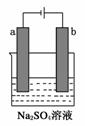
AЈ®ТЭіцЖшМеөДМе»эaөзј«өДРЎУЪbөзј«өД
BЈ®Т»өзј«ТЭіцОЮО¶ЖшМеЈ¬БнТ»өзј«ТЭіцҙМјӨРФЖшО¶ЖшМе
CЈ®aөзј«ёҪҪьіКәмЙ«Ј¬bөзј«ёҪҪьіцПЦА¶Й«
DЈ®aөзј«ёҪҪьіКА¶Й«Ј¬bөзј«ёҪҪьіцПЦәмЙ«
ҪвОцЈәөзҪвNa2SO4ИЬТәКөЦККЗөзҪвЛ®Ј¬ФЪaј«ЙъіЙH2Ј¬aј«ёҪҪьc(OHЈӯ)ФцҙуК№ИЬТәіКА¶Й«Ј¬bј«ЙъіЙO2Ј¬bј«ёҪҪьc(H+)ФцҙуК№ИЬТәіКәмЙ«ЎЈ
ҙр°ёЈәD
15Ј®ИзНјКЗөзҪвCuCl2ИЬТәөДЧ°ЦГЈ¬ЖдЦРcЎўdОӘКҜД«өзј«ЎЈФтПВБРУР№ШөДЕР¶ПХэИ·өДКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (ЎЎ)
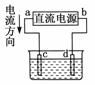
AЈ®aОӘёәј«ЎўbОӘХэј«
BЈ®aОӘСфј«ЎўbОӘТхј«
CЈ®өзҪв№эіМЦРЈ¬dөзј«ЦКБҝФцјУ
DЈ®өзҪв№эіМЦРЈ¬ВИАлЧУЕЁ¶ИІ»ұд
ҙр°ёЈәC
14Ј®°СРҝЖ¬әНМъЖ¬·ЕФЪКўУРПЎКіСОЛ®әН·УМӘКФТә»мәПИЬТәөДІЈБ§ЖчГуЦРЈ¬ҫӯ№эТ»¶ОКұјдәуЈ¬КЧПИ№ЫІмөҪИЬТәұдәмөДЗшУтКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (ЎЎ)
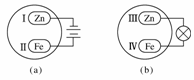
AЈ®ўсәНўуёҪҪьЎЎЎЎЎЎЎЎ  BЈ®ўсәНўфёҪҪь
BЈ®ўсәНўфёҪҪь
CЈ®ўтәНўуёҪҪьЎЎ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ DЈ®ўтәНўфёҪҪь
ҙр°ёЈәB
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com