
11.下列有关化学反应速率的说法正确的是 ( )
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B.100 mL2 mol·L-1的盐酸跟锌片反应时,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢
D.汽车尾气中的NO和CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
[答案] D
10.用纯净的CaCO3和稀HCl反应制CO2,实验过程记录如图所示。下列分析正确的是 ( )

A.OE段表示的反应速率最快
B.EF段表示的反应速率最快
C.GF段收集的CO2最多
D.OG段表示反应速率越来越快
[答案] B
9.将a g块状碳酸钙与足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示。在相同的条件下,将b g(a>b)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是 ( )

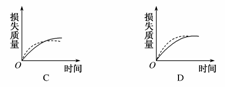
解析:不同形状的碳酸钙跟足量同浓度的盐酸反应时,反应速率块状比粉末状要小,质量大的CaCO3反应产生气体的量也就多。根据这些信息结合曲线图示可得出结论。
答案:C
8.(2009·江苏常州高三月考)在KIO3、KHSO3的酸性混合溶液中加入少量KI和淀粉,不停地搅拌,有下列反应发生:①IO+5I-+6H+===3I2+3H2O ②3I2+3HSO+3H2O===6I-+3SO+9H+。当反应进行到15 min时,溶液突然变为蓝色,随之又很快消失,这一反应称为时钟反应。有人用它来解释生物钟现象。下列有关说法错误的是 ( )
A.在整个反应过程中,起催化作用的物质是KI
B.上述两个反应中,反应速度较大的是②
C.时钟反应的快慢由反应②决定
D.“溶液的颜色迅速变蓝,随之又很快消失”这一现象与①、②的反应速率有关
答案:C
7.某温度下,对可逆反应:2X(g)+Y(g) Z(g)+W(s)ΔH>0的下列叙述正确的是
Z(g)+W(s)ΔH>0的下列叙述正确的是
( )
A.加入少量W,逆反应速度增大
B.升高温度时,正反应速率增大,逆反应速率减小
C.压强不变,充入与反应体系不反应的N2,反应速率减小;体积不变,充入N2,反应速度不变
D.平衡后加入X,上述反应的ΔH增大
答案:C
6.对反应:A+B AB来说,常温下按以下情况进行反应:
AB来说,常温下按以下情况进行反应:
①20 mL溶液中含A、B各0.01 mol
②50 mL溶液中含A、B各0.05 mol
③0.1 mol·L-1的A、B溶液各10 mL
④0.5 mol·L-1的A、B溶液各50 mL
四项反应速率的大小关系是 ( )
A.②>①>④ >③
B.④>③>②>①
>③
B.④>③>②>①
C.①>②>④>③ D.①>②>③>④
答案:A
5.在一密闭容器中充入一定量的H2和N2,经测定反应开始后3 s内的v(H2)=0.3 mol·L-1 ·s-1,则3 s末
·s-1,则3 s末 NH3的浓度为 ( )
NH3的浓度为 ( )
A.0.45 mol· L-1 B.0.6 mol·L-1
L-1 B.0.6 mol·L-1
C.0.9 mol·L-1 D.1.2 mol·L-1
答案:B
4.反应2SO2+O2 2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L
2SO3经一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L -1·s-1,则这段时间为 ( )
-1·s-1,则这段时间为 ( )
A.0.1 s B.2.5 s C.5 s D.10 s
答案:C
3.甲、乙两容器内都进行A→B的反应,甲中每分钟减少4
mol A,乙中每分钟减少2 mol A,则两容器中的反应速率 (  )
)
A.甲快 B.乙快 C.相等 D.无法确定
答案:D
2.把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是 ( )
A.盐酸的浓度 B.铝条的表面积
C.溶液的温度 D.加少量Na2SO4
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com