
5.在一定条件下,向密闭容器中充入30 mL CO和20 mL水蒸气,使其反应,当反应CO(g)+H2O(g) CO2(g)+H2(g)达到平衡时,水蒸气的体积分数与H2的体积分数相等,则下列叙述错误的是 ( )
CO2(g)+H2(g)达到平衡时,水蒸气的体积分数与H2的体积分数相等,则下列叙述错误的是 ( )
A.平衡后CO的体积分数为40%
B.平衡后CO的转化率为25%
C.平衡后水的转化率为5 0%
0%
D.平衡后混合气体的平均相对分子质量为24
解析:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
起始: 30 20 0 0
变化: x x x x
平衡: 30-x 20-x x x
由题意知:20-x=x 故x=10
故平衡后CO的体积分数为×100%=40%
CO的转化率为×100%=33.3%
H2O的转化率为×100%=50%
平衡后混合气体的平均相对分子质量不变,仍为=24,故选B。
答案:B
4.(2009·宁夏高考)将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s) NH3(g)+HI(g)
NH3(g)+HI(g)
②2HI(g) H2(g)+I2(g)
H2(g)+I2(g)
达到平衡时,c(H2 )=0.5
mol·L-1,c(HI)=4 mol·L-1,则此温度下反应①的平衡常数为
)=0.5
mol·L-1,c(HI)=4 mol·L-1,则此温度下反应①的平衡常数为
( )
A.9 B.16 C.20 D.25
答案:C
3.(2009·安徽江南十校模拟)在一个容积为V L的密闭容器中,放入2 L A(g)和1 L B(g),在一定条件下发 生下列反应:3A(g)+B(g)
生下列反应:3A(g)+B(g) nC(g)+2D(
nC(g)+2D( g),达到平衡后,A物质的量浓度减少,混合气的平均摩尔质量增大,则该反应的化学方程式中n的值是 ( )
g),达到平衡后,A物质的量浓度减少,混合气的平均摩尔质量增大,则该反应的化学方程式中n的值是 ( )
A.1 B.2 C.3 D.4
解析:因该反应在密闭容器中进行,反应达到平衡前后气体的总质量保持不变,而平衡后混合气体的平均摩尔质量增大,故混合气体的总物质的量减小,即正反应方向为气体物质的量减小方向,则3+1>n+2,n<2,故A项正确。
答案:A
2.(2009·潍坊模拟)在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
不能确定上述可逆反应在一定条件下已达到化学平衡状态的是 ( )
A.体系的压强不再发生变化
B.v正(CO)=v逆(H2O)
C.生成n mol CO的同时生成n mol H2
D.1 mol H-H键断裂的同时断裂2 mol H-O键
答案:C
1.对于可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
解析:由题意知v正(O2)?v(逆)(NO)=5?4,达到平衡时,v正(NO)=v逆(NO),故A正确;生成NO和消耗NH3,都表示正反应速率,B错;扩大容器体积,各物质的浓度都减小,所以正、逆反应速率都减小,C错;在反应的任意状态总有v正(NH3)?v正(H2O)=4?6,即3v正(NH3)=2v正(H2O),D不正确。
答案:A
16.(12分)对于生态环境的破坏,地表土裸露,大片土地沙漠化,加上春季干旱少雨,所以近年来我国北方地区3、4月份扬尘天气明显增多.特别是2006年的3月26日至28日,由于南下的冷空气所带来的大风,席卷了我国从新疆到沿海的北方大部分地区,出现罕见的沙尘暴天气.据环保部门测定,在北京地区沙尘暴严重时,最大风速达到12 m/s,同时大量的微粒在空中悬浮.
沙尘暴使空气中的悬浮微粒的最高浓度达到5.8×10-6 kg/m3,悬浮微粒的密度为2.0×103 kg/m3其中悬浮微粒的直径小于10-7 m的称为“可吸入颗粒物”,对人体的危害最大.北京地区出现上述沙尘暴时,设悬浮微粒中总体积的1/50为可吸入颗粒物,并认为所有可吸入颗粒物的平均直径为5.0×10-8 m,求1.0 cm3的空气中所含可吸入颗粒物的数量是多少?(计算时可把可吸入颗粒物视为球形,计算结果保留1位有效数字)
解析:沙尘暴天气时,1 m3的空气中所含悬浮微粒的总体积为V== m3=2.9×10-9 m3
那么1 m3中所含的可吸入颗粒物的体积为
V′==5.8×10-11 m3
又因为每一个可吸入颗粒的体积为
V0=πd3≈6.54×10-23 m3
所以1 m3中所含的可吸入颗粒物的数量
n=≈8.9×1011个
所以1.0 cm3的空气中所含可吸入颗粒物的数量为
n′=n×1.0×10-6=8.9×105个≈9×105个.
答案:9×105个
15.(12分)在做“用油膜法估测分子大小”的实验中,所用油酸酒精溶液的浓度为每104 mL溶液中有纯油酸6 mL.用注射器测得1 mL上述溶液有75滴,把1滴该溶液滴入盛水的浅盘里.待水面稳定后,将玻璃板放在浅盘上,用笔在玻璃板上描出油酸的轮廓,再把玻璃板放在坐标纸上,其形状和尺寸如图6所示,坐标中正方形方格的边长为1 cm.试求:
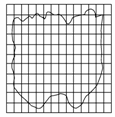
图6
(1)油酸膜的面积是多少平方厘米?
(2)每滴油酸酒精溶液中含有纯油酸的体积.
(3)按以上实验数据估测出油酸分子的直径.
解析:(1)由题图中形状,用补偿法近似处理(大于半格算一格,小于半格舍去),可知油膜实际占小方格99个,那么油膜面积S=99 cm2.
(2)由1 mL溶液中有75滴,1滴溶液的体积为 mL,又每104 mL溶液中有纯油酸6 mL, mL溶液中纯油酸的体积为V= mL=8×10-6 mL.
(3)油酸分子直径d== cm=8.1×10-10 m.
答案:(1)99 cm2 (2)8×10-6 mL (3)8.1×10-10 m
14.(12分)在地球表面上横截面积为3×10-2 m2的圆筒内装0.6 kg的水,太阳光垂直照射了2 min,水温升高了1 ℃.设大气顶层的太阳能只有45%到达地面,试估算出太阳的全部辐射功率.(设太阳与地球表面之间的平均距离为1.5×1011 m)
解析:圆筒内水吸收内能ΔE=cmΔt=4.2×103×0.6×1 J=2.52×103 J
太阳辐射球面的面积S=4πR2=4×3.14×(1.5×1011)2 m2=2.826×1023 m2
太阳辐射的总能量为E=×=× J=5.2752×1028 J
太阳的全部辐射功率为
P== W=4.4×1026 W.
答案:4.4×1026 W
13.(12分)将1 cm3的油酸溶于酒精,制成500 cm3的酒精油酸溶液,已知1滴该溶液的体积是 cm3.现取1滴该溶液滴在水面上,随着酒精溶于水,油酸在水面上形成单分子油膜层,油膜面积为0.4 m2,由此估算分子直径.
解析:每滴酒精油酸溶液中含有的油酸体积V=×10-6× m3=5×10-11 m3
估算出的分子直径d== m=1.3×10-10 m.
答案:1.3×10-10 m
12.(2009年湖北部分重点中学高三二联)某学生在用“油膜法估测分子大小”的实验中,计算结果明显偏大,可能是由于________.
A.油酸未完全散开
B.油酸中含有大量酒精
C.计算油膜面积时,舍去了所有不足一格的方格
D.求每滴体积时,1 mL的溶液的滴数误多记了10滴
解析:(1)用油膜法估测分子直径,是利用油酸的体积与形成的单分子油膜的面积的比值估算分子直径的,分子直径值明显偏大可能的原因有二:一是油酸体积测量值偏大;二是油膜面积测量值偏小.油酸未完全散开和舍去不足一格的方格均会造成油膜面积测量值偏小的结果,故AC两项正确;油酸中酒精更易溶于水,故不会产生影响,B项错;而D项计算每滴溶液中所含油酸的体积偏小,会使分子直径估算值偏小,D项错.
答案:AC
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com