
15.将Na2O2投入FeCl2溶液中, 可观察到的现象是( )
A.生成白色沉淀、有气泡产生 B.生成红褐色沉淀、有气泡产生
C.生成浅绿色沉淀、有气泡产生 D.生成黑色沉淀,有气泡产生
14.下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3;②(NH4)2SO3;③Al2O3;④Al(OH) 3;⑤Al;⑥NH4HCO3;
A.①③④⑤ B.①③④⑤⑥ C.②③④⑤⑥ D.全部
13.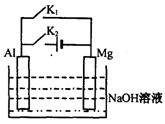 将 Mg 条、 Al 条平行插入一定浓度的 NaOH 溶液中,如图所示用导线连接起来。下列叙述符合事实的是 ( )
将 Mg 条、 Al 条平行插入一定浓度的 NaOH 溶液中,如图所示用导线连接起来。下列叙述符合事实的是 ( )
A.断开 K2,闭合 K1时, Al 电极反应
为: Al+ 4OH-一3e一===AlO2-+ 2H2O
B.断开 K2,闭合 Kl 时,由于 Mg 比 Al 活泼,
故 Mg失去电子被氧化成 Mg2+
C.断开 K1,闭合 K2时,电子由 Mg 向 Al 流动
D.断开 Kl ,闭合 K2时,溶液中立即会有白色沉淀析出
12. 已知:2H2(g)+ O2(g)=2H2O(l) ΔH= -571.6KJ· mol-1
已知:2H2(g)+ O2(g)=2H2O(l) ΔH= -571.6KJ· mol-1

 CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH= -890KJ· mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH= -890KJ· mol-1

 现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是( )
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是( )

 A.1∶1 B.1∶3
A.1∶1 B.1∶3 
 C.1∶4
D.2∶3
C.1∶4
D.2∶3
11.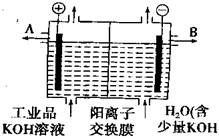 氢氧化钾是重要的工业产品,工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜电解提纯,电解槽内装有阳离子交换膜(只允许阳离子通过),其工业原理如下图所示:
氢氧化钾是重要的工业产品,工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜电解提纯,电解槽内装有阳离子交换膜(只允许阳离子通过),其工业原理如下图所示:
下列有关说法中错误的是( )
A.该电解槽的阳极反应式为4OH--4e-=2H2O+O2↑
B.通电开始后,阴极附近溶液的PH会增大
C.K+可从阳极区进入阴极区和OH-组成KOH
D.除去杂质后的KOH溶液从液体出口A导出
10.羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原,现用15.00mL 0.049 mol/L羟胺的酸性溶液与足量硫酸铁溶液反应(Fe3+转变为Fe2+)。生成的Fe2+ 恰好与24.50mL 0.020 mol/L KMnO4酸性溶液完全作用:
2KMnO4 + 6FeSO4 + 4H2SO4 = 3Fe2(SO4)3 + K2SO4 + 4H2O + 2MnO2,则上述反应中羟胺的氧化产物为( )
A.N2 B.N2O C.NO D.NO2
9.被称为万能还原剂的NaBH4(H元素为-1价)溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑,下列说法中正确的是 ( )
A.NaBH4既是氧化剂又是还原剂
B.NaBH4是还原剂,H2O是氧化剂
C.硼元素被氧化,氢元素被还原
D.被氧化的元素与被还原的元素的物质的量为1︰2
8、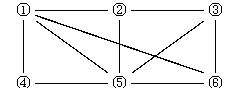 如右图所示,6个编号分别表示六种物质:Al、Fe2O3、NaOH溶液、氢碘酸、NH3、O2。凡是直线相连的两种物质均能
如右图所示,6个编号分别表示六种物质:Al、Fe2O3、NaOH溶液、氢碘酸、NH3、O2。凡是直线相连的两种物质均能
发生化学反应(已知高温时氨气能还原
Fe2O3。)图中①表示的物质是( )
A.Al B.NaOH溶液
C.氢碘酸 D.O2或Fe2O3
7.已知SO32-+I2+H2O=SO42-+2I-+2H+。某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该无色溶液中加入少量溴水,溶液仍呈无色。则下列关于该溶液组成的判断正确的是( )
A.肯定不含I- B.肯定不含Cu2+C.可能含有SO32- D.肯定不含有NH4+
6、现有CuO和Fe2O3组成的混合物a g,向其中加入4.0 mol•L–1硫酸溶液25 mL时恰好完全反应。若将a g原混合物在足量CO中加热,使其充分反应,冷却后剩余固体质量为( )
A.1.6 g B.1.6a g C.(a-0.8) g D.(a-1.6) g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com