
3、滴定管的使用方法
(1).滴定管是一种精确量具(0.01mL),滴定管有酸式和碱式之分,酸式滴定管用来盛酸性溶液(或KMnO4等氧化剂),碱式滴定管只能用来盛碱性溶液。
(2).滴定管使用时,先用自来水洗涤,然后用蒸馏水洗涤滴定管2-3次,再用待盛溶液润洗2-3次后,注入待盛溶液,注意驱赶滴定管尖嘴中的气泡。记录读数V1,读至小数点后第2位(0.01mL)。
(3).进行滴定操作时,左手控制滴定管将滴定管中溶液逐滴滴入锥形瓶中,右手顺时针方向不断地摇动锥形瓶使溶液混匀。滴加到锥形瓶中指示剂颜色发生突变时停止滴加,记录读数V2。
(4).滴加溶液的体积为V2-V1。为了使结果更可靠,应该重复进行三次滴定,最终取三次滴定结果的平均值。
2、中和滴定中的仪器及试剂
主要仪器有:酸式滴定管(不能盛放碱性溶液和HF)、碱式滴定管(不能盛放酸性溶液和KMnO4等氧化剂)、锥形瓶、铁架台、滴定管夹、烧杯、移液管等.
试剂有:标准溶液(已知浓度的某溶液)、待测溶液(要测浓度的某溶液),指示剂。
酸碱中和滴定用酚酞和甲基橙作指示剂,它们的变色范围:
酚酞:____(无色)_____8___(浅红)____10____(红色)_______;
甲基橙:___(红色)_____3.1___(橙色)_____4.4___(黄色)______.
氧化还原反应的滴定常用淀(与I2有关时);用KMnO4作氧化剂进行氧化还原滴定时,不要加指示剂,KMnO4本身就是指示剂.
1、 中和滴定原理(对于强酸、强碱溶液的滴定反应):
强酸与强碱溶液之间的中和反应的实质是:H+ + OH- = H2O , 所以:n(H+) = n(OH-),
即:c(H+)V(H+)=c(OH-)V(OH-),可写成: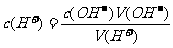
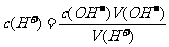 或:
或: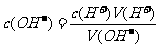
由上式可知:用已知浓度的强酸(或强碱)与未知浓度的强碱(或强酸)反应,如果测出恰好中和时二者的体积,即可由上式计算出未知液的浓度。
3、滴定法的综合应用。
[要点精析]
2、掌握酸碱中和滴定的简单计算。
1、了解酸碱中和滴定基本操作方法、误差分析等。
23.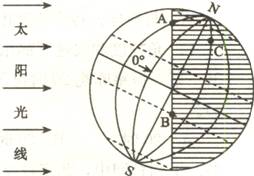 读地球光照图1-1-7,回答下列问题。(12分)
读地球光照图1-1-7,回答下列问题。(12分)
(1)A、B两点此时是__________(填“日出”或“日落”)。
(2)此时,北京时间是________月________日__________时。
(3)再过__________小时,C点将进入子夜。
|

22.读图1-1-6,回答问题。(20分)
(1)将左上图中的A、B、C、D四点标在右上图适当的位置,并注出二分二至的具体日期。
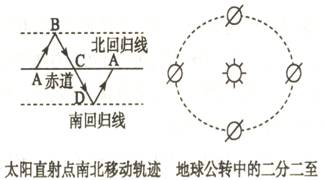 (2)在图中画出地球自转方向。
(2)在图中画出地球自转方向。
|
(4)A→B期间太阳直射点在_______半球,并且正在向_______移动
21.读图1-1-5,完成下列要求。(8分)
|
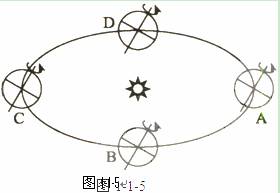
(1)在图中用箭头标出地球公转的方向。
(2)A、B、C、D四点位于近日点附近的是_____(填字母),日期为_______________,地球公转较快的是_________(填字母)。
20. 图l-1-4中横线是0°纬线,虚线是水平运动物体的原始方向,实线箭头是其偏转方向,正确的图示是( B )。
图l-1-4中横线是0°纬线,虚线是水平运动物体的原始方向,实线箭头是其偏转方向,正确的图示是( B )。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com