
读下图,回答1-2题:
1、图中符合下列条件的点为………………………………………………………………( )
①该点以东为西半球,以西为东半球
②该点以北为高纬度,以南为中纬度
A、a点 B、b点 C、c点 D、d点
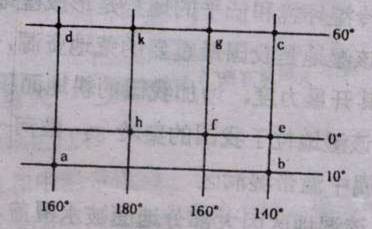
2、图中有关经纬线段长度叙述正确的是…………………………………………………( )
A、gk=hf B、dk>fe C、ad=bc D、ad=de
23.计算以下两小题时,除必须应用所有给出的数据外,还各缺少一个数据,指出该数据的名称(分别以a和b表示),并列出计算式。
⑴在温度为t℃和压强为pPa的情况下,19.5g A 与11.0g B恰好完全反应,生成固体C和3.00L的D气体,计算生成的C的质量(m)。
缺少的数据是:
计算式为m=
⑵0.48g金属镁与10mL盐酸反应,计算生成的H2在标准状况下的体积(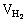 )
)
缺少的数据是:
计算式为:
|
|
A |
B |
C |
D |
E |
F |
G |
|
A |
- |
- |
- |
- |
- |
- |
↓ |
|
B |
- |
- |
- |
- |
↓ |
↓ |
↓ |
|
C |
- |
- |
― |
↓ |
|
↓ |
↓ |
|
D |
- |
|
↓ |
- |
↓ |
↓ |
↓ |
|
E |
- |
↓ |
- |
↓ |
- |
↓ |
- |
|
F |
- |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
|
G |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
- |
22.有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,
“-”表示观察不到明显变化。试回答下面问题。
⑴A的化学式是 ,G的化学式是 。
⑵写出其余几种物质的化学式。B: ,C: ,D: ,E: ,F: 。
21.(6分)在热的稀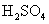 溶液中,溶解了11.4克
溶液中,溶解了11.4克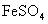 ,当加入50 mL0.5 mol/L
,当加入50 mL0.5 mol/L 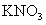 溶液后,使其中的
溶液后,使其中的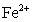 全部转化为
全部转化为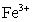 ,
,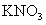 也完全反应,并有
也完全反应,并有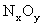 氮氧化物逸出,反应如下:
氮氧化物逸出,反应如下:
( )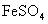 +( )
+( )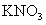 +( )
+( )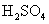
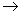
( )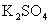 +( )
+( )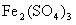 +( )
+( )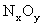 +( )
+( )
(1)推算出x=____________,y=________.
(2)配平该化学方程式.
20.(9分) 按照下图接通线路,反应一段时间后,回答下列问题(假设所提供的电能可以保证电解反应的顺利进行):
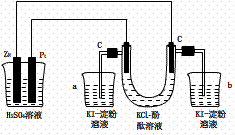
(1)U形管内发生什么现象?
(2)写出有关反应的化学方程式:
(3)在 a、b两烧杯中发生的现象:
(4)如果小烧杯中有0.508g碘析出,大烧杯中负极减轻 g.
19.(4分)有甲、乙、丙、丁四种分散系,它们分别为Fe(OH)3胶体、硅酸胶体、As2S3胶体、NaOH溶液。现将有关实验现象记录如下:
(1)电泳:甲的阳极周围颜色变浅,阴极周围颜色变深。
(2)将一束光通过乙液体,无丁达尔效应。
(3)将乙液体加入到丙液体中,先出现聚沉,后溶液变清。
则甲为_ ;乙为__ __;丙为__ __;丁为___ ___。
18.(6分)按要求回答下列问题:
(1)0.01mol/L的硫酸氢钠溶液的,在其中滴入等体积的pH=12的Ba(OH)2溶液后,所发生反应的离子方程式为 。
(2)配平□Cr2O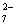 +□I-+□H+--□Cr3++□I2+□H2O
+□I-+□H+--□Cr3++□I2+□H2O
(3)已知1g乙醇完全燃烧生成液态水放出29.72KJ的热量。写出该反应的热化学方程式
17.(4分)理论预测以下物质的物理性质,用>、=、<填空:
(1)CS2的沸点 CCl4的沸点。
(2)NaCl的熔点 MgCl2的熔点。
(3)金属K的硬度 金属Ca的硬度。
(4)金刚石的硬度 晶体硅的硬度。
16.下列离子方程式书写正确的是…………………………………………………………( )
A.氯气通入水中 Cl2+H2O===2H++Cl-+ClO-
B.向偏铝酸钠溶液中滴入少量的硫酸氢钠溶液 AlO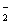 +H++H2O===Al(OH)3↓
+H++H2O===Al(OH)3↓
C.向澄清石灰水中加入过量的碳酸氢钠溶液 Ca2++OH-+HCO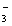 ===CaCO3↓+H2O
===CaCO3↓+H2O
D.向FeCl3溶液中通入H2S气体 2Fe3++S2-===2Fe2++S
第Ⅱ卷(非选择题 共52分)
15.已知下列氧化剂均能氧化+4价的硫元素,欲除去稀硫酸中混有的亚硫酸,以得到纯净的稀硫酸,应选用的最合理的氧化剂是……………………………………………………………… ( )
A.KMnO4 B.Ca(ClO)2 C.H2O2 D.Cl2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com