
5.在9g水中投入1.15g金属钠,则所得溶液中H2O分子和Na+物质的量比是 ( )
A. 10∶1 B. 9∶1 C. 1∶10 C. 90∶1
B.提高训练
4.将钠、铁、镁、铝各取0.1mol,分别投入足量的稀H2SO4中,充分反应后,放出的气体( )
A. 钠最多 B. 一样多 C. 铁最多 D. 铝最多
3. NA代表阿伏加德罗常数,下列说法正确的是 ( )
A. 16g氧气所含的氧原子数为2NA
B. 18g水所含的电子数为NA
C. 2.4g金属镁与盐酸(足量)反应失去的电子数为0.1NA
 D. 17g氨气所含电子数目为10NA
D. 17g氨气所含电子数目为10NA
2.下列情况中含微粒数目最多的是 ( )
A.
1mol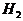 中的H原子 B.
0.5mol
中的H原子 B.
0.5mol 中的电子
中的电子
C.
0.6mol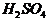 中的O原子 D.
1mol
中的O原子 D.
1mol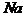 完全反应后失去的电子
完全反应后失去的电子
1.与12.8g 所含有原子数相等的NO的质量为
( )
所含有原子数相等的NO的质量为
( )
A. 3.0g B. 6.0g C. 9.0g D. 18.0g
2.某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为1.96g的该结晶水合物,分别制成溶液。一份加入足量Ba(OH)2溶液,生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色;加热该混合物,逸出能使湿润的红色石蕊试纸变蓝的气体;用稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33 g。另一份加入含0.001 molKMnO4的酸性溶液,MnO4-恰好完全被还原为Mn2+。
请回答以下问题:
⑴该结晶水合物中含有的两种阳离子是 和 ,阴离子是 。
⑵试通过计算确定该结晶水合物的化学式。
思维方法: 。
展望高考:
[针对训练]
A.基础训练
1.设NA为阿佛加德罗常数,下列叙述中正确的是( )
A.46 g NO2 和 N2O4混合气体中含有原子数为3NA
B.标准状况下22.4 L H2 中含中子数为2NA
C.1L 1mol/L醋酸溶液中离子总数为2NA
D.1molMg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子
思维方法: 。
展望高考
3.混合气体的平均相对分子质量的有关计算
⑴基本计算关系: M 
⑵变换计算关系:①M =
②M =
.[例题解析]
[例1]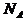 代表阿伏加德罗常数,下列说法正确的是( )
代表阿伏加德罗常数,下列说法正确的是( )
A. 含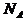 个H原子的
个H原子的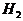 的物质的量为1mol
的物质的量为1mol
B. 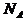 个CO分子和
个CO分子和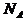 个
个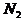 分子质量均为28g
分子质量均为28g
C. 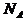 个
个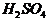 分子和
分子和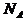 个
个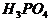 分子中所含氢原子的个数比为1:1
分子中所含氢原子的个数比为1:1
D. 5.6g亚铁离子得到0.2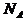 个电子可变成铁原子
个电子可变成铁原子
解题思路: 。
易错点: 。
[例2]标况下,mg气体A和ng气体B的分子数相等,下列说法不正确的是( )
A.同体积的气体A和气体B的质量比为m:n
B.25℃时,1kg气体A和1kg气体B的分子数比为m:n
C.同温同压时气体A和气体B的密度比为n:m
D.标况时,等质量的A和B气体的体积比为n:m
解题思路: 。
易错点: 。
[考题再现]
2.V、n、N之间的计算关系
⑴计算关系: 。
⑵使用范围:
①适用于所有的气体,无论是纯净气体还是混合气体。
②当气体摩尔体积用22.4L·mol-1时必须是标准状况。
1. m、n、N之间的计算关系
⑴计算关系: 。
⑵使用范围:只要物质的组成不变,无论是何状态都可以使用。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com