
3.酯的水解:
2.酯的物理性质:低级酯是具有芳香气味的液体,密度比水 ,难溶于 ,易溶于 。
1.酯的结构式: (其中两个烃基R和R,可不一样,左边的烃基还可以是H)
4、乙酸的用途
乙酸是一种重要的有机化工原料,用途极为广泛,可用于生产醋酸纤维、合成纤维(如维纶)、喷漆溶剂、香料、染料、医药以及农药等。
3、乙酸的化学性质
(1)弱酸性:CH3COOH在水溶液里部分电离产生H+,从而使乙酸具有酸的通性。乙酸能使紫色石蕊试液变红的原因: (电离方程式);乙酸与活泼金属反应放出氢气:
(用化学方程式举一例);与碱发生中和反应: (用化学方程式举一例);与碱性氧化物反应: (用化学方程式举一例);与某些盐反应:
(用化学方程式举一例);此反应证明乙酸的酸性强于碳酸
(2)酯化反应:和酸相互作用生成酯和水的反应叫做酯化反应。

2、乙酸的物理性质
乙酸是无色、有强烈刺激性气味的液体,乙酸在温度低于它的熔点(16.6℃)时会变成冰状晶体,所以无水乙酸又叫 。
1、乙酸的组成与结构
乙酸的分子式:C2H4O2; 结构简式:CH3COOH;官能团是-COOH(羧基)。从结构上看,乙酸是羧基和甲基相联接而成的。由于乙酸分子中羧基和羟基的相互影响,使羟基上的氢更活泼,在水溶液中能部分电离出氢离子,乙酸是一种典型的有机弱酸;羟基的存在也使羧基的加成反应相当困难,很难与氢气等发生加成反应。
3、乙醇的主要用途
乙醇有相当广泛的用途,是一种重要的有机原料,可用它制取乙酸、乙醚等。乙醇还可用作燃料它还是一种有机溶剂,用于溶解树脂、制造染料。在医疗上常用75%(体积分数)的酒精作消毒剂。
3、乙醇的化学性质
(1)乙醇与金属钠反应的化学方程式:2CH3CH2OH+2Na→2CH3CH2ONa +H2↑,此反应属于 ,该反应比钠与水反应要缓和得多,说明乙醇羟基上的氢原子活泼性 水分子中的氢原子,乙醇比水 电离,乙醇是非电解质。
(2)氧化反应
①乙醇燃烧的化学方程式:CH3CH2OH+3O2  2CO2+3H2O,乙醇燃烧时放出大量的热,常被用作酒精灯和内燃机的 。
2CO2+3H2O,乙醇燃烧时放出大量的热,常被用作酒精灯和内燃机的 。
特别提醒:燃烧消耗氧气的量与乙烯相同,燃烧生成二氧化碳和水的量与乙烷相同。
②乙醇的的化学方程式: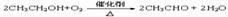 ,如果将光亮的铜丝放在酒精灯火焰上灼烧,然后再趁热插入乙醇中,将发现铜丝先由 色变为
色,插入乙醇中后,又变为 色,可闻到
。
,如果将光亮的铜丝放在酒精灯火焰上灼烧,然后再趁热插入乙醇中,将发现铜丝先由 色变为
色,插入乙醇中后,又变为 色,可闻到
。
③乙醇能被酸性高锰酸钾溶液或酸性(或酸性重铬酸钾)氧化生成乙酸,使溶液 。
(3)乙醇生成乙烯的化学方程式: ,醇发生消去反应时,是羟基与相连接碳原子相邻的碳原子上氢原子一起结合成水脱去,如果羟基相连接碳原子相邻的碳原子上无氢原子,则不能发生消去反应。
,醇发生消去反应时,是羟基与相连接碳原子相邻的碳原子上氢原子一起结合成水脱去,如果羟基相连接碳原子相邻的碳原子上无氢原子,则不能发生消去反应。
2、乙醇的物理性质
乙醇是无色透明而有特殊香味的液体,密度比水小,沸点为78.5 ℃,易挥发,能和水以以任意比混溶,乙醇本身是良好的 ,能溶解多种有机物和无机物。
特别提醒:乙醇由于和水互溶,不能萃取溴水和碘水。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com